- •Вопрос 1.8
- •Задача 1.19
- •Вопрос 1.19
- •Задача 1.26
- •Вопрос 1.26
- •Задача 2.8
- •Вопрос 2.8
- •Задача 2.19
- •Вопрос 2.19
- •Задача 2.26
- •Вопрос 2.26
- •Задача 3.8
- •Вопрос 3.8.
- •Задача 3.19
- •Вопрос 3.19
- •Задача 3.26
- •Вопрос 3.26
- •Вопрос 4.8
- •Задача 4.19
- •Вопрос 4.20
- •Вопрос 4.26
- •Вопрос 4.31
- •Задача 5.8
- •Вопрос 5.8
- •Задача 5.19
- •Вопрос 5.19
- •Вопрос 5.26
- •Вопрос 5.31
- •Задача 6.8.
- •Вопрос 6.8.
- •Вопрос 6.9
- •Задача 6.26
- •Вопрос 6.26
- •Список использованной литературы
Задача 2.19
В процессе расширения кислорода были зафиксированы три равновесных состояния, для которых параметры имеют следующие значения:1) p1=2 МПа, t1=487° С; 2) p2=1 МПа, v2=0,213 м 3/кг; 3)v3=0,3 м3/кг, t3=576° С. Доказать, что этот процесс является политропным, и определить показатель политропы.
Решение
Для доказательства определим значения
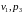 .
.
Считая кислород идеальным газом, из уравнения (51) для одного килограмма газа получим:
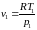 (63)
(63)
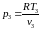 (64)
(64)
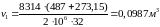
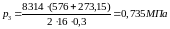
Предположим, что процесс политропный, тогда определим показатель политропы для процесса из выражения
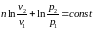 (65)
(65)
Откуда
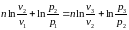 (66)
(66)
Из (64) выразим n
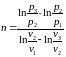 (67)
(67)
Тогда
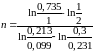 =0,9
=0,9
По определению политропного процесса (68)
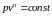 (68)
(68)
Тогда должно выполняться равенство
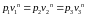 (69)
(69)
Проверим это
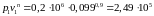
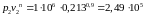
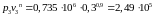
Поскольку равенство выполняется, то этот процесс является политропным
Построим график данного процесса в p-v- и T-s- диаграммах (Рис. 9, Рис. 10).При этом заметим, что 0<n<1, причем ближе к единице, то есть политропа будет приближаться к изотерме.
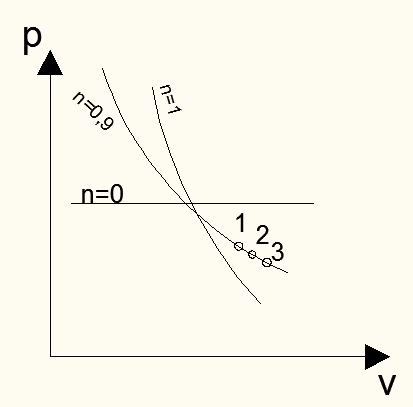
Рис. 9
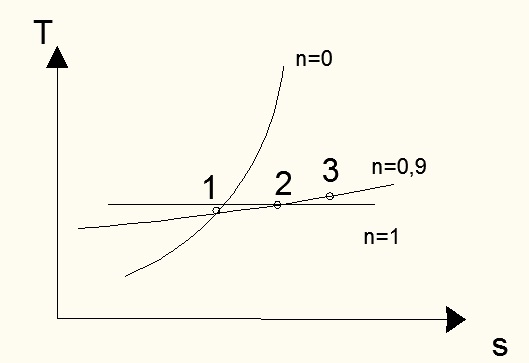
Рис. 10
Вопрос 2.19
Почему при наличии двух источников тепла единственно возможным обратимым циклом является цикл Карно?
Ответ
Изобразим заданный цикл в Ts – диаграмме (Рис. 11)
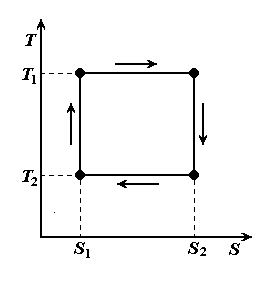
Рис. 11
Цикл Карно — идеальный термодинамический цикл. Тепловая машина Карно, работающая по этому циклу, обладает максимальным КПД из всех машин, у которых максимальная и минимальная температуры осуществляемого цикла совпадают соответственно с максимальной и минимальной температурами цикла Карно.
Одним из важных свойств цикла Карно является его обратимость: он может быть проведён как в прямом, так и в обратном направлении, при этом энтропия адиабатно изолированной (без теплообмена с окружающей средой) системы не меняется.
Для того чтобы цикл был обратимым, из него должна быть исключена передача тепла при наличии разности температур. Значит, передача тепла должна осуществляться в изотермическом процессе. Для того, чтобы менять температуру рабочего тела от температуры нагревателя до температуры холодильника и обратно, необходимо использовать адиабатические процессы (они идут без теплообмена и, значит, тоже не влияют на энтропию). Мы приходим к выводу, что любой обратимый цикл (состоящий только из рабочего тела, нагревателя и холодильника) должен быть составлен из циклов Карно.
Задача 2.26
Используя дифференциальное уравнение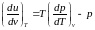 вывести зависимость внутренней энергии
от температуры и удельного объема для
реального газа, подчиняющегося
уравнению состояния Ван-дер-Ваальса
вывести зависимость внутренней энергии
от температуры и удельного объема для
реального газа, подчиняющегося
уравнению состояния Ван-дер-Ваальса
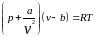 .Определить
для 1 кг углекислоты внутреннюю энергию
при t=400° С и v=0,1
м 3/кг, если а=191 Нм
4/кг2. Теплоемкость для СО2
взять при заданной температуре из табл.5
(см. приложение).
.Определить
для 1 кг углекислоты внутреннюю энергию
при t=400° С и v=0,1
м 3/кг, если а=191 Нм
4/кг2. Теплоемкость для СО2
взять при заданной температуре из табл.5
(см. приложение).
Решение
Из уравнения состояния () следует
выражение
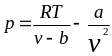 (71)
(71)
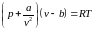 (70)
(70)
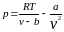 (71)
(71)
Из выражения (71) следует (72)
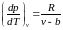 (72)
(72)
Подставим в соотношение () значение производной (72)
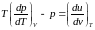 (73)
(73)
Тогда, интегрируя полученное выражение () получим новое выражение ()
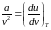 (74)
(74)
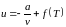 (75)
(75)
Где
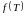 – производная функция от температуры.
Если V
– производная функция от температуры.
Если V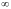 ,
то реальный газ по свойствам стремится
к идеальному и для него справедливо
выражение () Поэтому запишем выражение
(77).Откуда и получим искомое(78)
,
то реальный газ по свойствам стремится
к идеальному и для него справедливо
выражение () Поэтому запишем выражение
(77).Откуда и получим искомое(78)
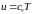 (76)
(76)
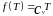 (77)
(77)
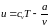 (78)
(78)
При помощи полученного выражения можем найти внутреннюю энергию углекислоты при заданных параметрах. При t =4000 C сvµ = 40,515кДж/(кмоль К)
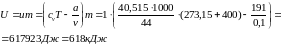
Ответ