
- •Контроль качества лс, содержащих аминокислоты (особенности контроля качества внутриаптечного и заводского изготовления).
- •Содержание
- •Список сокращений
- •Введение
- •1. Лс, содержащие аминокислоты
- •2. Контроль качества лс, содержащих аминокислоты
- •2.1 Внутриаптечный контроль
- •2.2 Анализ лс заводского производства
- •3. Хранение и применение
- •Заключение
- •Список литературы
2. Контроль качества лс, содержащих аминокислоты
2.1 Внутриаптечный контроль
Химический контроль заключается в определении подлинности и количественного содержания лекарственных средств, входящих в состав препаратов.
Для выполнения качественного и количественного анализа препаратов в условиях аптеки используется экспресс-анализ. Характерная особенность данного метода: возможность проведения анализа без изъятия изготовленного лекарства.
Качественный экспресс-анализ проводят на фильтровальной бумаге, предметном или часовых стеклах, на фарфоровой лодочке или в тигле, при этом расход анализируемого вещества составляет от 0,001 до 0,01 г для порошка или от 1 до 5 капель для жидкости.
Количественный экспресс – анализ в условиях аптеки предусматривает определение содержания ингредиентов в лекарствах титриметрическими и физико-химическими методами.
Внутриаптечному контролю подвергаются гамма-аминомасляная кислота, глицин, цистеин.
Испытания на подлинность
Гамма-аминомасляная кислота
Для испытания на подлинность аминокислот используют общую цветную реакцию с нингидрином. В результате реакции образуется аммонийная соль енольной формы дикетогидринденкетогидринамина, имеющая сине-фиолетовую окраску:


Цистеин
Реакция Фоля. При щелочном гидролизе «слабосвязанная сера» в цистеине легко отщепляется, в результате чего образуется сероводород, который, реагируя со щелочью, дает сульфиды натрия или калия. При добавлении ацетата свинца(II) образуется осадок сульфида свинца(II) серо-черного цвета.

Глицин
Реакция комплексообразования. Аминокислоты образуют с катионами тяжелых металлов внутрикомплексные соли. Со свежеприготовленным гидроксидом меди (II) в мягких условиях аминокислоты дают хорошо кристаллизующиеся внутрикомплексные соли меди (II) синего цвета:

Количественный анализ
Фармакопейные статьи (ФС) для количественного определения аминокислот рекомендуют использовать метод кислотно-основного титрования в смешанных растворителях [2]. Данный метод применим в экспресс-анализе для всех аминокислот. Метод основан на реакции нейтрализации. В водной среде титрование аминокислот осуществимо только при использовании специальных методов обнаружения конечной точки (например, потенциометрического метода). Титрант – гидроксид натрия, конечную точку титрования определяют потенциометрически. Fэ=1.

Количественное определение кислоты гамма-аминомасляной выполняют по ФС методом неводного титрования. Метод основан на усилении основных свойств. Титруют раствором хлорной кислоты в среде ледяной уксусной кислоты (индикатор кристаллический фиолетовый). Fэ=1.

2.2 Анализ лс заводского производства
Определение подлинности
Инструментальные методы анализа. Метионин и кислоту глутаминовую идентифицируют с помощью ИК-спектров по совпадению полос поглощения в области 4000-400 см-1 с прилагаемыми к ФС рисунками спектров. УФ-спектр поглощения цистеина имеет максимум поглощения при 236 нм. Удельный показатель поглощения равен 690 [5].
Реакции на подлинность.
Для определения подлинности аминокислот используют реакцию взаимодействия с солями меди (II). Аминокислоты образуют комплексные соединения, имеющие темно-синюю окраску:

Серосодержащие аминокислоты при установлении подлинности подвергают некоторым дополнительным испытаниям. Наличие тиогруппы в молекуле цистеина можно установить цветной реакцией в щелочной среде с нитропруссидом натрия (красно-фиолетовое окрашивание). Для обнаружения тиометильной группы в метионине его сплавляют с 30%-ным раствором гидроксида натрия. Происходит разрушение молекулы метионина с образованием производных меркаптана и сульфидов. Последние можно обнаружить цветной реакцией с нитропруссидом натрия (красно-фиолетовое окрашивание) или по запаху сероводорода и меркаптана, образующихся после добавления серной кислоты:
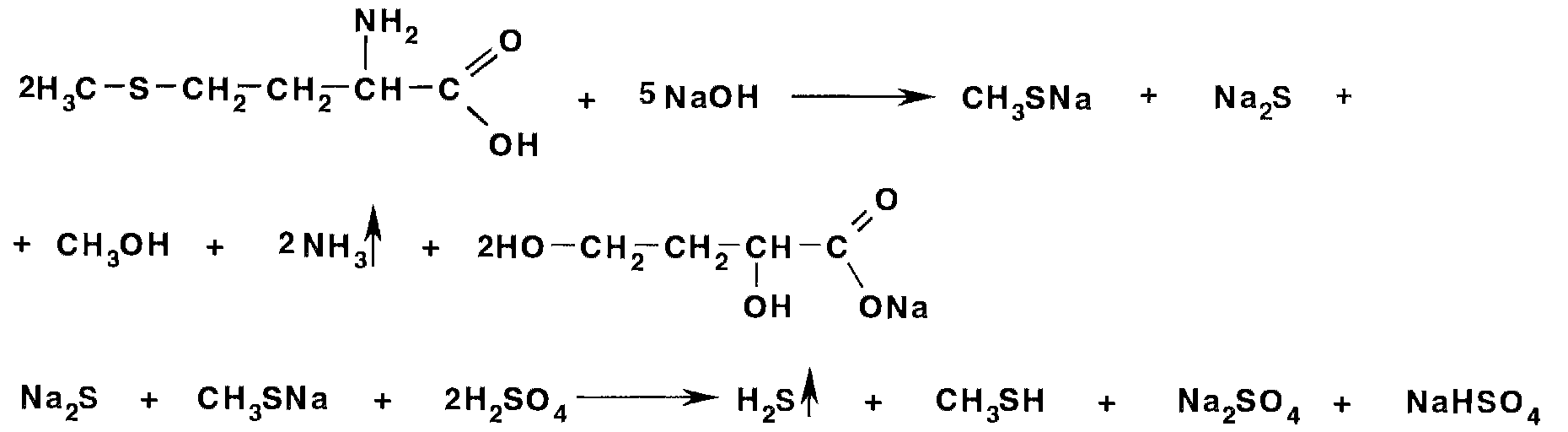
Тиогруппу в молекуле цистеина и ацетилцистеина подтверждают цветной реакцией с хлоридом железа (III) по появлению синего быстро исчезающего окрашивания или используют в качестве реактива нитрит натрия в присутствии уксусной кислоты (красное окрашивание). При действии на растворы цистеина и ацетилцистеина селенистой кислотой выпадает красный осадок. Цистеин при действии м-динитробензолом в присутствии гидроксида натрия приобретает желтое окрашивание. Метионин с 10%-ным раствором ацетата натрия и 2,5%-ным раствором ацетата меди образует сиреневато-синий осадок. Цистеин в этих условиях дает черный осадок, а кислоты гамма-аминомасляная и глутаминовая не осаждаются. Цистеин и пеницилламин восстанавливают фосфорновольфрамовую кислоту, появляется синее окрашивание [5].
При нейтрализации раствора аминокислоты 0,1 М раствором гидроксида натрия по фенолфталеину до розового окрашивания, а затем добавлении нейтрализованного (по этому же индикатору) раствора формальдегида, происходит обесцвечивание полученной смеси. Такое испытание рекомендовано ФС для подтверждения подлинности некоторых аминокислот. Оно основано на связывании аминогруппы формальдегидом до образования N-метилиденового производного (азометина) и демаскировании кислотных свойств аминокислоты:
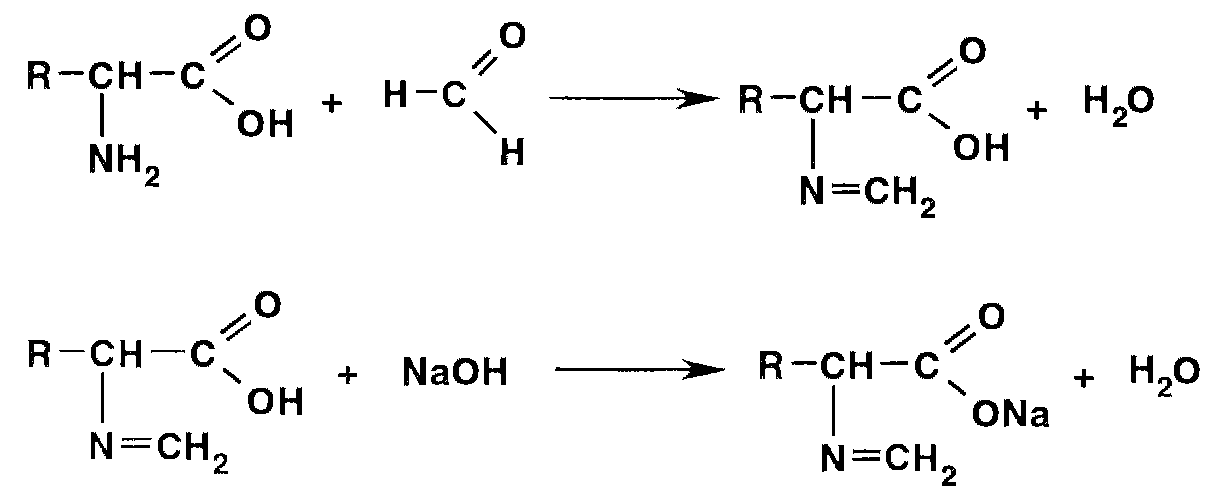
Количественное определение
Для количественного определения аминокислот и их синтетических аналогов могут быть использованы различные методы. Одним из них является метод, основанный на определении азота в органических соединениях (метод Кьельдаля).
Метод основан на предварительной минерализации азотсодержащего органического соединения до гидросульфата аммония. Определение выполняют с помощью прибора, состоящего из колбы Кьельдаля, парообразователя, холодильника, приемника. Используют упрощенный вариант метода Кьельдаля, исключающий стадию минерализации. Методика сводится к гидролизу амида в колбе Кьельдаля 30% раствором гидроксида натрия, отгонке выделяющегося аммиака или амина в приемник и титровании отгона 0,1 М хлороводородной кислотой. Титрант – борная кислота, индикатор – бремкрезоловый зеленый, fэ=1.
![]()

![]()
Параллельно выполняют контрольный опыт [2].
Для количественного определения аминокислот используют также метод Серенсена (формольное титрование). Тритруют раствором формальдегида (нейтрализованного по фенолфталеину). Метод основан на связывании аминогруппы формальдегидом. Fэ=1.
Серосодержащие аминокислоты (цистеин, пеницилламин, метионин) определяют йодометрическим методом. Цистеин и ацетилцистеин титруют в кислой среде 0,1 М раствором йода. Индикатор – крахмал, fэ=1/2. Определение основано на окислении сульфгидрильных групп по общей схеме:
![]()
Метионин (по ФС) предварительно растворяют в смеси растворов монокалийфосфата и дикалийфосфата (одно- и дву- замещенного фосфата калия) в присутствии йодида калия, а затем окисляют 0,1 М раствором йода (индикатор крахмал, fэ=1/2.) по схеме:

Йодхлорометрическое титрование основано на окислении метионина до соответствующего сульфоксида. Титруют йодхлором, индикатор – крахмал. Fэ=1.Избыток титранта оттитровывают натрия тиосульфатом.

