
- •Лабораторная работа № 1 Действие общих реагентов на катионы s-элементов
- •2. Реагент серная кислота Выполнение реакций
- •3. Реагент гидроксид натрия Выполнение реакций
- •4. Реагент гидроксид аммония Выполнение реакций
- •Уравнения реакций
- •5. Реагент карбонат натрия Выполнение реакций
- •6. Реагент сульфид натрия Выполнение реакций
- •Уравнения реакций
- •7. Реагент хромат калия Выполнение реакций
- •Лабораторная работа № 2 Характерные реакции катионов s-элементов
- •I. Характерные реакции катионов калия
- •1. Реагент гексанитрокобальтат-(III)-натрия Na3[Co(no2)6] Выполнение реакций
- •Уравнение реакции
- •Условия проведения
- •II. Характерные реакции катионов натрия
- •1. Реагент дигидроантимонат калия kh2SbO4
- •III. Характерные реакции катионов аммония
- •2. Реагент гидроксид натрия
- •IV. Характерные реакции катионов магния
- •1. Реагент магнезон I
- •Выполнение реакций
- •Выполнение реакции
- •Уравнение реакции
- •Лабораторная работа № 3 Действие общих реагентов на катионы р-элементов
- •3. Реагент серная кислота Выполнение реакций
- •4. Реагент соляная кислота Выполнение реакций
- •5. Реагент гидроксид натрия Выполнение реакций
- •Уравнения реакций
- •6. Реагент гидроксид аммония
- •7. Реагент карбонат натрия Выполнение реакций
- •8. Реагент иодид калия Выполнение реакций
- •Уравнения реакций
- •9. Реагент сульфид натрия Выполнение реакций
- •10. Реагент хромат калия
- •Лабораторная работа № 4 Характерные реакции катионов р-элементов
- •I. Характерные реакции катионов алюминия
- •1. Реагент ализарин Выполнение реакции
- •Уравнение реакции
- •Мешающие ионы
- •II. Характерные реакции катионов свинца
- •1. Реагент иодид калия (реакция «золотого дождя») Выполнение реакции
- •2. Реагент тиосульфат натрия Na2s2o3
- •III. Характерные реакции катионов олова
- •1. Реагент хлорид висмута
- •Открытие катионов олова в смеси катионов р-элементов
- •2. Реагент фосфорномолибденовая кислота
- •3. Реагент нитрат ртути (II)
- •IV. Характерные реакции катионов сурьмы
- •1. Реагент метиловый фиолетовый
- •Выполнение реакции
- •2. Реагент тиосульфат натрия
- •V. Характерные реакции катионов висмута (III)
- •1. Реагент тетрагидроксостаннит натрия Na2[Sn(oh)4]
- •Лабораторная работа № 5 Действие общих реагентов на катионы d-элементов
- •3. Реагент гидроксид натрия Выполнение реакций
- •Уравнения реакций
- •4. Реагент гидроксид аммония Выполнение реакций
- •5. Реагент карбонат натрия Выполнение реакций
- •Уравнения реакций
- •6. Реагент сульфид натрия
- •7. Реагент иодид калия
- •8. Реагент k3[Fe(cn)6] (гексацианоферрат-(III)-калия, красная кровяная соль)
- •9. Реагент k3[Fe(cn)6] (гексацианоферрат-(II)-калия, желтая кровяная соль)
- •Лабораторная работа № 6 Характерные реакции катионов d-элементов
- •I. Характерные реакции катионов кобальта
- •1. Реагент роданид калия Выполнение реакции
- •Уравнение реакции
- •Мешающие ионы
- •II. Характерные реакции катионов меди
- •1. Реагент насыщенный раствор бромида натрия и концентрированная серная кислота (реакция Сабатье)
- •2. Реагент тиосульфат натрия
- •III. Характерные реакции катионов железа
- •1. Реагент желтая кровяная соль k4[Fe(cn)6]
- •2. Реагент роданид калия Выполнение реакций
- •3. Реагент насыщенный раствор тиосульфата натрия
- •IV. Характерные реакции катионов хрома
- •1. Окисление хрома (III) в хром (VI). Реагент персульфат аммония или перманганат калия
- •Уравнения реакций
- •Мешающие ионы
- •V. Характерные реакции катионов ртути
- •1. Реагент иодид калия Выполнение реакции
- •Мешающие ионы
- •VI. Характерные реакции катионов никеля
- •1. Реагент реактив Чугаева (диметилглиоксим) Выполнение реакции
- •Уравнение реакции
- •Мешающие ионы
- •Лабораторная работа № 7 Общие и характерные реакции анионов р-элементов
- •1. Реагент хлорид бария Выполнение реакции
- •2. Реагент нитрат серебра Выполнение реакций
- •3. Реагент концентрированная серная кислота Выполнение реакций
- •Уравнения реакций
- •4. Реагент перманганат калия Выполнение реакций
- •Характерные реакции анионов р-элементов
- •II. Характерные реакции фосфат-ионов
- •1. Реагент магнезиальная смесь (MgCl2, nh4oh, nh4Cl)
- •III. Характерные реакции нитрат-ионов
- •1. Реагент металлический алюминий
- •IV. Характерные реакции хлорид, бромид, иодид-ионов
- •1. Разрушение аммиачных комплексов иодидом калия и конц. Азотной кислотой
- •Мешающие ионы
- •2. Реагент хлорная вода
- •Уравнения реакций
- •3. Реагент нитрит натрия Выполнение реакции
- •Уравнение реакции
- •V. Характерные реакции сульфат-ионов
- •1. Реагент хлорид бария
- •Аналитические реакции анионов р-элементов
Лабораторная работа № 5 Действие общих реагентов на катионы d-элементов
(Co2+, Ni2+, Cu2+, Fe3+, Hg2+, Cr+3)
1. Отметить окраску водных растворов солей катионов d-элементов.
2. Проверить растворимость солей в воде, измерить рH водных растворов солей. Сделать вывод.
3. Реагент гидроксид натрия Выполнение реакций
К 1-2 каплям водных растворов солей прибавить 2-3 капли раствора гидроксида натрия. Отметить цвет выпавших осадков. Проверить растворимость полученных осадков в избытке реагента и в концентрированных кислотах. Выписать из справочника значения произведений растворимости для полученных осадков. Сделать вывод о растворимости гидроксидов в воде и избытке щелочи. Написать молекулярные уравнения реакций.
Уравнения реакций
а) Co2+ + OH– + Cl– = CoOHCl CoOHCl + OH– = Co(OH)2 + Cl–
Осадок основной соли CoOHCl образуется в недостатке щелочи. При добавлении избытка щелочи основная соль превращается в Сo(OH)2. На воздухе Сo(OH)2 окисляется до Сo(OH)3 темно-бурого цвета.
4CoOHCl + O2 + 2H2O = 4Co(OH)3
б) Ni2+ + OH– Ni(OH)2; в) Cu2+ + OH– Cu(OH)2;
г) Fe3+ + OH– Fe(OH)3; д) Hg2+ + OH– HgO + H2O;
е) Cr3+ + OH– Cr(OH)3 Cr(OH)3 + OH– [Cr(OH)6]3–
4. Реагент гидроксид аммония Выполнение реакций
К 2-3 каплям водных растворов солей прибавить 1-2 капли раствора гидроксида аммония. Отметить цвет выпавших осадков. Проверить растворимость осадков в избытке концентрированного раствора аммиака. Написать молекулярные уравнения реакций.
Уравнения реакций
а) Сo2+ + NH4OH Co(OH)2 + NH4+;
Co(OH)2 + NH4OH [Co(NH3)4]2+ + OH– + H2O;
б) Ni2+ + NH4OH Ni(OH)2 + NH4+;
Ni(OH)2 + NH4OH [Ni(NH3)4]2+ + OH– + H2O;
в) Сu2+ + NH4OH Cu(OH)2 + NH4+;
Cu(OH)2 + NH4OH [Cu(NH3)4]2+ + OH– + H2O;
г) Fe3+ + NH4OH Fe(OH)3 + NH4+;
д) Cr+3 + NH4OH Cr(OH)3 + NH4+;

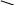 Hg
Hg
е ) Hg2+ + NH4OH + NO3– [NH2 O]NO3 + NH4+ + H2O;
Hg
NH2Hg2ONO3 + NH4OH [Hg(NH3)4](OH)2 + NH4NO3 + H2O.
5. Реагент карбонат натрия Выполнение реакций
К 2-3 каплям водных растворов солей прибавить 2-3 капли раствора реагента. Отметить цвет выпавших осадков. Написать уравнения реакций.
Уравнения реакций
а) При взаимодействии растворов солей железа и хрома с раствором карбоната натрия образуются осадки гидроксидов. Чем объяснить образование данных продуктов?
б) При взаимодействии солей кобальта и никеля с раствором карбоната натрия образуется смесь средних и основных солей (MeCO3, (MeOH)2CO3) в зависимости от условий проведения реакций.
CoCl2 + Na2CO3 + H2O (CoOH)2CO3 + NaCl + CO2
CoCl2 + Na2CO3 CoCO3 + NaCl
в) При действии карбоната натрия на раствор соли меди образуются основные карбонаты, состав которых зависит от условий осаждения mCuCO3 · pCu(OH)2.
CuSO4 + Na2CO3 + H2O Cu(OH)2 · CuCO3 + NaNO3 + CO2
г) При взаимодействии соли ртути с раствором карбоната натрия образуются основные карбонаты переменного состава mHgCO3 · pHgO.
Hg(NO3)2 + Na2CO3 HgCO3 ·3HgO + NaNO3 + CO2
6. Реагент сульфид натрия
Выполнение реакций
К 2-3 каплям водных растворов солей прибавить 2-3 капли раствора сульфида натрия. Отметить цвет выпавших осадков. Написать уравнения реакций. Выписать из справочника значения произведений растворимости для полученных осадков. Сделать вывод о растворимости сульфидов.
