
- •4. Термодинамічні властивості реальних газів і водяної пари
- •4.1 Рівняння стану реальних газів
- •4.2 Водяна пара та її характеристики
- •4.3 Три стадії отримання перегрітої пари
- •4.3.1. Перша стадія - процес підігріву води до температури насичення
- •4.3.2. Друга стадія - процес пароутворення
- •7.3.3 Третя стадія - перегрів пари
- •4.4. Використання „h-s” діаграми для процесів з водяною парою
7.3.3 Третя стадія - перегрів пари
Цей процес характеризується підвищенням температури від tн до температури перегрітої пари t при постійному тиску наданням додаткової теплоти сухій насиченій парі у пароперегрівачі (процес cd на рис. 4). Питомий об’єм пари при перегріві збільшується (v > v'' ). Звідси випливає, що пара, яка має при даному тиску температуру або питомий об’єм більші, ніж відповідні параметри сухої насиченої пари, є перегрітою.
Різниця температур t – tн називається ступенем перегріву пари.
Стан перегрітої пари визначається не одним, а двома незалежними параметрами: тиском р і температурою t, тобто питомий об’єм v = f(p, t).
Для залежності v = f(p, t) отримано велику кількість наближених рівнянь, наприклад, рівняння Вукаловича - Новикова, проте, через їх складність, вони у практичних розрахунках використовуються рідко. Для цього складені таблиці параметрів водяної пари v, h, та s в залежності від тиску р і температури t.
Кількість теплоти, яка необхідна для перегріву 1 кг сухої пари до потрібної температури t при постійному тиску, називається питомою теплотою перегріву qпер. Аналогічно до (7.8) можна записати
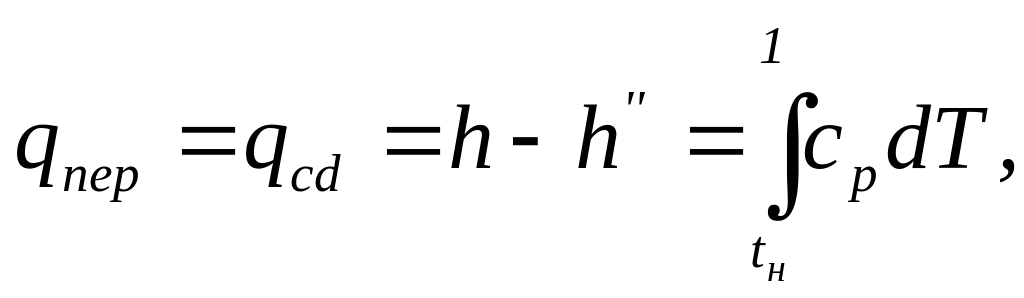 звідки: (19)
звідки: (19)
![]() (20)
(20)
cpm – питома середня ізобарна теплоємність перегрітої пари, яка залежить як від температури, так і від тиску. Згідно з першим законом термодинаміки
![]() тому
тому
![]() (21)
(21)
Зміна питомої ентропії в процесі ізобарного перегріву пари розраховується згідно з виразом (7)
 .
(22)
.
(22)
Процес перегріву пари на „T-s” діаграмі, рис. 4б, зображується логарифмічною кривою cd, а питома теплота перегріву qпер – площею під кривою.
4.4. Використання „h-s” діаграми для процесів з водяною парою
В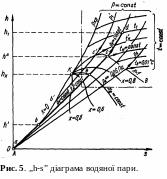
 розрахунках процесів з водяною парою
часто застосовується „h-s”
діаграма, на якій питомі теплота і
ентальпія вимірюються не площами, а
лінійними відрізками на осі „oh”,
див. рис. 5. Діаграму процесів у координатах
„h-s”, див. рис. 5, будують так: на першому
етапі за табличними даними величин h'
, s'
і h''
, s''
будують граничні криві АК
і КВ.
Гранична крива рідини проходить через
початок координат, оскільки при tн
= 0 ºС питомі
ентропія і ентальпія рідини приймаються
рівними нулю.
На другому
етапі наносять ізобари, які на ділянці
насиченої пари, є одночасно ізотермами
і прямими лініями, оскільки на „h-s”
діаграмі кутовий коефіцієнт ізобари
вологої пари (зона фазового переходу)
розрахунках процесів з водяною парою
часто застосовується „h-s”
діаграма, на якій питомі теплота і
ентальпія вимірюються не площами, а
лінійними відрізками на осі „oh”,
див. рис. 5. Діаграму процесів у координатах
„h-s”, див. рис. 5, будують так: на першому
етапі за табличними даними величин h'
, s'
і h''
, s''
будують граничні криві АК
і КВ.
Гранична крива рідини проходить через
початок координат, оскільки при tн
= 0 ºС питомі
ентропія і ентальпія рідини приймаються
рівними нулю.
На другому
етапі наносять ізобари, які на ділянці
насиченої пари, є одночасно ізотермами
і прямими лініями, оскільки на „h-s”
діаграмі кутовий коефіцієнт ізобари
вологої пари (зона фазового переходу)
![]() є сталим. При підвищенні тиску температура
насичення пари збільшується і кут нахилу
ізобар для насиченої пари зростає, тобто
ізобари між граничними кривими є прямими,
що розходяться.
є сталим. При підвищенні тиску температура
насичення пари збільшується і кут нахилу
ізобар для насиченої пари зростає, тобто
ізобари між граничними кривими є прямими,
що розходяться.
Для перегрітої пари (точки справа і зверху кривої КВ) ізобари і ізотерми розділяються, при- чому ізобари підніма- ються вгору у вигляді логарифмічних кри- вих, а ізотерми прямують до горизон- талі. Це пояснюється тим, що із зниженням тиску перегріта пара за своїми властивостям наближається до ідеального газу, питома ентальпія якого залежить лише від температури, тобто лінії t = const. одночасно є лініями h = const. На ділянці вологої пари на „h-s” діаграму наносять лінії однакового ступеня сухості x = const. На цю ж діаграму наносять ізохори, які проходять крутіше ізобар, див. рис. 7.6, де вони показані штриховими лініями.
Переважно для практичного використання будують у великому масштабі робочу частину діаграми, на рис. 5 ця частина обмежена штрих - пунктирною лінією і показана на рис. 6.
