
- •Содержание
- •Введение
- •Возникновение и развитие металлургии
- •История развития металлургии в России. Возникновение и развитие высшего металлургического образования
- •Выдающиеся российские ученые металлурги
- •Павел Петрович Аносов (1799 – 1851 гг.)
- •Павел Матвеевич Обухов
- •Дмитрий Константинович Чернов
- •Владимир Ефимович Грум-Гржимайло
- •Михаил Александрович Павлов
- •Евгений Оскарович Патон (1870 – 1953 гг.)
- •Борис Евгеньевич Патон
- •Николай Тимофеевич Гудцов
- •Иван Павлович Бардин
- •Сергейй Иванович Губкин
- •История развития металлургии и металлургического образования на Урале. Подготовка персонала для металлургических предприятий
- •2.1. Основатель Уральской научно-педагогической школы по обработке металлов давлением
- •Головин Аким Филиппович
- •Развитие теории обработки металлов давлением и работа на заводах
- •Выдрин в.Н. Доктор технических наук, Тарновский и.Я. Доктор технических наук, профессор, основатель кафедры профессор, заведующий кафедрой
- •Создание новых методов расчета формоизменения и силы деформации
- •Красовский н.Н. И Поздеев а.А. Выпускники 1949 г., отличные студенты и спортсмены, стали членами Академии наук ссср
- •Кафедра "Обработка металлов давлением"
- •Основы материаловедения
- •3.1.1. Классификация металлов
- •Средний химический состав земной коры по а.П. Виноградову (мощность 16 км без океана и атмосферы), % мас.
- •3.1.2. Потребительские свойства некоторых металлов и сплавов. Область применения
- •Примерные объемы мирового годового производства некоторых металлов
- •Разбивка нанопорошков по типам
- •3.2. Металлофонд России
- •Кристаллическое строение металлов. Аллотропические или полиморфные превращения
- •От расстояния между ними
- •Элементарной ячейки.
- •Аллотропические формы некоторых металлов
- •3.4. Структура реальных кристаллов
- •3.5. Кристаллизация металлов
- •3.6.1. Диаграмма состояния сплавов, образующих механическую смесь компонентов
- •Механическую смесь компонентов:
- •(Кристаллизации) эвтектики
- •3.6.2. Диаграмма состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии
- •3.6.3. Диаграмма состояния сплавов, образующих ограниченные твердые растворы
- •3.6.4. Диаграмма состояния сплавов, образующих химические соединения
- •Системы Mg-Pb
- •Системы Cu-Zn
- •Свойства и деформация металлов и сплавов
- •Физико-химические и физико-механические свойства металлов и сплавов
- •В таблице Менделеева
- •Физические и механические свойства важнейших металлов
- •3.7.2. Механические свойства металлов и сплавов
- •Деформация металлов и сплавов
- •Сдвига в положение а'в' (б); в - выход дислокации на поверхность кристалла
- •Возврат и рекристаллизация
- •Основы металлургии
- •4.1. Принципиальные основы производства металлов
- •4.2. Руды, подготовка руд к металлургическому переделу
- •4.2.1. Способы добычи руд
- •4.2.2. Цель подготовки руд к металлургическому переделу
- •4.2.3. Дробление и измельчение руд
- •4.2.4. Грохочение и классификация
- •А) в открытом цикле; б) в закрытом
- •4.2.5. Обогащение руд
- •Сепаратора:
- •Для очистки барабана;
- •4.2.6. Обжиг руд
- •Температуры плавления и кипения хлоридов металлов
- •4.2.7. Усреднение
- •4.2.8. Окускование
- •Рекуперации и охлаждения
- •Основы технологии производства важнейших металлов и сплавов
- •5.1. Производство железа – чугунов и сталей
- •5.1.1. Рудная база черной металлургии
- •5.1.2. I стадия - подготовка железных руд к плавке
- •Важнейшие железорудные месторождения России
- •Химические составы железной руды Оленегорского месторождения и полученного из нее концентрата
- •Месторождения
- •5.1.3. II стадия - доменное производство
- •5.1.3.1. Химические процессы в доменной печи
- •5.1.3.2. Управление доменным процессом
- •Калькуляция себестоимости передельного чугуна (в ценах 1985 г.)
- •Калькуляция себестоимости передельного чугуна (в ценах 1985 г.)
- •5.1.3.3. Мероприятия по повышению количества воздуха, вдуваемого в печь
- •5.1.3.4. Устройство и оборудование доменной печи
- •Ленточными конвейерами (галереи обозначены стрелками)
- •В доменную печь:
- •5 .1.3.5. Устройства для подачи и нагрева дутья
- •И «на дутье» (б):
- •5.1.3.6. Устройства для обслуживания горна и уборки чугуна и шлака
- •Огнеупорной массы; 6 - механизм поворота пушки к летке; 7 - защелка; 8 - люк для загрузки огнеупорной массы
- •Доменной печи:
- •5.1.3.7. Использование продуктов доменной плавки
- •5.1.4. III стадия - сталеплавильное производство
- •5.1.4.1. Принципиальные основы сталеплавильного производства
- •Химические составы чугуна и стали
- •5.1.4.2. Шлаковый режим сталеплавильного процесса
- •5.1.4.3. Мартеновское производство стали
- •5.1.4.4. Кислородно-конвертерный способ производства стали
- •Элементов в металле по ходу продувки в кислородном конвертере
- •Конвертерных газов:
- •5.1.4.5. Выплавка стали в конвертерах дуплекс-процессом
- •Транспортного назначения
- •5.1.4.6. Производство стали в электрических печах
- •5.1.4.6. Разливка стали
- •5.1.4.7. Классификация сталей
- •5.1.4.8. Бездоменные способы получения железа
- •Составы восстановительного и колошникового газов шахтиой восстановительной печи, %
- •5.1.4.9. Получение особо чистого железа
- •5.1.4.10. Производство ферросплавов
- •Удельные расходы шихтовых материалов и электроэнергии при выплавке ферросплавов
- •5.1.5. IV стадия - методы повышения качества стали
- •5.1.6. Современный электросталеплавильный цех по производству трубной непрерывнолитой заготовки
- •Технические характеристики мнлз №1
- •5.2. Производство алюминия
- •5.2.1. Рудная база
- •Из высококремиземистых бокситов
- •5.2.2. II стадия - получение а12о3
- •Выщелачивания бокситов:
- •Алюминатного раствора:
- •Перемешиванием; 2- гидроциклон;
- •5.2.3. III стадия - получение металлического алюминия
- •Р ис. 5.50. Схема электролиза для получения алюминия:
- •5.2.4. IV стадия - получение чистого алюминия
- •5.3. Производство меди
- •5.3.1. Рудная база
- •Химический состав медных руд, %
- •5.3.2. I стадия передела - механическое обогащение руд
- •5.3.3. II стадия - выплавка штейна (химическое обогащение)
- •Пирометаллургическим способом
- •Р ис. 5.56. Схема распределения химических процессов по высоте шахтной печи при полупиритной плавке
- •Тепловой баланс полупиритной плавки
- •Р ис. 5.58. Схема печи для взвешенной плавки:
- •Р ис. 5.59. Схема печи Ванюкова:
- •5.3.4. III стадия - получение черновой меди
- •Р ис. 5.60. Схема горизонтального конвертера:
- •5.3.5. IV стадия - получение чистой меди
- •Распределение элементов медных анодов в процессе электролиза, %
- •5.4. Производство титана
- •5.4.1. I стадия - механическое обогащение ильменитовых руд
- •5.4.2. II стадия - химическое обогащение
- •5.4.3. Ill стадия - получение чистых TiCl4 и то2
- •Непрерывного действия:
- •И кипения (верхняя горизонталь) некоторых хлоридов; штриховкой показан температурный диапазон, в котором производится ректификация TiCl4
- •От примесей:
- •Хлоридов; 7 - бак для сбора высококипящих хлоридов; 8 - запорные и регулирующие краны;
- •5.4.4. Получение конечной продукции
- •Восстановлением TiCl4
- •Для алюмотермического производства ферротитаиа:
- •Производство изделий из металлов и сплавов металлургическими методами
- •6.1. Обработка металлов давлением
- •Классификация процессов обработки металлов давлением. Методы омд
- •Классификация процессов листовой штамповки
- •6.1.1.1. Прокатка
- •6.1.1.2. Ковка
- •Боёк; 3 - обрабатываемое изделие; 4 и 5 - верхний и нижний штампы;
- •6.1.1.3. Штамповка
- •6.1.1.4. Прессование
- •6.1.1.5. Волочение
- •6.1.2. Элементы теории обработки металлов давлением
- •Оценка степени деформации металлического тела
- •Напряженное состояние
- •Принцип минимума энергии деформации (наименьшего сопротивления)
- •Элементы теории продольной прокатки
- •Очаг деформации, угол захвата
- •Опережение и отставание
- •Уширение при прокатке
- •Усилие и давление при прокатке
- •Механическое оборудование прокатных цехов
- •Главная линия прокатного стана и ее элементы
- •Вспомогательное оборудование
- •Классификация прокатных станов
- •Для холодной прокатки жести:
- •И рельсобалочных станах:
- •И трамвайные рельсы; 8 - двутавровая балка; 9 - швеллер; 10 - z-образный профиль
- •Технология прокатного производства
- •Нагрев металла перед омд
- •Калибровка прокатных валков
- •Для упрощения рисунка из девяти калибров приведено только четыре
- •Производство заготовок
- •Стана 900/700/500
- •Производство рельсов и балок
- •Производство листового проката
- •Стана холодной прокатки
- •Обозначения те же, что и на рис. 6.23
- •Производство труб
- •6.2. Литейное производство
- •Принципиальная схема изготовления отливок
- •6.2.2. Формовочные материалы и смеси
- •6.2.2.1. Требования, предъявляемые к формовочным и стержневым смесям
- •Свойства компонентов формовочных и стержневых смесей
- •6.2.3. Изготовление форм
- •6.2.4. Заливка форм металлом
- •Основные элементы литниковых систем
- •Типы литниковых систем
- •6.2.5. Литейные сплавы
- •6.2.6. Дефекты отливок
- •6.2.7. Специальные методы литья
- •6.2.7.1. Литье по выплавляемым моделям
- •С выплавляемыми моделями
- •Литье в металлические формы
- •Литье под давлением
- •Литье под регулируемым давлением
- •Центробежное литье
И кипения (верхняя горизонталь) некоторых хлоридов; штриховкой показан температурный диапазон, в котором производится ректификация TiCl4
Ректификация технического TiCl4. Очистка TiCl4 осуществляется последовательно в двух ректификационных колоннах (рис. 5.66). В первой из смеси газов выделяют хлориды с более низкими температурами кипения, чем у TiCl4:SiCl4; GeCl4; СС14. Во второй колонне разделяют TiCl4 и высококипящие хлориды: А1С13; FeCl3; NbCl5; ТаС15.

Рис. 5.66. Схема ректификационной установки для очистки TiCl4
От примесей:
1 - колонна для отделения легколетучих хлоридов; 2 - колонна для отделения высококипящих хлоридов; 3 - подогреватели; 4 - дефлегматоры; 5 - насос: б - бак для сбора низкокипящих
Хлоридов; 7 - бак для сбора высококипящих хлоридов; 8 - запорные и регулирующие краны;
9 - кубы-испарители; 10- неконденсируемые газы (СО2; Cl2; N2; COCI2 и др.); 11 - холодильник
Процесс ректификации ведут в колоннах из нержавеющей стали с дырчатыми тарелками. Технический TiCl4, нагревают до 136°С, подают в среднюю часть первой колонны, в верхней части которой поддерживается температура 60-130°С. В результате охлаждения в дефлегматоре до 100°С образуется конденсат из TiCI4 и других высококипящих хлоридов, который возвращается в процесс - на орошение колонны. Пары низкокипящих хлоридов (SiCl4; GeCl4; СС14) из дефлегматора собираются в специальной емкости после предварительной конденсации в холодильнике. Неконденсируемые газы (СО2; С12; СОС12; N2) направляют на очистку от пыли.
Кубовый остаток, содержащий TiCl4 и примеси высококипящих хлоридов, подают во вторую колонну, в верхней части которой поддерживают температуру 134-136°С. Отбираемый из дефлегматора дистиллят - чистый четыреххлористый титан. Примеси AICl3, FeCl3, ТаС15, NbCl5 остаются в кубовом остатке второй колонны.
Содержание примесей в очищенном TiCl4 составляет 10-3-10-5%.
5.4.4. Получение конечной продукции
Конечной продукцией в титановом производстве могут быть TiO2, чистый металлический титан и ферротитан.
Диоксид титана ТiO2 обычно получают способом «сжигания» четырех- хлористого титана: TiCl4 + O2 = ТiO2 + 2С12. При температурах 900-1000°С эта реакция протекает с достаточно высокой скоростью. Образующийся хлор возвращается на хлорирование титанового сырья. Представляется перспективным в качестве источника тепла использовать кислородную плазму с температурами 6000-10000°С.
Получение металлического титана восстановлением ТiO2 затруднено из- за высокого сродства титана к кислороду Тем более что активно растворяющиеся в титане в ходе предыдущей операции (окисления TiCI4) кислород и азот существенно ухудшают технологические свойства титана.
Основное количество титана производят магниетермическим восстановлением хлорида титана в вакууме или в атмосфере инертных газов: TiCl4(г) + 2Mg(ж) = Ti(тв) + 2MgCl2(ж).
Принципиальная схема производства титана приведена на рис. 5.67.
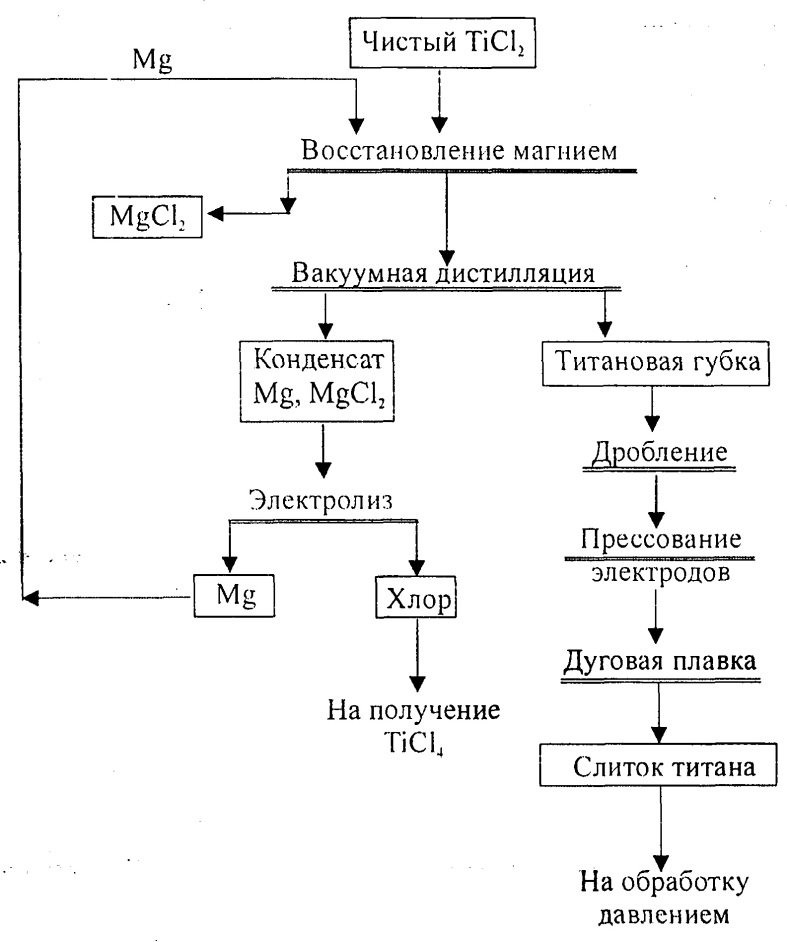
Рис. 5.67. Технологическая схема получения титана магниетермическим
