
- •Лекция № 29 тема: внутриаптечный контроль лекарственных форм с антибиотиками.
- •Анализ лекарственных форм с антибиотиками.
- •Натрия хлорида 0,09
- •Количественное определение
- •Фотолоколориметрический метод
- •Антибиотики. Общая характеристика антибиотиков.
- •С хромотроповой кислотой в присутствии концентрированной h2so4
- •Левомицетин.
- •Тетрациклины.
- •Количественное определение.
Тетрациклины.
Антибиотики тетрациклинового ряда имеют близкое химическое строение и занимают ведущее место среди антибиотиков широкого спектра действия.
Они подавляют размножение грамотрицательных, грамположительных, кислотоустойчивых бактерий, риккетсий.
Благодаря такому широкому спектру антибиотического действия тетрациклины применяются при лечении пневмонии, бруцеллеза, коклюша, дизентерии и других заболеваний.
Ценность тетрациклиновых антибиотиков состоит в том, что они, обладая высокой биологической активностью, имеют относительно низкую токсичность.
В основе химической структуры тетрациклиновых антибиотиков лежит гидронафтацен – конденсированная система из четырех частично гидрированных бензольных колец.
Различаются эти антибиотики лишь характером заместителя в положениях 5 и 7, что видно из представленной ниже химической структуры молекулы тетрациклинов.
CH3
 R
R1
N CH3
R
R1
N CH3
H3C OH
 OH
OH
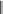 OH
CONH2
OH
CONH2
OH O OH O
Учитывая трудности синтетического получения тетрациклинов, до сих пор в промышленности их получают путем биосинтеза. Тетрациклины близки между собой по химической структуре, поэтому свойства их также повторяют во многом друг друга.
Все антибиотики тетрациклинового ряда имеют амфотерный характер. Основные свойства обусловлены диметиламино – группой.
CH3
N CH3
Кислотные свойства тетрациклины проявляют за счет фенольного гидроксила и главным образом за счет енольных групп.
Являясь амфотерными веществами, тетрациклины растворяются в гидроксидах щелочных металлов и кислотах с образованием солей. Сили тетрациклинов в водных растворах гидролизуются – при стоянии концентрированных растворов выпадает осадок основания.
 CH3
CH3
R R1 N CH3
H3C OH
OH

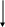

OH CONH2
 CH3
CH3
 H3C CH3
OH O OH O R1
HN+
CH3
H3C CH3
OH O OH O R1
HN+
CH3
R1 N
OH
O-
Na+ CL-
OH CONH2
OH CONH2
OH O
OH O
Ф енольная
гидроксильная группа в молекуле
тетрациклинов обусловливает окрашевание
при взаимодействии с хлоридом железа
(III)
и образование азокрасителя при сочетании
с солями диазония.
енольная
гидроксильная группа в молекуле
тетрациклинов обусловливает окрашевание
при взаимодействии с хлоридом железа
(III)
и образование азокрасителя при сочетании
с солями диазония.

 R N+
N
R N+
N
+ CL-

NH4OH
OH O SO2OH
 R
R
HOO2S N=N

OH O
азокраситель
Характерным свойством тетрациклинов является разложение их с образованием изотетрациклинов, что сопровождается углублением окраски по сравнению с самим антибиотиком.
Кроме общих реакций, присущих всем тетрациклинам, отличить их друг от друга можно по различному окрашиванию при действии концентрированной серной кислоты. При этом образуются ангидротетрациклины, окрашенные для каждого тетрациклина в определенный цвет, например, в случае окситетрациклина образуется пурпурно – красное окрашивание, а в случае тетрациклина – фиолетовое.
Характерной особенностью всех тетрациклинов является способность их флюоресцировать в УФ – области спектра, что используется для подтверждения их подлинности.
Окситетрациклина гидрохлорид
Oxytetracyclini hydrochloridum
С22H24N2O9 *HCL
Окситетрациклина дигидрат
Oxytetracyclini dihydras
C22H24N2O9 * 2H2O
Тетрациклина гидрохлорид
Tetracyclini hydrochloridum
С22H24N2O8 *HCL
Тетрациклин
Tetracyclinum
С22H24N2O8
По внешнему виду эти препараты представляют собой желтые кристаллические порошки без запаха, с горьким вкусом. Мало растворимы в воде (кроме тетрациклина и окситетрациклина гидрохлорида), трудно - в этиловом спирте. Соли тетрациклинов при стоянии мутнеют вследствие постепенного осаждения оснований. При хранении препараты постепенно темнеют, что связано с окислением их кислородом воздуха. Наиболее легко окисление воздухом протекают в водных щелочных растворах, которые при стоянии быстро темнеют.
Доброкачественность препаратов определяется физико – химическими показателями: удельным вращением, удельным показателем поглощения. Определяется кислотнось и щелочность растворов препаратов.
