
- •Основные положения
- •Правило фаз. Закон Гиббса
- •Правило отрезков для двухфазной области
- •Диаграммы состояний с образованием механической смеси компонентов с эвтектикой
- •Диаграммы состояния с ограниченной растворимостью компонентов эвтектикой
- •Диаграммы состояния о ограниченной растворимостью компонентов с перитектикой (рис.4)
- •Диаграммы состояния с устойчивыми химическими соединениями
- •Диаграммы состояния с неустойчивыми химическими соединениями, образующимися по перитектической реакции
- •Диаграммы состояния сплавов с превращениями в твердом состоянии (вторичная кристаллизация)
- •Переменная растворимость компонентов друг в друга
- •Полиморфные превращения
- •Комплексная диаграмма состояния
- •Литература
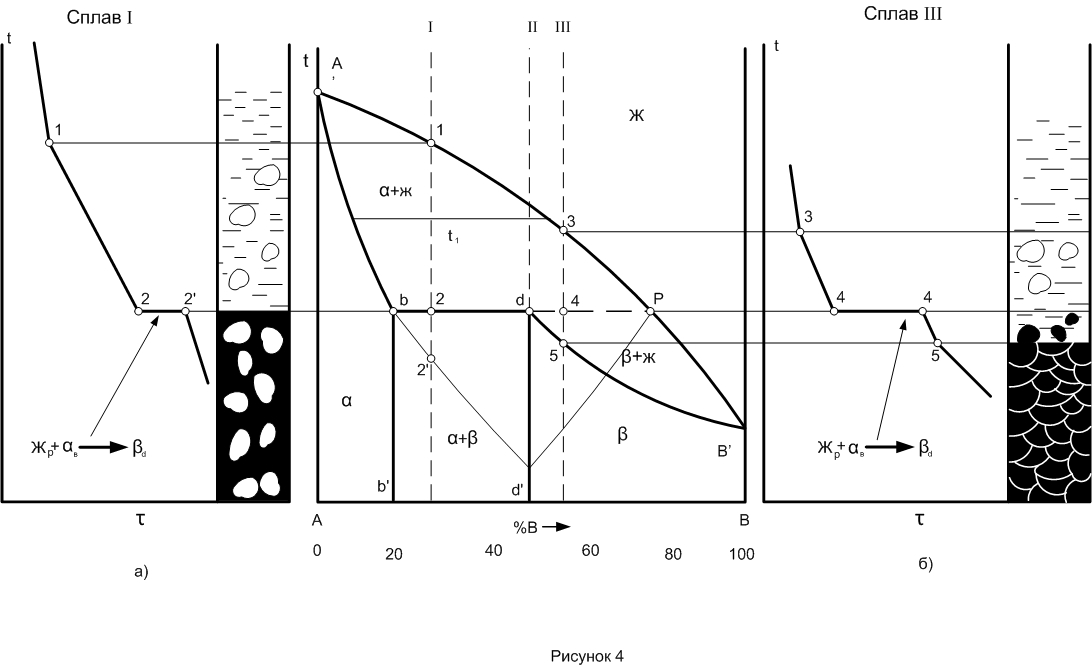
Диаграммы состояния о ограниченной растворимостью компонентов с перитектикой (рис.4)
В
данной системе, как г в предыдущей,
компоненты А и В
ограниченно
растворяются друг в друге. Компонент
В, растворяясь в А, образует твердый
раствор
с предельной растворимостью по линии
сольвус bb’.
Компонент А до 45$ растворяется в В,
образуя твердый раствор
,
о
максимальной растворимостью по линии
сольвус dd’
При температуре
![]() на линии bdp
происходит перитектическая реакция.
Физическая сущность этого превращения
состоит в том, что ранее выпавшие
кристаллы
концентрации b
взаимодействуют с жидкостью концентрации
р, образуя кристаллы твердого раствора
концентрации
d.
на линии bdp
происходит перитектическая реакция.
Физическая сущность этого превращения
состоит в том, что ранее выпавшие
кристаллы
концентрации b
взаимодействуют с жидкостью концентрации
р, образуя кристаллы твердого раствора
концентрации
d.
В сплаве II перитектического состава концентрации dd’ перитектическая реакция завершается образованием однофазной структуры кристаллов (предельная концентрация растворения - d) Количество фазы при этом
![]()
Сплав
II
- единственный, где реакция идет без
остатка фаз. В сплавах левее этого сплава
будет избыточное количество кристаллов
.
Для полной реакции требуется
![]() ,
а в
сплаве I
,
а в
сплаве I
![]() ,
т.е. в сплаве I
кристаллов
больше, чем необходимо для реакции.
Поэтому в результате перитектической
реакции в сплаве останутся избыточные
первичные кристаллы
(рис. 4 а).
,
т.е. в сплаве I
кристаллов
больше, чем необходимо для реакции.
Поэтому в результате перитектической
реакции в сплаве останутся избыточные
первичные кристаллы
(рис. 4 а).
Рассмотрение кристаллизации сплава III (рис. 4 б) показывает, что выделившиеся в интервале температур 3 - 4 кристаллы прореагируют с жидкостью и образуют кристаллы . При дальнейшем охлаждении в интервале температур 4 - 5 из жидкости будет продолжать кристаллизовыватъся - твердый раствор.
Применим правило фаз для сплава I.
1. При температуре t1 он двухфазен ( +Ж)
С = К – Ф + 1 = 2 – 2 + 1 = 1
2. При температуре перитектического превращения присутствуют три фазы: жидкость, и - твердые растворы
С = К – Ф + 1 = 2 – 3 + 1 = 0
Из уравнений видно, что в первом случае кристаллизация должна происходить в интервале температур. На кривой охлаждения появляется точка перегиба I. Перитектическая реакция должна происходить при - постоянной температуре (также как и эвтектическая реакция). На кривой охлаждения появляется горизонтальная площадка 2 - 2'
Диаграммы состояния с устойчивыми химическими соединениями
При
концентрации сплава, соответствующей
точке D,
образуется устойчивое химическое
соединение, состав которого
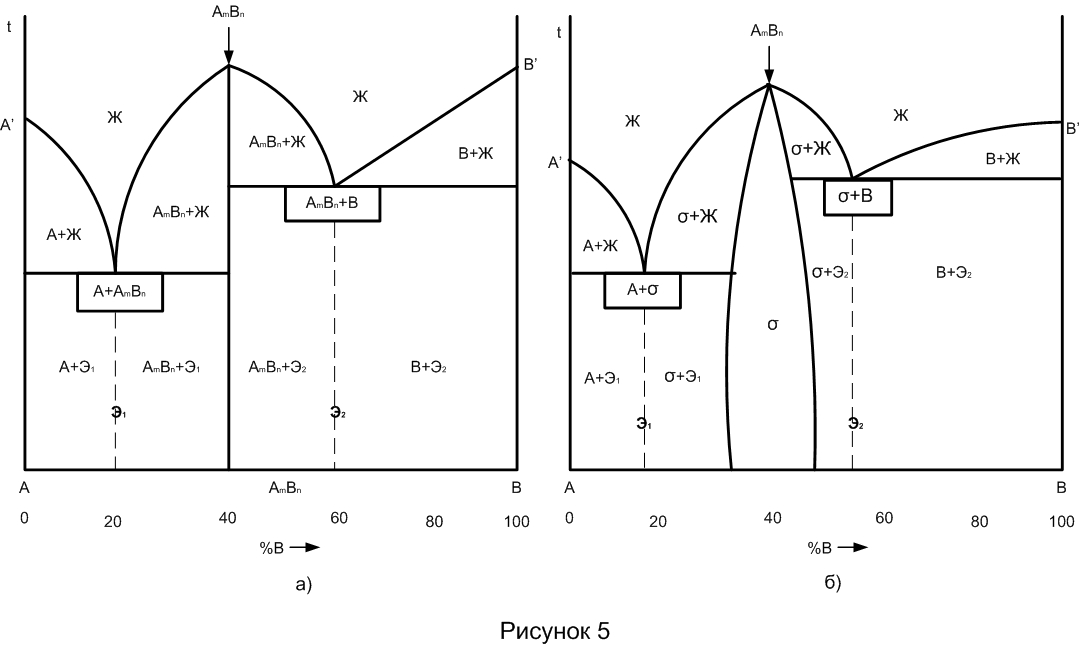
![]() (рис. 5 а). Это устойчивое химическое
соединение сохраняется при нагреве
вплоть до температуры плавления.
(рис. 5 а). Это устойчивое химическое
соединение сохраняется при нагреве
вплоть до температуры плавления.
Эту диаграмму можно рассматривать как две самостоятельные известные диаграммы с эвтектикой.
На
рис. 5 б изображена диаграмма, в которой
устойчивой является промежуточная
фаза
![]() ,
представляющая собой твердый раствор
на базе химического соединения
.
Фазовый и структурный составы сплавов
с учетом эвтектического превращения
изображены на диаграммах (см. рис.
5).
,
представляющая собой твердый раствор
на базе химического соединения
.
Фазовый и структурный составы сплавов
с учетом эвтектического превращения
изображены на диаграммах (см. рис.
5).
Диаграммы состояния с неустойчивыми химическими соединениями, образующимися по перитектической реакции
При
охлаждении сплава I,
при температуре![]() (рис. 6 а) по перитектической реакции
образуется химическое соединение
(рис. 6 а) по перитектической реакции
образуется химическое соединение
![]()
При нагреве химическое соединение устойчиво только до температуры 2. ( ), в то время как весь сплав перейдет в жидкое состояние только при температуре I. Для полного завершения перитектической реакции с образованием химического соединения без остатка фаз требуется

В
доперитектических сплавах (сплав II)
после перитектической реакции оудут
в избытке кристаллы А, так как их
количество в атом сплаве определяется
отношением
![]()
В
заперитектических сплавах (сплав III)
по завершении перитектической реакции
в избытке остается жидкость
![]() ,
При дальнейшем охлаждении в интервале
температур 4 - 5 из жидкости будет
кристаллизовыватъся химическое
соединение
.
Кристаллизация сплава III
завершится на линии аес образованием
эвтектики
,
При дальнейшем охлаждении в интервале
температур 4 - 5 из жидкости будет
кристаллизовыватъся химическое
соединение
.
Кристаллизация сплава III
завершится на линии аес образованием
эвтектики
![]()
На
рис. 6 б по перитектической реакции на
ланий bdp
происходит образование промежуточный
фазы
![]()

