
- •Сірковмісні сполуки
- •Тіоли (тіоспирти, меркаптани) та сульфіди
- •13.1.1 Будова та властивості тіолів.
- •13.1.2 Хімічні властивості тіолів
- •Сульфонові кислоти та їх похідні
- •Будова та властивості сульфонових кислот
- •13.2.3 Хімічні властивості сульфокислот
- •13.2.4 Методи добування сульфокислот
- •В алентні стани азоту
- •12.1.3 Хімічні властивості нітросполук
- •12.1.4 Методи добування нітросполук
- •12.2.1 Класифікація амінів
- •12.2.2 Номенклатура та ізомерія
- •Будова й властивості амінів
- •12.2.5 Методи добування амінів
- •Солі арендіазонію
- •12.3.1 Хімічні властивості
12.2.5 Методи добування амінів
Алкілювання амоніаку (реакція Гофмана).
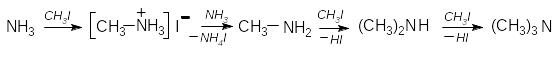
С6H5Cl + 2NH3 С6H5NH2 + NH4Cl
2. Реакції відновлення.
а) відновлення нітросполук - реакція Зініна промисловий метод добування аніліну:
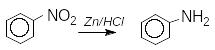
б) відновлення нітрилів:
![]()
в) відновлення оксимів:
![]()
г) відновлення амідів карбонових кислот:
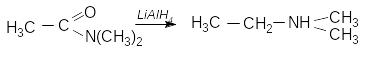
д) відновне амінування:
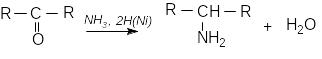
3. Реакція Гофмана (розщеплення амідів карбонових кислот)
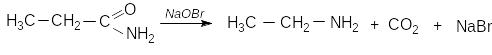
Солі арендіазонію
Вони мають загальну формулу ArN+ N X, де Х = Сl, Br, SO4H, NO3, CH3COO, OH. Назви солей діазонію утворюють подібно назвам солей мінеральних кислот, наприклад:
![]()
фенілдіазоній хлорид п-толілдіазоній бромід
Синтез солей діазонію з первинних ароматичних амінів і нітритної (азотистої) кислоти, що утворюється in situ в кислотному середовищі при дії нітриту натрію, має назву діазотування:
![]()
Реакція є екзотермічною, тому реакційну суміш охолоджують до 0оС.
12.3.1 Хімічні властивості
За допомогою солей діазонію можна здійснити чимало різноманітних перетворень, зокрема таких, які дуже важко здійснити іншими шляхами:
12.3.1.1. Реакції з виділенням азоту.
При цьому відбувається заміщення аміногрупи на різні атоми й групи атомів (водень, галогени, гідрокси-, нітро-, сульфо- та ціаногрупи).
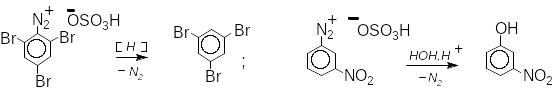
1,3,5-трибромбензен м-нітрофенол
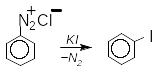
В присутності солей одновалентної міді відбувається перетворення діазосполук на різні похідні аренів - реакція Зандмайєра:

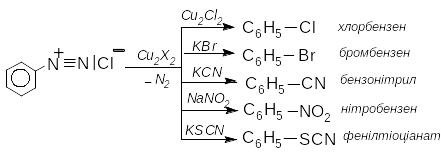
12.3.1.2 Реакції солей діазонія без вилученя азоту.
а) реакції відновлення. У м’яких умовах (SnCl2, Na2SO3, цинковий пил) діазосполуки відновлюються до гідразинів:
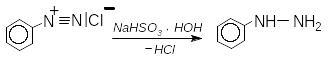 фенілгідразин
(промисловий метод)
фенілгідразин
(промисловий метод)
б) реакції азокопуляції. Це реакція електрофільного заміщення солей діазонію з фенолятами або третинними ариламінами з утворенням азосполук. Електрофілом є діазоній-катіон. Це слабкий електрофіл, він здатний реагувати лише з реакційноздатними сполуками, такими як феноли та ароматичні третинні аміни. Групи ОН, ONa, NR2 виявляють + М-ефект і підвищують електронну густину бензенового ядра. Електроноакцепторні замісники діазоскладової збільшують її реакційну здатність, а електронодонорні – зменшують.
Електрофільне заміщення водневих атомів бензенового ядра є селективним, відбувається в пара-положення відносно гідроксильної або аміногрупи.
В реакціях азосполучення солі діазонію називають діазоскладовою, а амін або фенол – азоскладовою азосполуки..:
![]()
діазоскладова азоскладова азосполука
(4-гідроксиазобензен)
Копуляцію діазосполук з фенолами проводять в слаболужному середовищі тому, що, по-перше, фенолят-аніон реакційноздатніший, а, по-друге, в лужному середовищі фенол краще розчиняється, що дозволяє проводити реакцію в гомогенному середовищі.
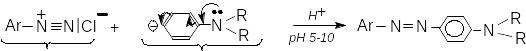
діазоскладова азоскладова азосполука
4-диметиламіноазобензен
Азокопуляцію з амінами проводять в слабокислому або нейтральному середовищі. В сильнокислому середовищі амін утворюватиме амонійну сіль, амонійна група є електроноакцептором і дезактивує бензенове ядро.
Як азоскладові найчастіше використовують наступні сполуки (стрілками позначені місця вступу діазосполуки):

N,N-диметиланілін 1,4-нафтиламіно сульфок-та резорцин -нафтол
Залежно від будови молекули азосполуки мають інтенсивне забарвлення жовтого, жовтогарячого, червоного, синього або зеленого кольору. Їх використовують як барвники, наприклад:

азоскладова діазоскладова діазоскладова азоскладова
Червоний барвник Метилоранж (індикатор)
Загальна формула азосполук: ArNNAr

Назви азосполук утворюють як похідніх від азобензену:
![]()
азобензен 4-нітроазобензен 4-(4-нітрофенілазо)-
N,N-диметиланілін
ХІМІЧНІ ВЛАСТИВОСТІ
Окиснення . Зв’язок N=N більш стійкий до дії окисників, ніж С=С-зв’язок. Азосполуки окиснюються перкислотами:
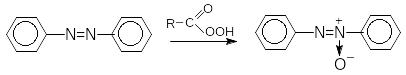
Відновлення. Азобензен відновлюється до гідразоазобензену:
![]()
Гідразобензен в кислому середовищі може перегруповуватися на бензидин (4,4’-діамінобіфеніл) – бензидинове перегрупування
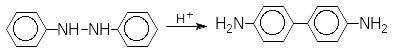
При дії сильних відновлювачив або при каталітичному гідруванні відбувається розрив NN-зв’язку з утворенням двох амінів:
![]()
п-амінофенол п-аміно-N,N-
диметиланілін
