
Лекція 1
Органічна хімія, як наука, існує з початку ХІХ століття, хоч використання органічних сполук для практичних цілей почалося ще дуже давно. Наші пращури знали про спиртове та оцтовокисле бродіння, фарбування індиго та алізарином. їм відомі були найпростіші види перегонки, які застосовувалися, наприклад, для перегонки скипидару. Стародавні люди вміли варити мило із золи та сала, тобто були обізнані з гідролізом естерів і так далі. Починаючи з 16 століття, були виділеними з рослин ефірні олії, добутий діетиловий етер, метиловий спирт, оцтова кислота, винна та янтарна. Далі почався бурхливий розвиток синтетичної органічної хімії. Одночасно розвивалися методи виділення й очищення (екстракція, кристалізація, перегонка й сублімація) та методи якісного аналізу – визначення елементного складу.
Які ж були причини виділення органічної хімії в окрему науку:
По-перше, сьогодні кількість відомих органічних сполук сягає 10 мільйонів, кожного року отримують ще близько 20000 нових органічних сполук ) для порівняння – неорганічних сполук відомо близько 650 тис.). Це пояснюється не тільки тим, що хіміки наполегливо та інтенсивно займаються синтезом та дослідженням органічних сполук, але й унікальною здатністю елементу вуглецю утворювати сполуки, що містять необмежену кількість атомів вуглецю, які сполучені в ланцюги та цикли. Отже органічну хімію можна визначити, як хімію сполук вуглецю.
По-друге, органічні сполуки мають дуже велике значення через їх широке практичне використання. Світ, що нас оточує, побудований з органічних речовин: харчи, паливо, одяг, ліки, барвники, миючи засоби та ще багато чого іншого.
Крім того, органічні сполуки відіграють велику роль в процесах життєдіяльності організмів.
По-третє, властивості та реакційна здатність більшості органічних сполук істотно відрізняється від неорганічних сполук, тому й методи дослідження їх також відрізняються.
Широке практичне застосування органічних сполук визначає цінність органічної хімії для суспільства. На жаль, сьогодні в нашій країні хімічна промисловість в занедбаному стані. А між тим, рівень хімічної освіти колишніх країн СНГ залишається дуже високим. Ми займаємо друге місце за німцями, американці посідають п’яте місце.
Чому знання органічної хімії важливо для спеціалістів-екологів?
Виробництво органічних речовин з одного боку покращує людське життя, а з іншого боку забруднює довкілля та іноді загрожує здоров΄ю людей. За даними всесвітньої організації охорони здоров΄я на сьогодні широко використовується до 500 тис. хімічних сполук. Близько 40 тис. з них мають шкідливі для людини властивості, а 12 тисяч – токсичні. Ці нові токсичні речовини, що не існували в природі, не можуть перероблятися або розкладатися організмами. Їх дія призводить до виникнення невідомих раніше в природі генетичних, токсикологічних, алергічних, ендокринних та інших захворювань.
Я скравим
прикладом може бути препарат ДДТ
(дихлордифенілтрихлоретан).
скравим
прикладом може бути препарат ДДТ
(дихлордифенілтрихлоретан).
За створення цього ефективного пестициду в 1948 році вчені в свій час отримали Нобелівську премію, його світове виробництво протягом 30 років сягало 100 тис. т. на рік; ДДТ спасав ліса та врожаї, але через здатність його накопичуватися в довкіллі та включатися в харчові ланцюги (як з΄ясувалося пізніше), шкоду від його використання навіть важко оцінити. ДДТ зараз знаходять всюди, навіть у молоці жінок, що годують немовлят та пташиних яйцях в Антарктиді. В Радянському Союзі він був заборонений ще в 1970 році, але в деяких країнах Азії та Африки його використовують й досі.
Деякі хімічні сполуки, що відносно нешкідливі, при потраплянні в атмосферу можуть перетворюватися, наприклад, під дією сонячної радіації, на значно токсичніші сполуки. Так головною причиною утворення фотохімічних туманів-смогів у містах-гігантах є олефіни. Смог подразнює очі, горло, спричинює задуху, бронхіальну астму, порушення вітамінного обміну, емфізему легенів. Особливо небезпечний він для дітей.
Накопичення хлорполіциклічних сполук в природі відбувається через широке застосування людиною хлоромістячих пестицидів, з відпадків целюлозо-паперової промисловості та при спалювання сміття. Їх небезпечність полягає в їх високій біологічній активності та здатності до біопереносу в природі. Навіть в найменшій концентрації ці сполуки пригнічують імунну систему організму і зменшують його здатність до адаптацій в змінних умовах зовнішнього світу, виявляють мутагенну, канцерогенну, тератогенну та ембріотоксичну дію, уражають центральну нервову систему, травні органи та ін.
Особливо це стосується діоксинів.
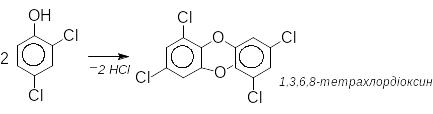
Так продукти хлорування фенолу, наприклад 2,4-дихлорфенол (гербіцид 2,4-Д) виробляють у великих кількостях . Вони й самі забруднюють довкілля, але за певних умов здатні утворювати надзвичайно токсичні діоксини:
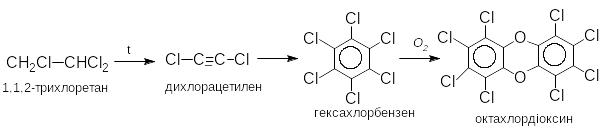 При
нагрівані трихлоретилену (широко
используемый растворитель в химчистке)
може утворюватися дихлорацетилен, який
легко тримеризуеться до гексахлорбензолу.
Останній на повітрі димеризуеться з
утворенням відповідного діоксину:
При
нагрівані трихлоретилену (широко
используемый растворитель в химчистке)
може утворюватися дихлорацетилен, який
легко тримеризуеться до гексахлорбензолу.
Останній на повітрі димеризуеться з
утворенням відповідного діоксину:
Діоксини потрапляють у воду і накопичуються в довкіллі, також вони здатні кумулюватися в організмі людини. Это очень токсичные соединения: подразнюють шкіру, викликають алергічні реакції, знижують імунітет, уражають печінку, викликають утворення і ріст пухлин та негативно впливають на наследственность (мутагенна дія).
Тому, при виробництві органічних хлоропохідних, особливо ароматичних, виключно важливим є контроль за технологічними процесами та ретельною утилізацією відходів виробництва, а також правильне застосування таких сполук.
У виробництві ковбас, беконів та інших мясних продуктів застосовують нітрит натрію, який покращує зовнішній вигляд мясопродуктів, надаючи їм приємний червоний колір, а також запобігає розвитку бактерій, які викликают ботулізм, смертельну хворобу. Проте давно вже було зясовано, що при вживанні цих продуктів в організмі людини утворюються канцерогенні нітрозоаміни. Наприклад, в хотдогах знайдений N-нітрозодиметиламін, а в беконі – N-нітрозопіролідин:

Далі було зясовано, що нітрозоаміни утворюються в організмі людини з цілком натуральних продуктів. Наприклад, шпінат, кормовий буряк та інші овочі містять відносно великі кількості нітратів, які в організмі під дією ферментів відновлюються до нітритів. Багато компонентів їжі є вторинними амінами, які в кислому середовищі шлунку здатні реагувати з нітритами з утворенням нітрозамінів і викликати рак. Зрозуміло, як важливо в сільському господарстві дотримуватися агротехнічних норм при застосуванні добрив.
Крім того існує так званий ефект сумації дії шкідливих речовин, наприклад, сумісна дія ацетону та фенолу, ацетальдегіду та вінілацетату значно небезпечніша, ніж окрема дія тих самих сполук у тієї ж самій концентрації.
Ще більш небезпечним є забруднення гідросфери, тому що процеси регенерації у водному середовищі відбуваються значно повільніше, ніж в повітрі, і джерела забруднень водойм різноманітніші. Особливо гостра проблема стічних вод, які сучасними методами очистити на 100% неможливо. Треба відзначити, що екологічний стан водних басейнів України дуже тяжкий. Особливо це стосується Дніпра, Дністра, Чорного та Азовського морей.
Окремою є проблема утилізації відходів. На Україні ця проблема стає дедалі гострішою. Крім того з 1994 року на Україну почали у великих кількостях надходити імпортні пестициди, поверхнево-активні речовини та інші сполуки, багато з яких заборонені на Заході і використовуються у нас через екологічну неосвіченість.
Отже сучасна екологічна освіта повинна використовувати матеріали багатьох дисциплін, і органічної хімії в тому числі.
Органічна хімія – це наука про сполуки вуглецю з іншими елементами, про синтез, властивості та будову органічних речовин
.Назву “органічна” хімія та “органічні” речовини запровадив шведський хімік Я.Берцеліус, маючи на увазі, що органічна хімія вивчає речовини рослинного та тваринного походження. Ці назви збереглися ще й досі, хоча зміст їх істотно змінився – зараз органічними речовинами вважають не тільки ті, що добуті з природного матеріалу, але й сполуки добуті штучно, за допомогою лабораторних синтезів або промисловими методами. До речі, не всі сполуки вуглецю класифікують як органічні. Наприклад, СО2, HCN, CS2 традиційно відносять до неорганічних речовин.
Зображення молекул органічних сполук
Щоб описати структуру молекули використовують різні хімічні формули: емпіричну, молекулярну та структурну. Молекулярна, або брутто-формула позначає, які атоми в якій кількості входять до складу молекули: С6Н6, СН4О.
В молекулярній формулі спочатку позначають кількість атомів вуглецю та водню, а потім в алфавітному порядку (маються на увазі латинські назви) інші елементи, наприклад, хлористий ацетил – С2Н3СlO.
Молекулярна формула не відображає будову молекули, наприклад:
Етанол і диметиловий етер мають однакову молекулярну формулу: С2Н6О,
але різні структурні формули і зовсім різні хімічні властивості:
СН3СН2ОН та СН3ОСН3
Структурна формула повинна відбивати природу атомів, що входять до складу молекули, їх кількість та послідовність сполучення, а також тип зв’язку між атомами.
Наприклад: бутан, ізобутан, циклобутан

бутен-1, бутен-2, ізобутилен
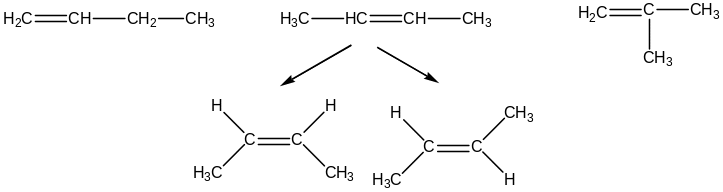
Або етилен, ацетилен.
![]()
С3Н6О: ацетон, пропаналь, метоксиетен, пропен-2-ол (аліловий спирт), циклопропанол, оксетан.
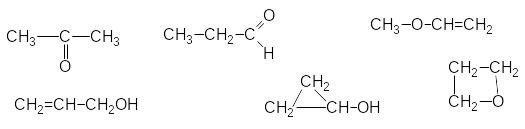
Застосовується скорочений метод написання структурних формул. Вуглецевий скелет молекули зображується тільки валентними зв’язками без позначення атомів вуглецю. Наприклад:


Органічна хімія вивчає процеси перетворення речовин, які мають назву хімічних реакцій. Чим відрізняються реакції органічних сполук від неорганічних?
Неорганічні сполуки, як правило, реагують у вигляді іонів; перебіг реакції відбувається за звичайних умов і майже миттєво. Органічні сполуки реагують у вигляді молекул з руйнуванням одних ковалентних зв’язків та утворенням інших, що вимагає певного часу, підвищення температури, тиску або застосування каталізаторів.
При контакті органічних речовин можуть здійснюватися кілька паралельних реакцій, причому перевага певної реакції над іншими залежить від умов реакції.
Наслідком паралельного перебігу кількох реакцій є зниження виходу продукту реакції, тоді як при неорганічних реакціях вихід майже завжди кількісний (100%).
Ці особливості органічних реакцій визначають спосіб їх запису. Органічні реакції записують не у вигляді рівнянь, а у вигляді схем реакції, в яких увага приділяється не стільки стехіометричному співвідношенню реагентів скільки умовам реакції. В цих схемах вихідні продукти (реагенти) відокремлюються від продуктів реакції стрілкою, над якою записують умови реакції і каталізатори, а під стрілкою із знаком „мінус” – сполуки, що вивільняються під час реакції. Наприклад:

Всю безліч органічних хімічних реакцій класифікують за різними ознаками. Якщо виходити з рівняння хімічної реакції й порівнювати структури реагентів і продуктів реакції, то реакції всіх органічних сполук можна класифікувати таким чином:
За напрямком реакції розрізняють оборотні й необоротні, односпрямовані й багато спрямовані або паралельні:

Прикладом оборотної реакції може бути реакція естерифікації (взаємодія карбонової кислоти та спирту з утворенням естеру):

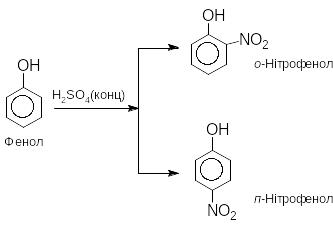 Паралельні
реакції є найхарактернішими в органічній
хімії, наприклад:
Паралельні
реакції є найхарактернішими в органічній
хімії, наприклад:
Органічні
реакції можна класифікувати також за
перебудовою вугл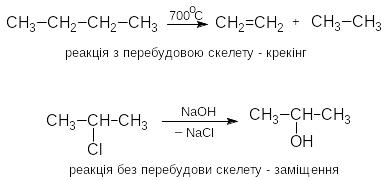 ецевого
скелету:
ецевого
скелету:
Сучасна класифікація органічних сполук ґрунтується на теорії хімічної будови. За основу класифікації прийнято особливості будови вуглецевого ланцюга, тому класифікація органічних сполук за будовою може виглядати таким чином:
-

 Органічні
сполуки
Органічні
сполуки



 Ациклічні
Циклічні
Ациклічні
Циклічні




Насичені Ненасичені Карбоциклічні Гетероциклічні

Аліциклічні Ароматичні Насичені Ненасичені
Аліциклічні або аліфатичні – ц е сполуки з відкритим (незамкненим вуглецевим ланцюгом)
Карбоциклічні -
Органічні сполуки розподілено на класи залежно від складу й будови. Ознакою класу є так звана функційна група, яка визначає типові хімічні властивості сполук цього класу.
Наприклад, наявність карбоксильної групи (-СООН) дає можливість класифікувати сполуку, як карбонову кислоту.
Номенклатура органічних сполук
Найважливіша частина професійної мови хіміків – це точні назви хімічних речовин. Проте в органічній хімії через поширене явище ізомерії недостатньо позначити склад молекули, назва органічної сполуки повинна відображати її структурну будову. Номенклатура повинна дати можливість по назві написати тільки одну структурну формулу. На перший погляд здається, що дуже просто розробити нову систему номенклатури та примусити всіх хіміків використовувати тільки її. Проте номенклатура – це тільки частина мови, в ній існують назви-синоніми й неможливо декретувати введення нової номенклатури та забути про стару, хоча б тому, що при цьому стає незрозумілою вся стара література.
Існування різних систем номенклатури, чисельність назв органічних сполук завдають додаткові труднощі при вивченні органічної хімії. Щоб їх зменшити, треба із самого початку засвоїти деякі засади, які є загальними для всіх існуючих зараз систем номенклатур. Так, наприклад, при складенні назв широко користуються назвами насичених вуглеводнів (алканів) і відповідних одновалентних радикалів (алкілів). Перші чотири вуглеводні з нерозгалуженим ланцюгом мають випадкові тривіальні назви, наступні мають коренем грецькі числівники й закінчення –ан. Назви радикалів утворюються заміною закінчення –ан на –ил (-іл). Розгалужені радикали мають приставку –ізо, використовується також і поняття про первинні, вторинні та третинні вуглецеві атоми. Наприклад, бутильні радикали мають 4 ізомери; 2- нерозгалуженої будови, й 2 – розгалуженої:

На початку розвитку органічної хімії, коли уявлення про природу органічних сполук були зовсім туманні, їм давали випадкові (тривіальні) назви, наприклад, оцтова та мурашині кислоти, винний спирт, сечовина, молочна кислота і багато інших. Тривіальні назви не несуть інформації про хімічну природу сполуки, не розшифровують її будову. Ці назви завантажують пам’ять і утруднюють засвоєння практичного матеріалу. Проте іноді їх зручніше використовувати, особливо, якщо систематична назва сполуки дуже довга.
Історично першою системою структурних назв була раціональна номенклатура, що була відбитком теорії типів, яка панувала в середині минулого століття. До речі, деякі раціональні назви широко застосовуються й нині, особливо в біохімії та медицині. До основи назви раціональної номенклатури положено прототип, з яким порівнюються сполуки. Наприклад:
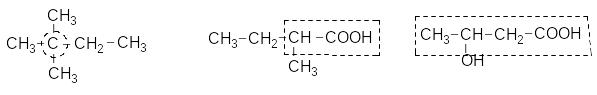
триметилетилметан метилетилоцтова кислота β-оксимасляна к-та
(прототип - метан) (прототип – оцтова к-та) (прототип – масляна к-та)
В 1892 році на Міжнародному конгресі в Женеві була прийнята Женевська номенклатура й тим самим була зроблена спроба надати кожній сполуці єдину офіційну назву. Проте це вдалося зробити тільки для порівняно нескладних сполук. І ось в 1947 році Міжнародною спілкою чистої та прикладної хімії (IUPAC) була створена комісія для упорядкування хімічної номенклатури. Деякі назви цією комісією були визнаними помилковими, а деякі – затвердженими. Ці правила узагальнюють номенклатурну практику цілого століття й, незважаючи на окремі недоліки, є найповнішими та визнаються у всьому світі.
