
- •Порівняльна характеристика аренів
- •Будова ароматичних сполук
- •Будова молекули нафталену
- •Номенклатура і ізомерія
- •Хімічні властивості
- •Реакції електрофільного заміщення
- •Механізм електрофільного заміщення в бензеновому ядрі
- •Орієнтація заміщення в нафталеновому ядрі
- •5.6.1.5 Орієнтація в дизаміщених бензену
- •Реакції заміщення в бічному ланцюгу
Орієнтація заміщення в нафталеновому ядрі
Напрямок заміщення в монозаміщених нафталенах визначається:
Електронною природою орієнтанту
Підвищеною реакційною здатністю в -положеннях
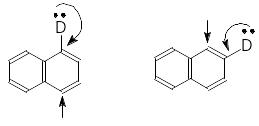
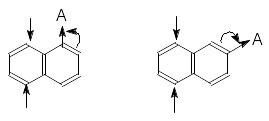
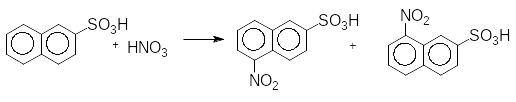
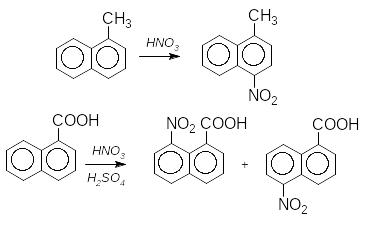
Наприклад, при нітруванні -нафталенсульфонової кислоти утворюється суміш ізомерів:
5.6.1.5 Орієнтація в дизаміщених бензену
Я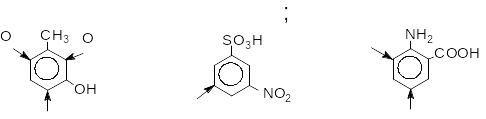 кщо
два замісники в бензеновому ядрі
розташовані таким чином, що орієнтують
в однакові положення, то така орієнтація
має назву узгодженої,
наприклад:
кщо
два замісники в бензеновому ядрі
розташовані таким чином, що орієнтують
в однакові положення, то така орієнтація
має назву узгодженої,
наприклад:
Якщо орієнтуючі дії замісників не співпадають, то ця орієнтація має назву неузгодженої, наприклад:
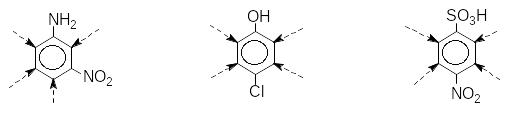
Щоб визначити місце входження наступного замісника слід користуватися наступними правилами:
М
 ісце
входження третього замісника визначається
орієнтантом I роду:
ісце
входження третього замісника визначається
орієнтантом I роду:
2 .
Якщо два замісники є електронодонорами
й розміщені в о-
і п-положеннях
відносно один одного, то вхід третього
замісника визначається сильнішими
орієнтантами.
.
Якщо два замісники є електронодонорами
й розміщені в о-
і п-положеннях
відносно один одного, то вхід третього
замісника визначається сильнішими
орієнтантами.
За силою орієнтуючого впливу замісники можна розташувати в ряд:
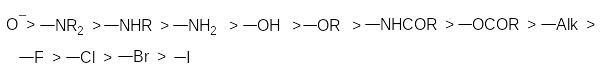
С6Н5
3. Якщо два електроноакцепторні замісники перебувають в о - і п-положеннях, то вхід третього замісника визначається сильнішим орієнтантом. За силою орієнтаційної дії замісники II роду розміщують в ряд:
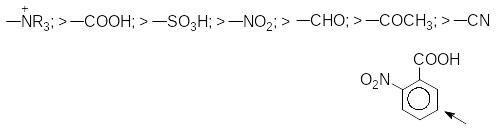
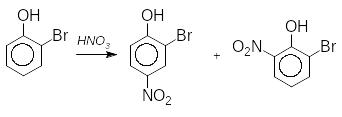
Для приблизного визначення орієнтуючої властивості замісників можна скористатися таблицею активності замісників:
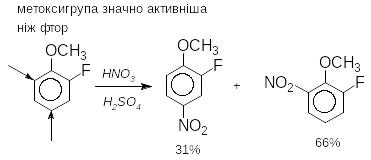
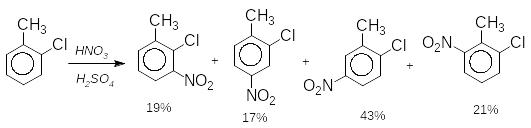
Якщо активність замісників приблизно однакова то в результаті реакції утворюється суміш всіх можливих ізомерів, як в прикладі нітрування о-хлортолуену:
Реакції нуклеофільного заміщення аренам невластиві. Але наявність сильних електроноакцепторних замісників в ароматичному ядрі з одного боку зменшує його реакційну здатність до реакцій електрофільного заміщення, але збільшує можливість заміщення водневих атомів на ціано-, гідрокси- або аміногрупу, тобто до реакцій нуклеофільного заміщення.
Реакції приєднання невластиві аренам. Щоб здійснити реакцію приєднання, спочатку треба подолати енергетичний бар’єр кон’юґованої системи -електронів. Тому ці реакції відбуваються з багатими на енергію реагентами – частинками з неспареними електронами або вільними радикалами.
Можна здійснити каталітичне гідрування
а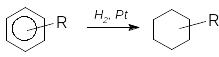 )
Бензен та його похідні гідруються над
нікелевими або платиновими каталізаторами
до відповідних циклогексанів:
)
Бензен та його похідні гідруються над
нікелевими або платиновими каталізаторами
до відповідних циклогексанів:
Я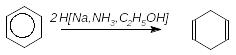 к
виняток отримано 1,4-циклогексадієн
відновленням натрієм у рідкому стані
в присутності етанолу:
к
виняток отримано 1,4-циклогексадієн
відновленням натрієм у рідкому стані
в присутності етанолу:
Нафтален відновлюється легше. При каталітичному гідруванні нафталену спочатку гідрується одне ароматичне ядро з утворенням тетрагідронафталену (тетраліну), який при дещо вищій температурі гідрується далі:
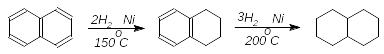
нафтален тетралін декалін
Обидва ці вуглеводні використовують як висококиплячі розчинники (200 С) для жирів, лакофарбних матеріалів, гуми, каучуків, синтетичних смол.
Антрацен і фенантрен гідруються так само поступово. Спочатку відбувається приєднання водню в положеннях 9,10, а потім відбувається відновлення ароматичних ядер.
На відміну від бензену, нафтален, фенантрен і антрацен відновлюються воднем у мить його виділення:
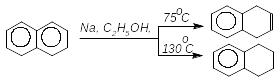 !,4-дигідронафтален
!,4-дигідронафтален
1,2,3,4-тетрагідронафтален
б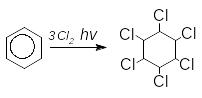 )
Хлор і бром приєднуються до бензену при
УФ-опромінюванні за відсутністю
каталізаторів:
)
Хлор і бром приєднуються до бензену при
УФ-опромінюванні за відсутністю
каталізаторів:
гексахлорциклогексан
При звичайній або зниженій температурі за відсутністю каталізатору нафтален приєднує хлор з утворенням продукту 1,4-приєднання:
в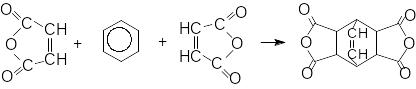 )
При УФ-опромінюванні бензен також має
здатність вступати до реакції
Дільса-Альдера з приєднанням малеїнового
ангідриду:
)
При УФ-опромінюванні бензен також має
здатність вступати до реакції
Дільса-Альдера з приєднанням малеїнового
ангідриду:
Антрацен легко приєднує малеїновий ангідрид та інші дієнофіли:
Окиснення:
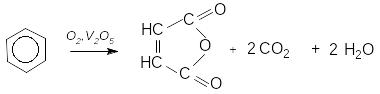
За звичайних умов бензен стійкий до дії окисників. Він не знебарвлює водний розчин перманганату калію навіть при тривалому нагріванні. Лише при нагріванні його в присутності каталізатора відбувається часткове окиснення до малеїнового ангідриду:
Гомологи бензену, на відміну від бензену, легко окиснюються до карбонових кислот, причому, незалежно від довжини бічного вуглецевого ланцюга, карбоксильна група кислоти, що утворюється, завжди сполучена з бензеновим ядром:
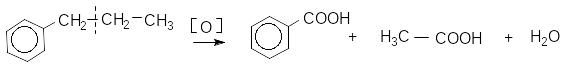
пропілбензен бензойна кислота оцтова кислота
В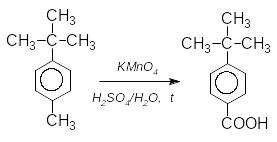 иняток
– наявність замісника з четвертинним
вуглецевим атомом. Через відсутність
бензольного водневого атома, він не
окиснюється при нагріванні з розчином
перманганату калію:
иняток
– наявність замісника з четвертинним
вуглецевим атомом. Через відсутність
бензольного водневого атома, він не
окиснюється при нагріванні з розчином
перманганату калію:
4-трет-бутилтолуен 4-трет-бутилбензойна кислота
Під дією озону відбувається утворення нестійких озонідів:

гліоксаль
На відміну від бензену, який за звичайних умов стійкий до дії окисників, нафтален, антрацен і фенантрен окиснюються різними окисниками:

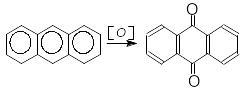 !,4-нафтохінон
фталевий
ангідрид
!,4-нафтохінон
фталевий
ангідрид
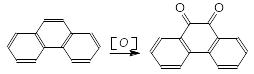
антрацен 9,10-антрахінон фенантрен 9,10-фенантренхінон
Гомологи нафталенів окиснюются до карбонових кислот:
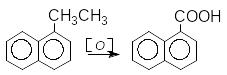
1-етилнафтален нафталенкарбонова к-та-1
Більш чутливим до дії окисників є нафталенове ядро, на відміну від гомологів бензену.:
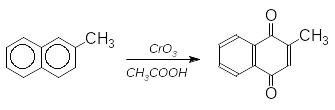
2-метилнафтален 2-метилнафтохінон-1,4
Заміщені нафталени окиснюються залежно від властивостей замісника: при наявності електронодонорного замісника окиснюється те саме ароматичне ядро, що містить цей замісник, при наявності електроноакцепторного замісника, незаміщене ядро:
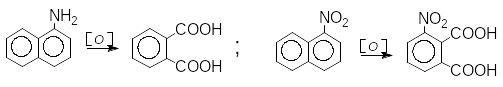
-нафтиламін о-фталева -нітронафтален 3-нітрофталева
кислота кислота
