2.2. Основное уравнение молекулярно-кинетической теории газов
Это уравнение устанавливает взаимосвязь между давлением газа (термодинамическим параметром) и средней кинетической энергией теплового движения его молекул (механической характеристикой системы). С точки зрения молекулярно-кинетической теории, давление газа на стенку сосуда является результатом многочисленных ударов молекул газа о стенку. При огромном числе молекул, находящихся в сосуде, одновременно будет производиться огромное количество ударов о стенки. Поэтому достаточно малые и очень быстро меняющиеся силы, порождаемые отдельными ударами, будут складываться практически в постоянную силу, давления, действующую на каждую единицу площади стенок сосуда.
Найдем давление идеального газа на стенку сосуда. Сила, с которой газ действует на стенку, определяется упругими столкновениями молекул со стенкой и, в соответствии со вторым основным законом динамики, равна импульсу, передаваемому стенке всеми молекулами за единицу времени, а давление газа найдется как отношение этой силы к площади стенки. При этом будем считать, что идеальный газ – это система, состоящая из исчезающе малых по размерам твердых шариков конечной массы, хаотически движущихся во всем доступном им объеме, не взаимодействующих на расстоянии и сталкивающихся между собой и со стенками сосуда по законам соударения упругих шаров.
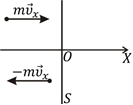
Выделим на
поверхности сосуда, в который газ
заключен, малую площадку S.
Вследствие малости ее можно считать
плоской. Введем декартову систему
координат, направив ось X
перпендикулярно выделенной площадке,
как показано на рис. 2.2. С площадкой S
могут столкнуться только те молекулы,
которые летят в ее направлении, т.е. у
которых x-компонента
скорости
 Предположим сначала, что все подлетающие
к площадке молекулы имеют одно и то же
значение этой x-компоненты.
При упругом ударе молекулы о площадку
знак этой скорости, а значит, и импульса
меняются на противоположный, не изменяя
своей величины. Изменение импульса
одной молекулы при столкновении с
площадкой составит
Предположим сначала, что все подлетающие
к площадке молекулы имеют одно и то же
значение этой x-компоненты.
При упругом ударе молекулы о площадку
знак этой скорости, а значит, и импульса
меняются на противоположный, не изменяя
своей величины. Изменение импульса
одной молекулы при столкновении с
площадкой составит
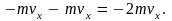 Здесь
–
масса молекулы. Импульс, переданный
площадке этой молекулой, в соответствии
с законом сохранения импульса, будет
Здесь
–
масса молекулы. Импульс, переданный
площадке этой молекулой, в соответствии
с законом сохранения импульса, будет

Рис. 2.2 |
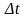 до
площадки долетят и столкнутся с ней
только те молекулы, которые в начальный
момент находились от площадки на
расстоянии, не большем vxΔt,
и занимали объем
до
площадки долетят и столкнутся с ней
только те молекулы, которые в начальный
момент находились от площадки на
расстоянии, не большем vxΔt,
и занимали объем
 слоя пространства, примыкающего к
площадке. Число ударов молекул о площадку
за время
будет
равно числу молекул, находящихся внутри
этого слоя, т.е.
слоя пространства, примыкающего к
площадке. Число ударов молекул о площадку
за время
будет
равно числу молекул, находящихся внутри
этого слоя, т.е.
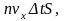 где n –
концентрация молекул газа. Импульс,
переданный площадке этими молекулами,
составит
где n –
концентрация молекул газа. Импульс,
переданный площадке этими молекулами,
составит

Предположение,
что все молекулы газа имеют скорости с
одной и той же компонентой vx,
конечно, не верно. Скорости vx
у всех молекул разные и каждая молекула,
ударяясь о площадку, вносит свой вклад.
Учтем, однако, что нам требуется оценить
только коллективный эффект, возникающий
от столкновения с площадкой большого
числа молекул. Этот эффект описывается
средним значением полученного выше
выражения. Именно средний импульс
определяет силу давления молекул на
стенку сосуда. Усредняя это выражение
по всем
 ,
примем во внимание, что не все молекулы
с одним и тем же значением
сталкиваются с площадкой, а только те
из них, у которых x-компонента
vx
> 0. Учтем также,
что в равновесном состоянии движение
молекул является полностью беспорядочным.
Поэтому число молекул, летящих к площадке
S
и от нее, в среднем одно и то же. Это
означает, что среднее значение
для vx
> 0 вдвое меньше
среднего значения
для всех vx.
Таким образом, оказывается, что за время
площадка S
со стороны газа получит импульс, в
среднем равный
,
примем во внимание, что не все молекулы
с одним и тем же значением
сталкиваются с площадкой, а только те
из них, у которых x-компонента
vx
> 0. Учтем также,
что в равновесном состоянии движение
молекул является полностью беспорядочным.
Поэтому число молекул, летящих к площадке
S
и от нее, в среднем одно и то же. Это
означает, что среднее значение
для vx
> 0 вдвое меньше
среднего значения
для всех vx.
Таким образом, оказывается, что за время
площадка S
со стороны газа получит импульс, в
среднем равный
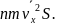 Разделив этот импульс на промежуток
времени
,
получим среднее значение силы, с которой
газ действует на данную площадку, а
разделив затем эту силу на площадь
площадки S,
найдем давление, оказываемое газом на
площадку:
Разделив этот импульс на промежуток
времени
,
получим среднее значение силы, с которой
газ действует на данную площадку, а
разделив затем эту силу на площадь
площадки S,
найдем давление, оказываемое газом на
площадку:

Вследствие
беспорядочности движения молекул
средние значения квадратов компонент
вектора скорости будут одинаковы. А так
как
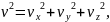 то для средних значений всех квадратов
компонент скорости будем иметь
то для средних значений всех квадратов
компонент скорости будем иметь
 (2.5)
(2.5)
С учетом этого находим
 (2.6)
(2.6)
Отсюда видно, что давление идеального газа определяется только концентрацией молекул, их массой и средним значением квадрата скорости молекулы.
Правую часть этой
формулы можно записать в виде
 где
где
 – среднее
значение кинетической энергии
поступательного движения молекулы.
Учитывая это, получим
– среднее
значение кинетической энергии
поступательного движения молекулы.
Учитывая это, получим
 (2.7)
(2.7)
Это и есть основное уравнение молекулярно-кинетической теории газов. Основным его называют потому, что это первое соотношение, которое было получено на основе представления о газе как о совокупности быстро и хаотически движущихся частиц. Его называют также уравнением Клаузиуса.