
- •Міністерство освіти і науки, молоді і спорту україни
- •1 Пояснювальна записка
- •1.1 Мета і задачі дисципліни. Структурні модулі
- •1.2 Тематичний план самостійної роботи
- •1.3 Рекомендована література
- •2 Підготовка до лабораторних (практичних) занять
- •3 Підготовка до семінарських занять
- •4 Теми для самостійного опрацювання
- •4.1 Викладення теоретичного матеріалу, завдання для перевірки засвоєння нового матеріалу розділ 1 оcнови теорії теплопередачі
- •Тема 1.1 Теплопровідність
- •Тема 1.2 Конвекційний теплообмін
- •Тема 1.3 Теплообмін випромінюванням
- •Тема 1.4 Теплопередача
- •Розділ 2 технічна термодинаміка
- •Тема 2.2 Поняття про термодинамічний процес. Закони ідеального газу.
- •Питання 2 Визначення параметрів при заданні суміші масовими та об’ємними частками
- •Тема 2.3 Теплоємність. Визначення кількості теплоти
- •Тема 2.4 Перший закон термодинаміки. Ентальпія
- •Тема 2.6 Другий закон термодинаміки. Ентропія. - діаграма. Прямий і
- •Тема 2.7 Реальні гази. Водяна пара
- •Тема 2.9 Цикли паросилових установок
- •4.2 Перелік запитань для підготовки до модульного і рейтингового контролю
Тема 2.7 Реальні гази. Водяна пара
Самостійна робота № 10 Процес пароутворення в Тs– діаграмі. іs- діаграма водяної пари.
Графічне зображення термодинамічних процесів водяної пари в Рv -,
Ts– та іs- діаграмах (4 год.)
Питання 1 Процес пароутворення в Тs– діаграмі
Ц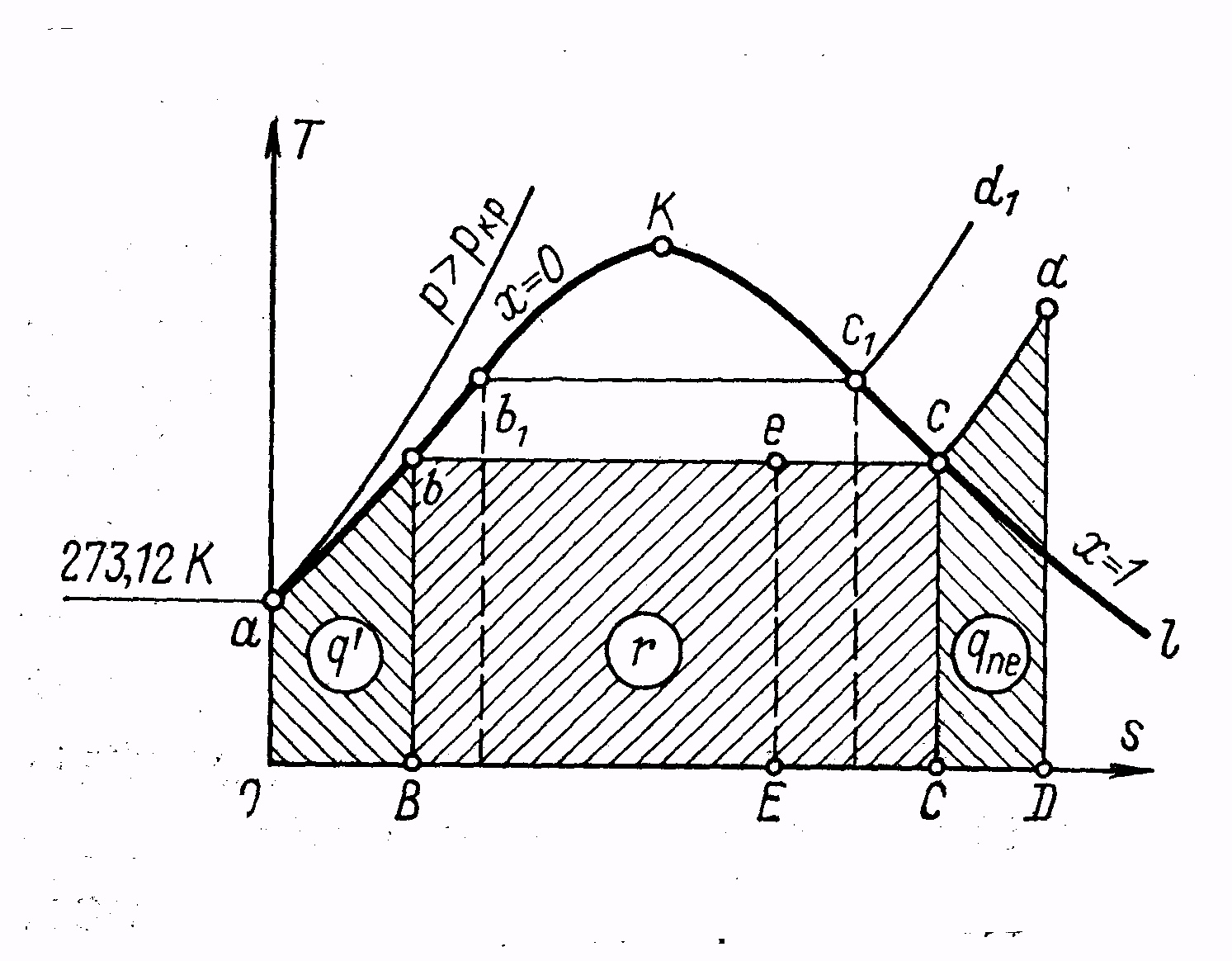 я
діаграма широко застосовується при
дослідженнях розімкнутих і колових
процесів водя- ної пари (рисунок 2.7).
я
діаграма широко застосовується при
дослідженнях розімкнутих і колових
процесів водя- ної пари (рисунок 2.7).
При
будь – якому тиску і при температурі 0
оС
ентропія води sо
дорівнює нулю. Тому ізотерма води при
t
= 0 оС,
що зображалася в Р
v
– координатах лінією І,
в Тs
–
координатах перетворюється в точку і
позначається буквою
а.
Ця точка лежить на осі ординат і служить
початком побудови нижньої прикордонної
кривої. Перш за все будують прикордонні
лінії. Абсцисами точок нижньої прикордонної
кривої авК
є
значення ентропії киплячої рідини s![]() ,
а верхньої прикордонної кривої
Ксl
– значення ентропії сухої насиченої
пари
,
а верхньої прикордонної кривої
Ксl
– значення ентропії сухої насиченої
пари
![]() .
При досягнен-
.
При досягнен-
Рисунок 2.7 - Тs– діаграма водяної ні критичної температури лінії авК і Ксl перетинаються в
пари точці К, що визначає критичний стан. Потім будують ізобари
авсd, ав1с1d1 тощо. На ділянці а – в відбувається нагрівання рідини від 0 до температури ки- піння tн , на ділянці в – с - пароутворення, а на ділянці с – d – перегрів пари.
У
процесі ав
підігрівання рідини до кипіння ентропія
її змінюється від sо
= 0 до
![]() і визна-чається за формулою
і визна-чається за формулою
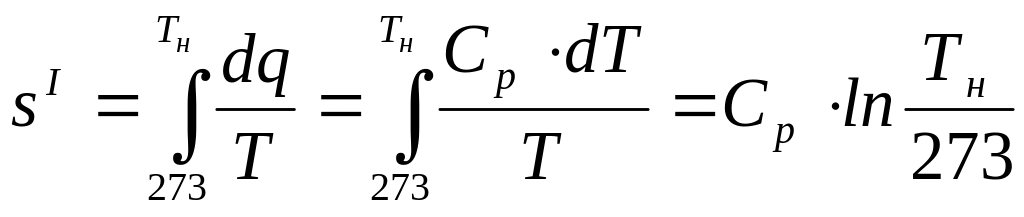 .
(2.42)
.
(2.42)
Ізобара ав є логарифмічною лінією, кривизна якої незначно відрізняється від кривизни ниж- ньої прикордонної кривої авК. Тому прийнято вважати, що при тисках аж до критичного ізобари рідини співпадають з нижньою прикордонною кривою. Таким чином, нижня прикордонна крива є всією областю рідини від 0 оС до температури кипіння при різних тисках, аж до критичного.
Ізобари води надкритичного тиску проходять лівіше нижньої прикордонної кривої і перети-нають її тільки в одній точці а.
Ізобара пароутворення вс зображується горизонтальною лінією, бо це не тільки ізобара, але й ізотерма при tн = const.
Ізобари перегріву пари сd , с1d1 тощо зображуються лініями, близькими до логарифмічних. Між прикордонними кривими авК і Ксl розташована область вологої насиченої пари, а праворуч і вище верхньої прикордонної знаходиться область перегрітої пари. В області вологої пари звичай-но наносяться лінії постійної сухості, які зображуються кривими лініями, що виходять з критич- ної точки (на рисунку 2.7 не показані).
Площі
під кривою процесу в Тs
– діаграмі зображують теплоту процесу.
На рисунку 2.7 площа ОавВ
під
ізобарою
ав
зображує теплоту рідини q;
площа
ВвсС
в
процесі
вс
– теплоту пароутворення r
;
площа СсdD
процесу сd
- теплоту перегріву q![]() .
.
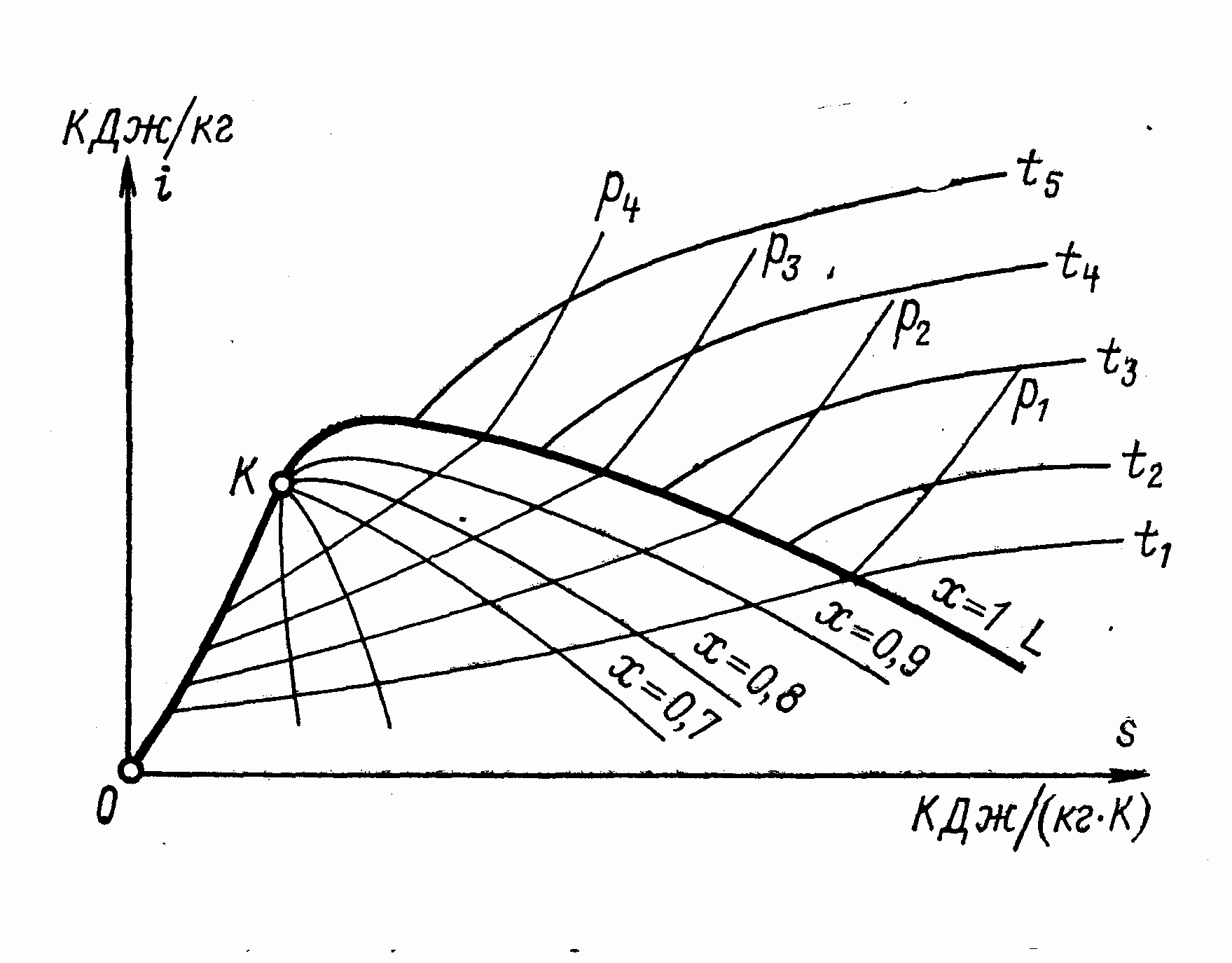
Питання 2 іs– діаграма водяної пари
 Лінії
діаграми побудовані шляхом використання
значень ентальпій та ентропій, що взяті
з таблиць термодинамічних властивостей
води і водяної пари (рисунок 2.8).
Лінії
діаграми побудовані шляхом використання
значень ентальпій та ентропій, що взяті
з таблиць термодинамічних властивостей
води і водяної пари (рисунок 2.8).
На
іs
- діаграмі криві лінії ОК
і КL
– прикор- донні криві киплячої рідини
і сухої насиченої пари. Крива ОК
виходить
з початку координат, бо при 0![]() і0
=
0
і s0
= 0. Ізобари в області вологої насиченої
пари збігаються з ізотермами. В області
перегрітої пари ізотерми є кривими
лініями, повернутими ви- пуклістю угору,
а ізобари – кривими, що увігнуті. Ізохори
зображуються кривими лініями або
пунктир- ними, або кольоровими (вони
можуть бути відсутні).
і0
=
0
і s0
= 0. Ізобари в області вологої насиченої
пари збігаються з ізотермами. В області
перегрітої пари ізотерми є кривими
лініями, повернутими ви- пуклістю угору,
а ізобари – кривими, що увігнуті. Ізохори
зображуються кривими лініями або
пунктир- ними, або кольоровими (вони
можуть бути відсутні).
Рисунок 2.8 - іs– діаграма водяної пари
Питання 3 Зображення термодинамічних процесів водяної пари в Рv-, Тs- та іs– діаграмах
Кожен з чотирьох термодинамічних процесів (ізохорний, ізобарний, ізотермічний та адіа-батний) можуть протікати цілком в області вологої або перегрітої пари, тобто без зміни агрегатно-го стану. Але більш цікавим є випадок зміни агрегатного стану.
Через те що водяна пара не підпорядковується законам ідеальних газів, співвідношення між параметрами і рівняння для підрахунку теплоти, зміни внутрішньої енергії і роботи для пари не- прийнятні.
При вирішенні задач із використанням таблиць необхідно спочатку встановити стан робо-чого тіла на початку і в кінці процесу. Для цього при відомому тиску порівнюють будь – який ві- домий параметр (v,i,s,t) з відповідним параметром сухої насиченої пари. Нехай відомо початкове значення ентропії s, тоді, якщо:
а) s/<s<s//, пара буде волога. Спочатку необхідно визначити степінь сухості х, а інші параметри
підрахувати за відомими формулами;
б) s=s//, пара буде суха насичена і всі необхідні її параметри знаходять за допомогою таблиць сухої
насиченої пари;
в) s>s//, пара буде перегріта. Її параметри визначають за допомогою таблиць перегрітої пари;
г) s<s/, це вода, яка не догріта до кипіння, і всі параметри знаходять за допомогою таблиць води і
перегрітої пари.
При вирішенні задач по і s – діаграмі стан робочого тіла визначають як точку перетину будь – яких двох ліній і всі параметри (за винятком и) знаходять з діаграми.
Ізохорний процес (v= const) (рисунок 2.9)
В Тs- діаграмі ізохора має вигляд кривої лінії з випуклістю вгору в області вологої насиче-ної пари і випуклістю униз в області перегрітої пари. В іs– діаграмі ізохора зображується кривою
1 – 2, причому початковий стан, що визначається точкою 1, знаходиться на перетині заданої ізохо- ри v з ізобарою Р1. Кінцевий стан визначається точкою 2, яка знаходиться на перетині тієї ж ізохо-
ри v з ізотермою t2.
Через те що в процесі робота не здійснюється, вся теплота витрачається на зміну внутріш-
ньої енергії, тому
![]() 2-Р2
2-Р2
![]() )-(і1-Р1
)-(і1-Р1![]() ).
(2.43)
).
(2.43)

Рисунок 2.9 - Ізохорний процес для водяної пари
Ізобарний процес (Р=соnst ) (рисунок 2.10)
В Тs- діаграмі в області вологої насиченої пари ізобара співпадає з ізотермою і тому пред- ставлена горизонтальною лінією, в області перегрітої пари – кривою, близькою до логарифмічної. В іs– діаграмі ізобара зображена лінією 1 – 2, причому початковий стан визначається точкою 1 і
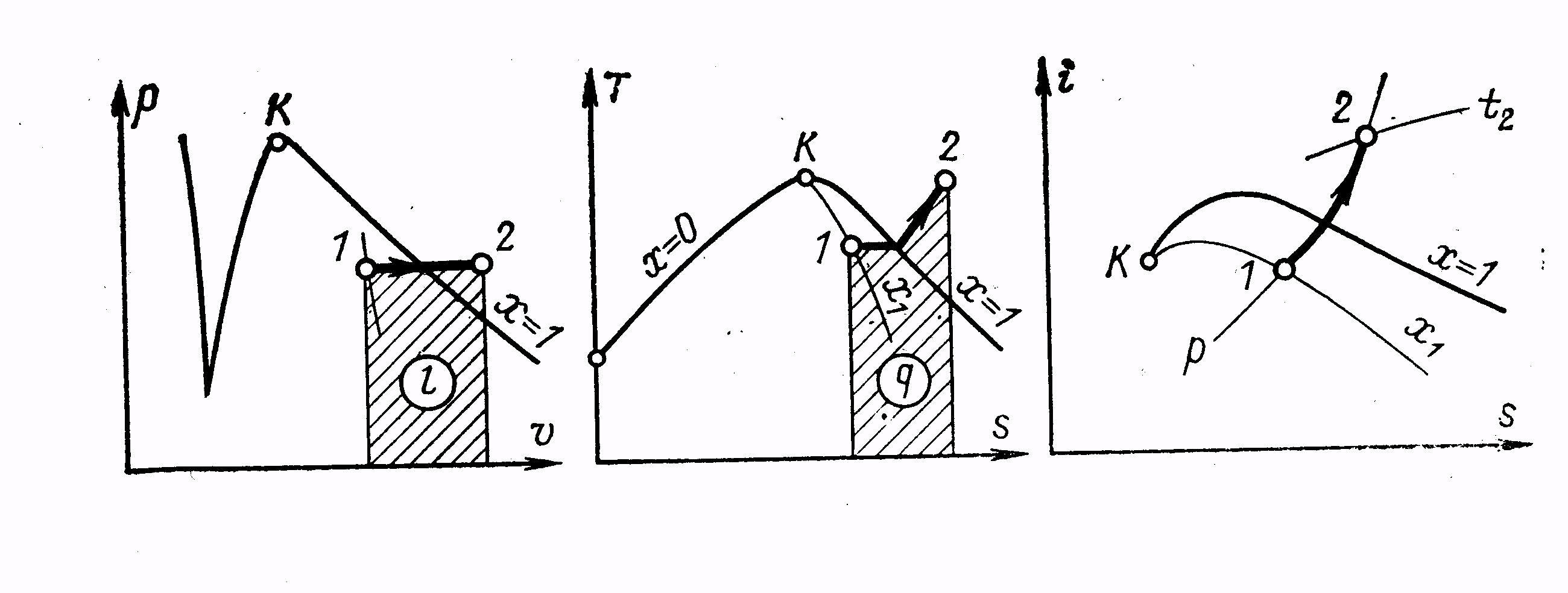
Рисунок 2.10 - Ізобарний процес для водяної пари
знаходиться на перетині заданої ізобари 1 - 2 і лінії постійної сухості х1, а кінцевий стан – точкою 2, яка знаходиться на перетині ізобари й ізотерми t2.
Теплота процесу визначається рівнянням q = і2 - і1, (2.44)
зміна внутрішньої енергії по формулі (1.93), а робота розширення
![]() .
(2.45)
.
(2.45)
В цьому процесі переважна частина теплоти, що підводиться, витрачається на зміну внут- рішньої енергії.
Ізотермічний процес (t =const) (рисунок 2.11)
В ізотермічному процесі в початковому стані пара волога, а в кінцевому – перегріта. В Рv- діаграмі в області вологої пари ізотерма зображується горизонтальною лінією, а області перегрітої пари – гіперболічною кривою, більш пологою, ніж для газу. В іs- діаграмі ізотерма представлена лінією 1 - 2. Початковий стан пари (точка 1) знаходиться на перетині ізобари Р1 і лінії постійної сухості х1, а кінцевий стан (точка 2) на перетині заданої ізотерми t та ізобари Р2.

Рисунок 2.11 - Ізотермічний процес для водяної пари
У процесі ізотермічного розширення пари частина теплоти, що підводиться, витрачається на зміну його внутрішньої потенційної енергії і в цьому полягає його відмінність від того ж проце- су в ідеальних газах.
Теплота процесу визначається по рівнянню
![]() ,
(2.46)
,
(2.46)
зміна внутрішньої енергії – по формулі (1.93), а робота розширення – із І закону ТД
![]() .
.
Адіабатний процес (dq=0) (рисунок 2.12)
В адіабатному процесі ентропія не змінюється (s = const), тому в Тs– та іs– діаграмах адіа-бата – вертикальна лінія. В Рv– діаграмі адіабата зображається лінією, схожою на гіперболічну криву, яка може бути наближено виражена рівнянням типу Рvк =const.
У невеликих межах зміни тиску коефіцієнт к приймають рівним:
- для перегрітої пари к =1,3;
- для сухої насиченої пари к = 1,135;
- для вологої пари к = 1,035+0,1х, де х – початкова степінь сухості пари.
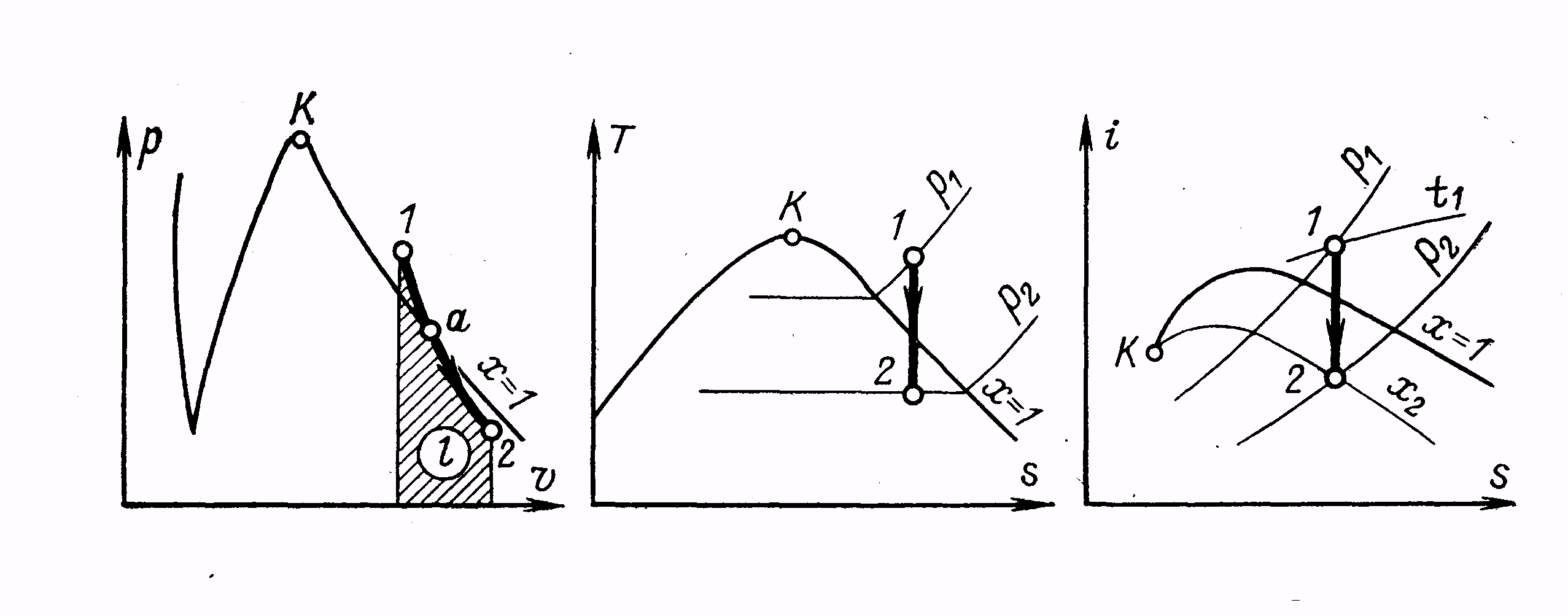
Рисунок 2.12 - Адіабатний процес водяної пари
Отже, в області перегрітої пари адіабата йде крутіше ніж в області вологої пари, і в точці а перетину її з верхньою прикордонною кривою є перегин.
В іs – діаграмі адіабата зображається лінією 1 - 2, причому початковий стан пари (точка 1) знаходиться на перетині ізобари Р1 та ізотерми t1. Опускаючи з точки 1 вертикальну лінію s = const до перетину з ізобарою Р2, знаходять точку 2 (кінцевий стан пари в кінці розширення). В точках 1 і 2 знаходять відсутні параметри пари, необхідні для вирішення задач.
В адіабатному процесі робота здійснюється за рахунок внутрішньої енергії і визначається рівнянням
![]() .
(2.47)
.
(2.47)
Для виконання самостійної роботи № 10 необхідно, крім конспекту теоретичної частини, розв’язати наступні задачі.
Задача 22
За допомогою таблиць термодинамічних властивостей води і водяної пари визначте пара-метри (питомий об’єм, щільність, ентальпію, ентропію) для:
а) киплячої рідини; б) сухої насиченої пари; в) вологої насиченої пари,
якщо відомі температура насичення tн і степінь сухості х. Вихідні дані наведені в таблиці 2.7.
Таблиця 2.7 - Вихідні дані до задачі 22
Вар. |
tн, о С |
х |
Вар. |
tн, о С |
х |
Вар. |
tн, о С |
х |
Вар. |
tн, о С |
х |
1 |
25 |
0,9 |
9 |
15 |
0,76 |
17 |
75 |
0,77 |
25 |
85 |
0,97 |
2 |
50 |
0,95 |
10 |
0 |
0,91 |
18 |
100 |
0,88 |
26 |
125 |
0,79 |
3 |
65 |
0,8 |
11 |
60 |
0,73 |
19 |
10 |
0,96 |
27 |
140 |
0,83 |
4 |
30 |
0,85 |
12 |
35 |
0,86 |
20 |
95 |
0,87 |
28 |
130 |
0,98 |
5 |
55 |
0,7 |
13 |
90 |
0,94 |
21 |
115 |
0,78 |
29 |
135 |
0,89 |
6 |
80 |
0,75 |
14 |
105 |
0,71 |
22 |
45 |
0,74 |
30 |
145 |
0,99 |
7 |
20 |
0,92 |
15 |
40 |
0,82 |
23 |
110 |
0,81 |
|
|
|
8 |
70 |
0,84 |
16 |
5 |
0,93 |
24 |
120 |
0,72 |
|
|
|
Задача 23
Суха насичена пара з тиском Р при охолодженні перетворюється в вологу насичену зі степеню сухості х. Визначте за допомогою і,s - діаграми параметри вологої і сухої насиченої пари, а також кількість відведеної теплоти. Чому дорівнює масова ізобарна теплоємність даного процесу? Вихідні дані для задачі наведені в таблиці 2.8.
Таблиця 2.8 - Вихідні дані для задачі 23
Вар. |
Р, МПа |
х |
Вар. |
Р, МПа |
х |
Вар. |
Р, МПа |
х |
Вар. |
Р, МПа |
х |
1 |
0.14 |
0.9 |
10 |
0.04 |
0.85 |
19 |
0.1 |
0.83 |
28 |
1.5 |
0.8 |
4 |
0.01 |
0.87 |
13 |
0.02 |
0.89 |
22 |
0.18 |
0.88 |
|
|
|
7 |
0.3 |
0.84 |
16 |
0.07 |
0.86 |
25 |
0.5 |
0.91 |
|
|
|
Задача 24
1 кг водяної пари при тиску Р і температурі t1 нагрівається в ізобарному процесі до t2. Ви- значте за допомогою іs - діаграми кількість теплоти, роботу процесу і зміну внутрішньої енергії
пари. При розв’язку задачі використовуйте дані таблиць термодинамічних властивостей води і водяної пари. Вихідні дані для задачі наведені в таблиці 2.9.
Таблиця 2.9 - Вихідні дані для задачі 24
Вар. |
Р, бар |
t1, о С |
t2, о С |
Вар. |
Р, бар |
t1, о С |
t2, о С |
Вар. |
Р, бар |
t1, о С |
t2, о С |
2 |
10 |
220 |
370 |
14 |
5 |
190 |
330 |
26 |
45 |
270 |
390 |
5 |
1 |
150 |
310 |
17 |
7.5 |
180 |
300 |
29 |
35 |
280 |
380 |
8 |
3 |
160 |
280 |
20 |
4 |
200 |
320 |
|
|
|
|
11 |
2 |
130 |
260 |
23 |
20 |
230 |
340 |
|
|
|
|
Задача 25
Перегріта пара з початковим тиском Р1 і температурою t1 cтискається по ізотермі і в кінці процесу стає вологою зі степеню вологості (1-х). Визначте за допомогою іs - діаграми кількість теплоти, що відводиться, зміну внутрішньої енергії і роботу, що витрачається на стиснення. При розв’язку задачі використовуйте дані таблиць термодинамічних властивостей води і водяної пари. Вихідні дані для задачі наведені в таблиці 2.10.
Таблиця 2.10 - Вихідні дані для задачі 25
Вар. |
Р1, бар |
t1, о С |
1-х |
Вар. |
Р1, бар |
t1, о С |
1-х |
Вар. |
Р1, бар |
t1, о С |
1-х |
3 |
1 |
250 |
0,12 |
15 |
0,2 |
170 |
0,08 |
27 |
0,13 |
140 |
0,11 |
6 |
10 |
200 |
0,15 |
18 |
0,7 |
130 |
0,2 |
30 |
0,05 |
100 |
0,22 |
9 |
0,5 |
150 |
0,1 |
21 |
0,4 |
200 |
0,13 |
|
|
|
|
12 |
20 |
220 |
0,05 |
24 |
0,9 |
230 |
0,17 |
|
|
|
|
