
- •Лекция 1 «Хладагенты неорганического происхождения»
- •1 История развития
- •2 Требования, предъявляемые к хладагентам
- •3 Обозначение и классификация хладагентов
- •3.1 Хладагенты неорганического происхождения
- •3.1.1 Обозначение хладагентов
- •3.1.2 Теплофизические и химические свойства
- •4 Атомно-молекулярная теория
- •5 Газовые законы
- •5.1 Объединенное уравнение газовах законов. Газовая постоянная
- •5.2 Закон Дальтона. Парциальное давление
- •5.3 Закон Бойля-Мариотта. Сжижение газов. Критические давление, температура, объем
- •5.4 Уравнение Клапейрона-Менделеева
- •5.5 Уравнение Ван-дер-Ваальса
- •Лекция 2
- •1 Обозначение хладагентов
- •2 Основные химические свойства
- •3 Классификация хладагентов
- •Лекция 3 «Цепные реакции. Молекулярно-кинетическая теория. Физические принципы понижения температуры»
- •1 Цепные реакции
- •1.2 Линейная цепная реакция
- •1.3 Разветвленная цепная реакция.
- •1.4 Взрываемость и самовоспламенение
- •2 Молекулярно–кинетическая теория
- •3. Физические принципы понижения температуры
- •1) Дросселирование (эффект Джоуля-Томсона).
- •2) Расширение в вихревой трубе (эффект Ранка-Хильша).
- •3) Термоэлектрический эффект (эффект Пельтье).
- •4) Расширение с совершением полезной работы.
- •5) Электрокалорический эффект охлаждения (эк).
- •7) Намагничивание сверхпроводников.
- •8) Механокалорический эффект.
- •1 Парокомпрессионные холодильные машины
- •2 Теплоиспользующие холодильные машины
- •Лекция 4 «абсорбционные холодильные машины»
- •1 Абсорбция
- •3 Растворы
- •3.1 Общие свойства растворов
- •3.1.1 Классификация систем, состоящих из двух и более веществ
- •3.1.2 Способы выражения состава растворов
- •9 Коррозия металлов
- •9.1 Виды и типы коррозии
- •9.2 Способы защиты металлов от коррозии
- •9.2.1 Изолирование металлов от внешней среды
- •9.2.2 Изменение состава коррозионной среды
- •9.2.3 Рациональное конструирование
- •9.2.4 Электрохимические способы защиты от коррозии
- •Ингибиторы коррозиии
- •Глава 1. Ингибиторы коррозии на основе комплексов переходных металлов и азотсодержащих алифатических и ароматических соединений (обзор литературы)
- •Глава 1. Ингибиторы коррозии на основе комплексов переходных металлов и азотсодержащих алифатических и ароматических соединений (обзор литературы)
- •1.1. Ингибиторы коррозии для водных сред, содержащих кислород
- •1.2. Ингибиторы на основе азотсодержащих алифатических и ароматических соединений
- •1.3. Ингибиторы сероводородной коррозии
- •1.4. Ингибиторы углекислотной коррозии
- •1.5. Ингибиторы коррозии в нейтральных средах
- •Список использованной литературы
5.4 Уравнение Клапейрона-Менделеева
Для описания состояния идеального газа на практике также широко применяется уравнение Клапейрона-Менделеева
РV = nRТ. (2)
5.5 Уравнение Ван-дер-Ваальса
Одним из наиболее ранних и изученных уравнений состояния реальных газов является уравнение Ван-дер-Ваальса
 (3)
(3)
где,
 - поправка, учитывающая взаимное
притяжение молекул, которое действует
как некое давление,
- поправка, учитывающая взаимное
притяжение молекул, которое действует
как некое давление,
 -
поправка, учитывающая объем молекул и
взаимное отталкивание между ними при
малых растояниях.
-
поправка, учитывающая объем молекул и
взаимное отталкивание между ними при
малых растояниях.
На практике могут применяться другие подходы для описания свойств реальных газов. Это применение коэффициента сжимаемости, уравнения Тафта и др.
Лекция 2
«Хладагенты органического происхождения»
1 Обозначение хладагентов
В качестве хладагентов могут быть использованы первые представители предельных, непредельных и циклических углеводородов, их кислород-, галоген- и азотсодержащие производные, а также другие классы органических соединений, обладающие необходимыми теплофизическими свойствами.
В соответствии с ИСО 817-74 принята следующая номенклатура:
За основу классификации взяты первые четыре представителя предельных углеводородов, которые обозначили условными цифрами:
CH4 – 1, C2H6 – 11, C3H8 – 21, C4H10 – 31.
Вначале записывается буква R, далее к условной цифре прибавляется число атомов водорода в молекуле хладагента и затем пишется цифра «0», указывающая на отсутствие фтора. Приведем названия соответствующих хладагентов:
CH4 , метан, R(1+4)+0→ R50;
C2H6 , этан, R(11+6)+0→R170;
С3H8 , пропан, R(21 + 8) + 0→R290 .
Для двух изомеров бутана применяются следующие названия:
С4H10 , бутан → R600 и изобутан → R600а.
При наличии фтора, вместо цифры «0» пишется число атомов фтора в молекуле. Например,
CHF3, трифтор метан → R23.
Количество атомов хлора не указывается, так как их число определяется по числу оставшихся свободных химических связей. Углерод в органических соединения 4-х валентен. Например,
CHFCl2 , фтордихлорметан → R21.
Для хладагентов, содержащих бром, добавляют в названии букву «В» и цифру указывающую на количество брома. Например: CF3Br , трифторбромметан → R13B1. Допускается второй вариант названия. Например, для R13B1 второе название будет Н1301. То есть вместо буквы R пишется буква Н, за которой следуют цифры: первая указывает на метановый ряд, вторая ─ число атомов фтора, третья ─ число атомов хлора, четвертая ─ число атомов брома.
Циклические соединения обозначаются – RC. Например:
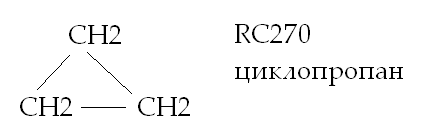 .
.
В случае непредельных соединений вначале цифрового обозначения добавляется цифра 1 до тысяч. Например:
CH2=CH2, этилен → R1150;
CH2=CH–CH3, пропилен → R1270; CH2=CH–CH2–CH3, бутен(бутилен) → R1390; ClCH=CHCl, 1,2-дихлорэтилен → R1130.
Для изомеров с ассимметричным строением добавляются буквы:
«а», «б», «в» и т.д. Например:
CH2F–CH2F, 1,2-дифторэтан → R152;
CHF2–CH3, 1,1-дифторэтан → R152а.
Несмотря на то, что изомеры имеют одинаковый состав, но в холодильной технике могут быть не взаимозаменяемы, так как часто существенно различаются по теплофизическим свойствам. Например: R152 - неполярное соединение с температурой кипения … 0С, а R152а, вследствие несимметричности молекулы, - полярное соединение со значительно более высокой температурой кипения равной …0С.
Для кислород- и азотсодержащих соединений применяются следующие названия:
CH3NH2, метиламин → R630;
C2H5NH2, этиламин → R631;
C2H5ОC2H5, диэтиловый эфир → Е610;
CH3ОCH3, диметиловый эфир → E170;
HCООCH3, метилформиат → Е611;
СНF2ОСF3, пентафторэтановый эфир → Е125 и др навания.
Для смесевых хладагентов применяются следующие названия:
1) Зеотропным или раздельно кипящим присвоена серия R400. Например:
R401А (R22-53%, R152 – 13%, R124 – 34%);
R401В (R22-61%, R152 – 11%, R124 – 28%) и т.д.
2) Азеотропным или нераздельно кипящим смесям присвоена серия R500. Например:
R500 (R12-73,8%, R152а-26,2%);
R501 (R22-75%, R12-25%) и т.д.
Каждая фирма-производитель хладагентов выпускает в продажу свою продукцию под собственным наименованием, например:
R407C может поступать на рынок под марками FORANE®407C, SUVA®9000, MackFri-07C и т.д.
