
- •Тиреоидные гормоны
- •Методы исследования.
- •Диффузный токсический зоб
- •Медикаментозная терапия.
- •2. Хирургическое лечение
- •3. Терапия радиоактивным йодом
- •4. Лечение эндокринной офтальмоптии
- •Синдром гипотиреоза
- •Тироксин, трийодтиронин
- •Повышена
- •Подавлена
- •Подавлена
- •Повышена
- •Подавлена
- •Подавлена
- •Ситуационные задачи
- •Задача № 3.
ГОУ ВПО «ВОРОНЕЖСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ
АКАДЕМИЯ ИМ. Н.Н. БУРДЕНКО ФЕДЕРАЛЬНОГО АГЕНСТВА ПО ЗДРАВООХРАНЕНИЮ И СОЦИАЛЬНОМУ РАЗВИТИЮ»
КАФЕДРА ГОСПИТАЛЬНОЙ ТЕРАПИИ
УТВЕРЖДАЮ
Заведующий кафедрой
_________________/Э.В. Минаков
«______»__________________200 г
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ ПРЕПОДАВАТЕЛЮ ПО ТЕМЕ ПРАКТИЧЕСКОГО ЗАНЯТИЯ: Изменения внутренних органов и систем при заболеваниях щитовидной железы, проявляется тиреотоксикозом и гипотиреозом. Дифференциальная диагностика и лечение данных заболеваний.
Факультет: лечебный
Курс: 6
Цикл: Патология внутренних органов при эндокринных заболеваниях.
Автор: Петрова Т.Н.
ТЕМА: Изменения внутренних органов и систем при заболеваниях щитовидной железы, проявляется тиреотоксикозом и гипотиреозом. Дифференциальная диагностика и лечение данных заболеваний.
ЦЕЛЬ ЗАНЯТИЯ: студент должен научиться лабораторно верифицировать повышенную и сниженную функцию щитовидной железы. Изучить заболевания, приводящие к тиреотоксикозу и гипотиреозу, изменения внутренних органов и систем, сопровождающие их, освоить их диагностические и дифференциально диагностические критерии, оценить их значение своевременной диагностики. Научиться правильно лечить ДТЗ, АИТ, и подострый тиреоидит.
МОТИВАЦИЯ ТЕМЫ ЗАНЯТИЯ: совершенствование практических и теоретических знаний по данной теме с целью дифференциальной диагностики данной патологии в клинике внутренних болезней.
КОНТРОЛЬНЫЕ ВОПРОСЫ ЗАНЯТИЯ:
Назовите основные заболевания ЩЖ сопровождающиеся синдромами гопо- и гипертиреоза.
Назовите алгоритм лабораторной диагностики повышенной и сниженной функции щитовидной железы.
Вопросы этиологии, патогенеза диффузного токсического зоба, хронического аутоиммунного и подострого тиреоидитов – заболеваний, приводящих к тиреотоксикозу и гипотереозу.
Клиническая картина перечисленных заболеваний щитовидной желез, патология внутренних органов и систем при этих заболеваниях.
Классификация тиреотоксикоза и гипотиреоза.
Критерии построения диагноза и дифференциальной диагностики диффузного токсического зоба, тиреоидитов.
Что такое субклинический и олигосимптоматический гипотиреоз и каково значение его современной диагностики.
ИСХОДНЫЙ УРОВЕНЬ ЗНАНИЙ: студент должен знать этиологию, патогенез ДТЗ, АИТ, и подострого тиреоидита, заболеваний, приводящих к повышению и снижению функции щитовидной железы. Знать клиническую картину перечисленных заболеваний, классификацию тиреотоксикоза и гипотериоза. Уметь квалифицировано собрать жалобы, охарактеризовать их, поставить диагноз заболевания, уметь пальпировать щитовидную железу, определить глазные симптомы. Оценить выраженность патологии внутренних органов и систем. Лабораторные, рентгенологические, ЭКГ, УЗИ, методы диагностики. Знать основные группы лекарственных препаратов, используемых в
лечении ДТЗ, АИТ, подострого тиреоидита.
ТЕОРЕТИЧЕСКИЙ МАТЕРИАЛ ЗАНЯТИЯ
Щитовидная железа (glandula thyroidea) — железа внутренней секреции, синтезирующая ряд гормонов, необходимых для поддержания гомеостаза.
Щитовидная железа состоит из двух долей и перешейка. Доли прилегают слева и справа к трахее, перешеек расположен на передней поверхности трахеи. Иногда от перешейка или чаще левой (реже правой) доли железы отходит дополнительная пирамидальная доля. В норме масса щитовидной железы составляет от 20 до 60 г. В период полового созревания масса Щ. ж. увеличивается, а в старческом возрасте уменьшается. У женщин Щ. ж. больше, чем у мужчин; во время беременности происходит ее физиологическое увеличение, которое исчезает самостоятельно в течение 6—12 мес. после родов.
Щитовидная железа имеет наружную и внутреннюю соединительнотканные капсулы. За счет наружной капсулы образуется связочный аппарат, фиксирующий железу к трахее и гортани. Верхней границей железы (боковых долей) является щитовидный хрящ, нижней — 5—6 кольца трахеи. Перешеек расположен на уровне I—III или II—IV хрящей трахеи.
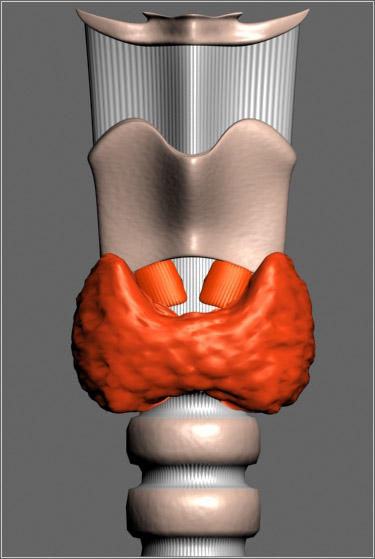
Щитовидная железа, является одним из наиболее кровоснабжаемых органов с развитой артериальной, и более мощной венозной системами. Кровь в железу поступает по двум верхним тиреоидным артериям (ветви наружной сонной артерии) и двум нижним тиреоидным артериям, которые образуют между собой анастомозы. Венозная и лимфатическая системы осуществляют отток от Щ. ж. крови и лимфы, содержащих тиреоидные гормоны, тиреоглобулин, а при патологичесих состояниях антитиреоидные антитела, тиреостимулирующие и тиреоблокирующие иммуноглобулины.
Иннервация Щ. ж. осуществляется веточками как блуждающего нерва (парасимпатическая), так и ветвями шейных ганглиев (симпатическая).
Основной структурной и функциональной единицей Щ. ж. являются фолликулы — пузырьки различной формы, чаще округлой, диаметром 25—500 мкм, отделенные друг от друга тонкими прослойками рыхлой соединительной ткани с большим количеством кровеносных и лимфатических капилляров. Просвет их заполнен коллоидом — бесструктурной массой, содержащей тиреоглобулин, который синтезируется фолликулярными, или так называемыми А-клетками, формирующими стенку фолликула. Это эпителиальные клетки кубической или цилиндрической (при повышении функциональной активности) формы. При снижении тиреоидной функции они уплощаются. Наряду с фолликулами в Щ. ж. имеются межфолликулярные островки эпителиальных клеток (В-клетки, клетки Асканази), являющихся источником образования новых фолликулов. Клетки Асканази крупнее А-клеток, имеют зозинофильную цитоплазму и округлое центрально расположенное ядро: в цитоплазме выявлены биогенные амины, в т.ч. серотонин. Помимо А- и В-клеток в Щ. ж. имеются и парафолликулярные клетки (С-клетки). Они расположены на наружной поверхности фолликулов, являются нейроэндокринными клетками, не поглощают йод и относятся к АПУД-системе.
Щитовидная железа секретирует два йодосодержащих гормона — тироксин (Т4) и трийодтиронин (Т3) и один пептидный гормон— кальцитонин. Тироксин и трийодтиронин синтезируются в апикальной части тиреоидного эпителия и частично в интрафолликулярном пространстве, где накапливаются, включаясь в состав тиреоглобулина. Кальцитонин (тиреокальцитонин) вырабатывается С-клетками щитовидной железы, а также паращитовидными железами и вилочковой железой.
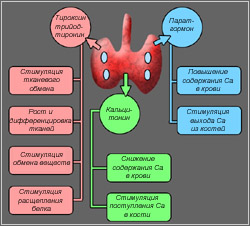
Фолликулярные клетки Щ. ж. обладают уникальной способностью захватывать из кровотока йод, который при участии фермента пероксидазы связывается с тиреоглобулином коллоида. Тиреоглобулин играет роль внутрифолликулярного резерва тиреоидных гормонов. При необходимости путем пиноцитоза определенное количество его поступает внутрь фолликулярной клетки, где в результате протеолиза происходит выделение Т3 и Т4 из тиреоглобулина и отделение их от других гормонально-неактивных йодированных пептидов. Свободные гормоны поступают в кровь, а йодпротеины подвергаются дейодизации; освободившийся йод идет на синтез новых тиреоидных гормонов. Скорость расщепления тиреоглобулина, синтеза тиреоидных гормонов зависит как от центральной регуляции, так и от уровня йода и крови и наличия в ней веществ, влияющих ни йодный обмен (иммуностимулирующих глобулинов, тиоцианатов, бромидов и т.д.). Таким образом, их синтез и секреция осуществляются с такой скоростью и в таком количестве, которые необходимы организму для поддержания в тканях концентрации гормонов, обеспечивающих гомеостаз. Последнее достигается сложной системой центральной и периферической регуляции.
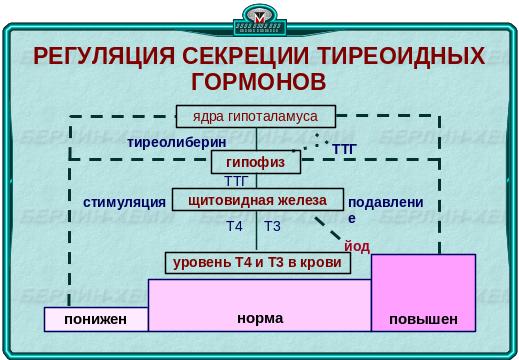
Центральная регуляция осуществляется выработкой тиреолиберина (рилизинг-фактора тиреотропного гормона) и, возможно, тиреостатина (фактора, ингибирующего синтез тиреотропного гормона). Тиреотропный гормон (ТТГ) синтезируется тиреотрофами передней доли гипофиза, он стимулирует рост и функциональную активность тиреоидного эпителия. Поступление ТТГ в кровь регулируется уровнем концентрации тиреоидных гормонов в крови и тиреолиберином, однако основным регулирующим фактором является концентрация тиреоидных гормонов в крови; чрезвычайно высокий уровень последних делает тиреотрофы резистентными к тиреолиберину. Периферическая регуляция тиреоидного обмена зависит от числа специфических рецепторов к тиреоидным гормонам в клетке; в условиях высокого содержания тиреоидных гормонов их число сокращается, при низком содержании — увеличивается. Кроме того, большая часть тироксина может метаболизироваться в неактивную форму и таким образом осуществлять один из видов периферической регуляции функционального состояния организма.
Физиологическое содержание тиреоидных гормонов необходимо для нормального синтеза белков в различных органах и тканях (от ц.н.с. до костной ткани); избыток их ведет к разобщению дыхания тканевого и окислительного фосфорилирования в митохондриях клеток с последующим резким снижением энергетического запаса организма. Кроме того, повышая чувствительность рецепторов к катехоламинам, тиреоидные гормоны вызывают усиление возбудимости вегетативной нервной системы, проявляющееся тахикардией, аритмией, повышением систолического АД, усилением моторики желудочно-кишечного тракта и секреции пищеварительных соков: они также усиливают распад гликогена, тормозят его синтез в печени, влияют на липидный обмен. Недостаток тиреоидных гормонов обусловливает резкое снижение скорости всех окислительных процессов в организме и накопление гликозаминогликанов. Наиболее чувствительны к этим изменениям клетки ц.н.с. миокарда, эндокринных желез.
Тиреоидные гормоны
Тиреоидные гормоны [анат. (glandula) thyreoidea щитовидная железа] — тироксин и трийодтиронин, гормоны, синтезируемые щитовидной железой.
Тироксин — 3,5,3',5' тетрайодтиронин (Т4), йодированная аминокарбоновая кислота, производное аминокислоты тирозина, основной гормон щитовидной железы, является главной циркулирующей формой тиреоидных гормонов. На долю тироксина приходится 3/4 всего йода, содержащегося в крови.
Тироксин обладает многообразным физиологическим действием: он необходим для нормального роста, развития и дифференциации тканей, стимулирует сердечную деятельность, азотистый, углеводный и жировой обмен, проведение нервных импульсов, усиливает поглощение кислорода тканями и их теплопродукцию, повышает активность отдельных ферментных систем как в целом организме, так и в культуре тканей. L-тироксин обладает физиологической активностью, в 3 раза превышающей активность D-тироксина. Обычно ответ на тироксин наступает по истечении определенного латентного периода и проявляется усилением метаболизма в печени, сердце, мышцах и почках. В ряде других органов (головном мозге взрослого человека, селезенке, семенных пузырьках) изменений метаболизма, вызванных тироксином, не обнаружено.
Биосинтез тироксина осуществляется, как полагают, путем окислительной конденсации двух молекул дийодтирозина, находящихся в связанном состоянии в тиреоглобулине; образовавшиеся в результате реакции тироксин и дегидроаланин или серин остаются в составе молекулы тиреоглобулина. Секреции тироксина в кровь предшествует постепенный гидролиз молекул тиреоглобулина протеазами лизосом фолликулярных клеток щитовидной железы при миграции в направлении базальной мембраны фолликулярной клетки.
Тиреоидные гормоны циркулируют в крови в основном в виде комплексов с белками сыворотки крови. Среди сывороточных белков, избирательно связывающих тироксин, выделяют тироксинсвязывающие глобулин, альбумин и преальбумин. Свободный тироксин находится в крови в состоянии подвижного равновесия со связанным с белками тироксином и может проникать в клетки. Концентрация циркулирующего тироксина определяется интенсивностью его секреции щитовидной железой и потреблением гормона на периферии и контролируется выбросом в кровоток тиреотропного гормона. Тироксин в комплексе с глобулином обладает большей стабильностью, чем связанный с альбумином и преальбумином. Свободный тироксин, содержащийся в крови в незначительных количествах, тем не менее определяет тиреоидное состояние организма (гипо-, гипер- или эутиреоз), обусловливает периферический эффект гормона, скорость его метаболизма (в норме период биологической полужизни тироксина равен 6—7 дням) и влияние на гипофиз.
Известен ряд трансформаций тироксина, важнейшая из которых заключается в его монодейодировании в положении 5 и 5'. Монодейодирование тироксина происходит под действием специфической дейодазы, отличающейся от йодтирозин-дейодазы, с образованием 3,5,3'-трийодтиронина (Т3) и 3,3',5'-трийодтиронина — так называемого обратного трийодтиронина (oT3), не обладающего гормональной активностью, которые также секретируются в кровь. В щитовидной железе взрослого человека в сутки в среднем вырабатывается 87 мкг тироксина, из которых около 8 мкг превращаются в трийодтиронин, 0,9 мкг — в оТ3, а основная масса гормона поступает в кровоток без изменений. Большая часть Т3 образуется в печени, которая принимает активное участие в метаболизме тироксина. Соотношение между количеством Т3 и оТ3, изменяется при некоторых физиологических и патологических состояниях. Физиологическая активность Т3 в 5—10 раз выше, чем физиологическая активность тироксина. Процесс образования оТ3 рассматривают как путь изъятия избыточного количества тироксина из обмена веществ. В неизмененном виде с мочой или калом экскретируется только небольшое количество тиреоидных гормонов.
Для Т. г. не установлены специфические органы-мишени и до сих пор нет общепринятой теории, объясняющей их влияние на обмен веществ на молекулярном уровне. Предполагают, что тироксин является регулятором обмена веществ во всех чувствительных к нему тканях и, вероятно, это действие осуществляется путем присоединения гормона к клеточному ядру с первоначальным влиянием на активность ДНК-зависимой РНК-полимеразы и последующим повышением интенсивности синтеза белка. Аналогичный, но не постоянный эффект тироксин может оказывать и на митохондрии. Повышенное поглощение кислорода тканями типично для тиреотоксикоза. Однако тиреоидная стимуляция окислительного фосфорилирования в митохондриях оказалась сопряженной с тканевым дыханием, за исключением случаев тяжелого тиреотоксикоза. Тироксин вначале стимулирует энергопотребляющую систему, например активный трансмембранный перенос ионов Na+, за которым следуют повышение поглощения кислорода тканями, усиление синтеза белка, необходимое для образования митохондрии, и наполнение их ферментами, а также усиливает синтез дыхательных ферментов в тканях.
Содержание тироксина в крови в норме составляет 4—11 мкг/100 мл. Количество его повышено при зобе диффузном токсическом, различных заболеваниях, сопровождающихся тиреотоксикозом, и понижено при гипотиреозом. Тироксин обнаружен и в грудном молоке; его концентрация в первые дни лактации составляет 0,6—1,5 мкг/100 мл, она относительно низка по сравнению с содержанием гормона в сыворотке крови матери, но постепенно к 3—4-й неделе концентрация тироксина достигает 7,3—12,9мкг/100 мл.
Тироксин входит в состав лекарственных средств, используемых для заместительной терапии при гипофункции щитовидной железы, — тиреоидина, L-тироксина-100, синтетически комбинированных препаратов.
Трийодтиронин вырабатывается в щитовидной железе в количестве, во много раз меньшем, чем тироксин. Биосинтез Т3 происходит аналогично биосинтезу тироксина в составе молекулы тиреоглобулина. Метаболизм трийодтиронина в организме осуществляется путем постепенного дейодирования Т3 и оТ3 с последовательным образованием дийодтиронинов (Т2), монойодтиронина (T1) и, наконец, тиронина, полностью лишенного атома йода. Трансаминирование и окислительное дезаминирование трийодтиронина происходят во многих органах. Продукт этих превращений 3,5,3'-трийодтиреоуксусную кислоту обнаруживают в моче и желчи.
Действие трийодтиронина аналогично физиологическому эффекту тироксина. Полагают, что главной мишенью для трийодтиронина является генетический аппарат клетки, т.к. этот гормон отличается большим сродством к ядерным участкам связывания. Рецепторные участки в ядре для тироксина и трийодтиронина идентичны, и эти гормоны конкурируют за них, однако сродство клеточных ядерных рецепторов к трийодтиронину в 4—10 раз выше, чем к тироксину. Трийодтиронин связывается преимущественно с хроматином ядра. Возможно, связывание трийодтиронина с ядерными рецепторами стимулирует транскрипцию ДНК с последующим усилением синтеза РНК и белка. Количество мест связывания гормона в различных органах коррелирует с чувствительностью ткани к Т. г. Больше всего трийодтиронина связывается в гипофизе; полагают, что регуляция секреции тиреотропного гормона по принципу обратной связи осуществляется благодаря именно этому процессу.
В крови трийодтиронин циркулирует в виде комплекса с глобулином, однако его связи с белком гораздо слабее, чем у тироксина, что объясняет высокую скорость оборота трийодтиронина в организме (период его биологической полужизни равен 2 дням) и низкую концентрацию этого гормона в крови несмотря на его непрерывное поступление в кровоток из щитовидной железы, а также из печени и почек. Содержание свободного трийодтиронина, не связанного с белками, составляет всего 0,2% от его общего количества в крови здорового человека, которое в среднем
равно 45—180 нг/100 мл.
При тиреотоксикозе содержание трийодтиронина в крови значительно повышается параллельно повышению концентрации тироксина. Однако описаны случаи так называемого трийодтиронинового тиреотоксикоза, илиТ3-тиреотоксикоза, вызванного избыточным содержанием в крови Т3, в то время как концентрация Т4 остается нормальной. Трийодтирониновый тиреотоксикоз составляет примерно 5% всех случаев тиреотоксикоза. Чаще всего он отмечается у больных с тиреотоксикозом, уже лечившихся ранее, у которых, однако, несмотря на нормальную концентрацию тироксина в крови сохраняются клинические признаки тиреотоксикоза. Клиническая картина трийодтиронинового тиреотоксикоза не отличается от таковой при обычном тиреотоксикозе. Частота встречаемости симптомов тиреотоксикоза, обусловленных
изолированным повышением концентрации трийодтиронина в крови, при тиреотоксической аденоме гипофиза достигает 20—30%.
Содержание оТ3 в крови здоровых людей колеблется в пределах 30—60 нг/100 мл. Концентрация оТ3 в крови увеличивается (а концентрация Т3 параллельно снижается) при голодании, системных хронических заболеваниях, циррозе печени.
Для оценки содержания Т. г. в крови и других биологических субстратах широко применяют так называемые радиолигандные методы, которые позволяют специфически определять Т4, Т3 и другие йодированные компоненты. Один из этих методов — радиоиммунологический метод — с помощью специальных стандартных наборов позволяет с высокой степенью точности установить концентрацию Т4 в сыворотке крови.
