
- •Глава 16
- •16.1.3. Нахождение в природе, изотопный состав
- •16.1.4. Краткие исторические сведения
- •16.2. Простые вещества
- •16.2.1. Кислород и озон
- •16.2.1.1. Двухатомная молекула 02
- •16.2.1.2. Трехатомная молекула кислорода — озон
- •16.2.2. Сера, селен, теллур, полоний
- •16.3. Сложные соединения элементов 16-й группы
- •16.3.1. Особенности строения и свойств кислородных соединений
- •16.3.1.1. Классификация оксидов
- •16.3.1.2. Оксиды с преимущественно ионной связью
- •16.3.1.3. Оксиды с ковалентной связью элемент-кислород
- •16.3.1.4. Пероксиды, надпероксиды, пероксокислоты
- •16.3.1.5. Соединения кислорода в положительной степени окисления
- •16.3.1.6. Комплексы молекулярного кислорода
- •16.3.2. Кислородные соединения элементов подгруппы серы
- •16.3.2.3. Низкие степени окисления
- •16.3.2.4. Кислородные соединения, содержащие цепочки —э—э—
- •16.3.3. Водородные соединения (гидриды) и их соли
- •16.3.3.1 Гидриды
- •16.3.3.2. Сульфиды элементов-металлов
- •16.3.4. Соединения с галогенами
- •16.3.5. Соединения с азотом
- •16.4. Комплексообразование с участием элементов 16-й группы
- •16.5. Биологическая роль элементов 16-й группы
16.2. Простые вещества
Простые вещества, образуемые легкими элементами 16-й группы ПС, проявляют свойства неметаллов. Благодаря большому числу валентных электронов и малому размеру атомов (см. табл. 16.1), эти элементы устойчивы в гомоатомных соединениях, поскольку формируют заполненные 8-электронные оболочки за счет образования ковалентных связей между однородными атомами.
Таблица 16.4. Свойства простых веществ, образованных элементами 16-й группы.
-
Элемент
ТПЛ, 0С
ТКИП, 0С
Структура
Плотность, г/см3
О
-219 (О2)
-192,7 (О3)
-183 (О2)
-111,9 (О3)
Двухатомная молекула О2
Угловая молекула О3
1,141 (жидкий)
1,354 (жидкий)
S
112,8 (ромб.)
119 (монокл.)
444,6
S8, кольцо
2,07 (ромб.),
1,96 (монокл.)
Se
220 (гексагон.)
685
Серый селен - гексагональный,
красный селен - аморфный
4,807
Те
450 (гексагон.)
990
Гексагональный теллур
6,24
Ро
254
962
α-форма - кубическая,
β-форма - ромбоэдрическая
9,4
Для кислорода, имеющего самый маленький размер атома во 2-м периоде ПС и в 16-й группе, как и для его соседа по периоду азота, энергетически очень выгодно состояние двухатомной молекулы с кратной ковалентной связью (см. разд. 16.1.2). У серы и селена, благодаря их большому радиусу, прочность кратных связей в гомоатомных веществах понижается, но зато возрастает прочность одинарных связей. Это приводит к увеличению числа атомов в молекулах: наиболее стабильное состояние - S8 и Se8. Образование цепочек - Sn - называется катенацией. У теллура и особенно у полония устойчивее более короткие цепочки - Э2, так как уменьшается прочность одинарных ковалентных связей Э-Э. Наряду с этим появляются признаки металлического состояния: простые вещества Те и Ро имеют металлический блеск и электропроводны. Естественно, что переход от молекулярной структуры (О, S, Se) к металлической (Те, Ро) сопровождается повышением ТПЛ и ТКИП простых веществ (табл. 16.4).
16.2.1. Кислород и озон
Кислород как простое вещество представлен двумя аллотропными модификациями: в форме обычных двухатомных молекул О2 (собственно кислород) и в форме О3 - озона (см. разд. 14.2.1).
16.2.1.1. Двухатомная молекула 02
Электронная оболочка изолированного атома кислорода с позиций МВС имеет следующее строение:

В соответствии с правилом Гунда только два электрона изолированного атома кислорода находятся в неспаренном состоянии, а два других электрона образуют на 2p-подуровне дублет с антипараллельным спином.
С позиций метода МО два атома кислорода сближаются, образуя молекулярные орбитали, причем в этом процессе принимают участие только электроны 2s- и 2p-подуровней, а электроны 1s-уровня в связи не участвуют. Взаимное расположение 3σСВ- и 1πСВ-МО (рис. 16.1) отличается от расположения аналогичных МО молекулы азота (см. разд. 15.2.1).
2О0 = 2[1s22s22p4] = O2[КК (1σСВ)2(2σ*)2(3σСВ)2(1πСВ)4(2π*)2] или
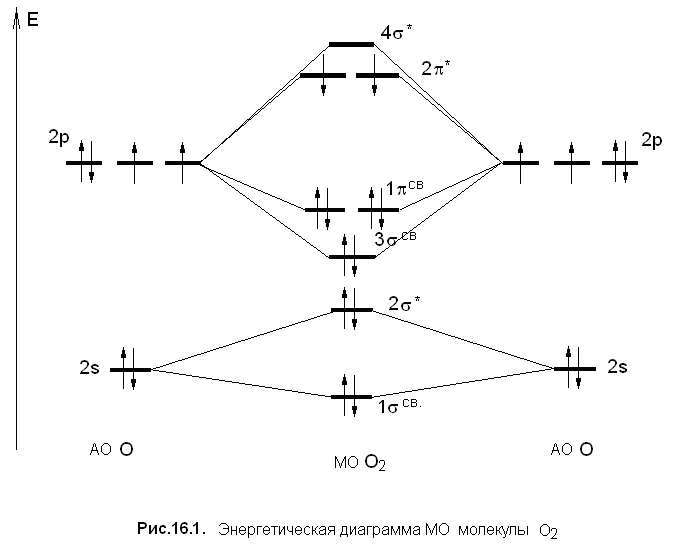
Объясняют такой порядок МО тем, что у элементов конца второго периода велика разница в энергии 2s- и 2p-АО (у кислорода 14,9 эВ, у фтора 20,4 эВ, у неона 26,8 эВ, тогда как у азота 6,0 эВ), поэтому при образовании МО кислорода взаимодействие этих орбиталей практически отсутствует, т.е. 1σСВ- и 2σ*-МО формируются только из 2s-AO, а 3σСВ- и 4σ*-МО - из 2р-АО. В соответствии с рис. 16.1 у молекулярного кислорода на каждой из двух вырожденных 2π*-МО размещается по одному электрону с параллельными спинами, так как, согласно правилу Гунда, 2 электрона на двух одинаковых по энергии орбиталях в основном состоянии молекулы (с минимальной энергией) должны иметь максимальный суммарный спин. Эти неспаренные электроны и обусловливают парамагнетизм молекулярного кислорода, впервые установленный экспериментально М.Фарадеем в 1848 г.
Электронное строение молекулярного кислорода в основном (невозбужденном) состоянии называют триплетным, это - парамагнитный кислород. При возбуждении тем или иным видом энергии кислород О2 переходит в синглетное состояние, при котором неспаренные электроны остаются на разных 2π*-МО. но приобретают антипараллельный спин, или, при еще большем возбуждении, образуют электронную пару, переходя на одну из 2π-МО. Энергии этих состояний выше основного на 94,72 и 157,85 кДж/моль соответственно.
В обоих случаях кислород в синглетном состоянии (с нулевым суммарным спином) теряет парамагнетизм. При переходе в синглетное состояние расстояние О—О увеличивается сначала до 1,2155 Å, а затем до 1,2277 Å вместо 1,2074 Å в невозбужденной молекуле О2. Удлинение связи О—О в синглетном кислороде повышает его химическую активность, так как молекула О2 становится менее прочной.
Молекулярный кислород, благодаря ковалентной природе молекул О2, представляет собой типичный газ (см. табл. 16.4) с низкими температурами плавления и кипения. Критическая температура его низкая -118,40С, критическое давление 50,15 атм. Значит, чтобы перевести кислород в жидкое состояние, необходимо сначала охладить его до температуры ниже критической, а потом подвергнуть действию высокого давления.
Первая машина для сжатия воздуха была предложена немецким инженером К.Линде и английским инженером В. Гампсоном одновременно и независимо друг от друга в конце XIX века. Машина давно уже устарела, но принцип ее действия применяется в современных агрегатах для получения сжиженных газов и состоит в следующем. Воздух сжимают под давлением 100 атм, при этом он разогревается Горячий воздух пропускают через холодильник, где он приобретает комнатную температуру, а затем давление воздуха резко понижают до 10 атм. В результате расширения воздух охлаждается. Температура его падает на 300 (эффект Джоуля - Томсона). Используют трубки с двойными (концентрическими) стенками - по наружной трубке идет расширяющийся (охлаждающийся) газ, по внутренней трубке – сжимаемый (охлаждаемый наружным) газ. При многократном повторении этого цикла можно охладить кислород воздуха до температуры более низкой, чем критическая. Тогда при очередном охлаждении, происходящем вследствие расширения газа и сопровождающемся падением его давления, газ переходит в жидкое состояние.
На современных заводах работают установки непрерывного действия, в которых сжижаемый газ проходит через так называемый этандер - расширитель - и непрерывно подвергается расширению, а затем тоже непрерывно сжатию. Прерывность, цикличность, характерная для машины Линде - Гампсона, здесь устранена.
Чтобы получить в лаборатории жидкий кислород, можно газообразный кислород, взятый, например, из баллона, пропустить через змеевик, погруженный в жидкий азот. Кислород при этом сжижается, так как его температура становится на несколько десятков градусов ниже температуры кипения. Жидкий кислород хранят в сосудах Дьюара.
Сжиженный кислород - это светло-голубая, почти бесцветная жидкость; вылитый из сосуда Дьюара в стеклянный стакан, он кипит до тех пор, пока стенки стакана не охладятся до температуры ниже ТKИП кислорода. Если опыт проводят не в сухой камере, стенки стакана с жидким кислородом покрываются инеем: пары воды, присутствующие в воздухе, конденсируются на холодной поверхности.
Как хорошо известно, тлеющая лучинка в газообразном кислороде вспыхивает. Если опустить тлеющую лучинку в жидкий кислород, она с треском воспламеняется и горит в нем. Тлеющая лучинка не гаснет, хотя температура жидкого кислорода очень низкая. Это объясняется тем, что горение сопровождается выделением большого количества энергии, и выделяющееся тепло перекрывает охлаждение.
Древесный уголь тоже горит в жидком кислороде. Если мелко раздробленный уголь положить на вату и смочить жидким кислородом, при соприкосновении с тлеющей лучинкой происходит энергичная вспышка. При внесении нескольких предварительно нагретых угольков в жидкий кислород происходит энергичное взаимодействие углерода и кислорода, связанное с очень высокой концентрацией кислорода в системе. Уголек с большой силой вылетает из жидкого кислорода, поскольку он воспламеняется сначала только с одного конца, которым он соприкасается с жидким кислородом (принцип действия ракетного двигателя).
Смесь угольного порошка с жидким кислородом - «оксиликвит» - используют как взрывчатое вещество. По взрывчатой силе он не уступает динамиту, но гораздо более безопасен, поскольку, в отличие от динамита, со временем теряет взрывчатую силу: жидкий кислород постепенно испаряется, диффундируя через стенки патрона. Если почему-либо патрон не взорвался, через некоторое время он сам по себе обезвреживается.
Очень интересны магнитные свойства жидкого кислорода. Для экспериментальной проверки его парамагнитных свойств можно поместить между полюсами электромагнита пробирку с жидким кислородом, подвешенную на нитке. При включении магнита пробирка с жидким О2 притягивается к одному из полюсов магнита. Если выключить магнит, пробирка снова повисает между полюсами. При повторном включении тока в катушке электромагнита снова пробирка с жидким кислородом притягивается к одному из полюсов.
Парамагнитными свойствами обладает не только жидкий, но и газообразный кислород. Однако эти свойства газообразного О2 наблюдать труднее - они относительно менее сильно выражены из-за более низкой концентрации кислорода.
Теория Льюиса, а также метод валентных связей, в отличие от метода магнитных орбиталей, не могут объяснить парамагнетизма молекулярного кислорода. С позиций МВС молекулярный кислород должен обладать диамагнитными свойствами, так как согласно МВС, в молекуле О2 существует двойная двухэлектронная ковалентная связь:

Это исключает возможность присутствия в О2 неспаренных электронов, обусловливающих парамагнетизм.
Кислород (газ) в сравнимых условиях несколько тяжелее, чем воздух. Так, если 1 л воздуха при н. у. имеет массу 1,293 г, то 1 л кислорода при тех же условиях - 1,429 г. Плотность жидкого О2 равна 1,141 г/см3.
Молекулярный кислород, будучи ковалентным соединением с молекулярной структурой, в полярном растворителе - воде растворяется плохо: в 100 объемах Н2О при обычном давлении растворяется 4,89, 3,16 и 1,70 объемов О2 (при 0, 20 и 1000С соответственно). Но в неполярных жидкостях он растворяется очень интенсивно, поэтому чтобы насытить их кислородом достаточно простого перемешивания неполярных растворителей на воздухе.
Остановимся теперь на окислительных свойствах молекулярного кислорода. Обычно считают, что окислительная способность кислорода связана с тем, что нейтральный атом кислорода, присоединяя два электрона, превращается в отрицательно заряженный двухзарядный ион, имеющий устойчивую 8-электронпую конфигурацию. Такие ионы действительно существуют в ряде соединений. Например, оксид кальция состоит из ионов Са2+ и О2–, электростатически связанных друг с другом. Поэтому расплав оксида кальция обладает заметной электропроводностью, и, если электролиз расплава СаО проводить в вакууме, на катоде выделяется металлический кальций, а на аноде - молекулярный кислород.
Таким образом, существование ионов О2– доказывается довольно просто.
Однако в подавляющем большинстве кислородных соединений связь между атомами кислорода и других элементов носит не ионный, а в значительной мере ковалентный характер. Так, если партнером кислорода является водород, обладающий сильным поляризующим действием, то вместо ионной связи в молекуле Н2О возникает ковалентная полярная связь. Если же взаимодействуют одинаковые атомы, например, в молекуле О2, то возникающая ковалентная связь носит неполярный характер.
Несколько неожиданным оказывается тот факт, что присоединение двух электронов к атому кислорода является эндотермическим процессом. Действительно, если объединение двух атомов кислорода в молекулу О2 сопровождается выделением 493,6 кДж, а присоединение одного электрона к каждому из двух атомов кислорода - выделением 141,0 кДж (сродство кислорода к электрону), то для того чтобы присоединить еще по одному электрону и образовать 2 иона О2–, надо затратить более 1400 кДж/моль. Тем не менее, как уже упоминалось, такие ионы существуют, и известно много соединений, их содержащих. Несомненно, что существование ионов О2– возможно лишь в том случае, если в процессе образования соединения есть стадия, связанная с выделением большого количества энергии. Например, объединение ионов Са2+ и О2– в кристаллический оксид СаО сопровождается выделением большого количества энергии в результате сильного электростатического взаимодействия ионов Са2+ и О2–. Выделение энергии кулоновского взаимодействия при образовании кристаллической структуры, а также некоторый энергетический выигрыш в стадии образования О– перекрывают затраты энергии на диссоциацию молекулы и на присоединение второго электрона к атому кислорода.
Диссоциация О2 с образованием атомного кислорода протекает довольно легко. В частности, установлено, что на освещенной части нашей планеты молекулярный кислород атмосферы в значительной мере диссоциирует.
Очевидно, что рекомбинация атомного кислорода должна сопровождаться выделением энергии. Предложен проект использования процесса рекомбинации (моляризации) атомного кислорода, содержавшегося в атмосфере, для создания световых реклам. Полагают, что, «выстреливая» в атмосферу катализатором моляризации кислорода, можно получить световой эффект в результате выделения энергии рекомбинации: 2ОАТ = О2.
Молекулярный кислород - очень активный химический реагент. Со многими веществами, например с металлами, О2 взаимодействует уже при обычной температуре, а при повышенной температуре с О2 реагируют большинство химических соединений (и простых, и сложных).
К числу характерных для кислорода реакций относится его взаимодействие с металлами и неметаллами, в результате которого, как правило, образуются оксиды.
В железную ложечку помещают немного серы и нагревают в пламени газовой горелки до температуры, несколько более высокой, чем ТПЛ серы, чтобы сера загорелась. Пламя ее на воздухе почти незаметно. При внесении ложечки с горящей серой в колбу с кислородом, на дно которой насыпан песок (если на дно колбы попадет раскаленный продукт реакции, она может треснуть), сера горит ярким синим пламенем:
S
+ О2
![]() SO2.
SO2.
Таким образом, в кислороде сера горит намного интенсивнее, чем на воздухе: по сравнению с чистым О2 концентрация кислорода в воздухе в пять раз меньше.
Другой неметалл - фосфор также на воздухе горит менее активно, чем в кислороде. Чтобы убедиться в этом, нужно кусочек белого фосфора слегка нагреть на пламени горелки, затем загоревшийся на воздухе фосфор внести в колбу с кислородом. Пламя становится ослепительно белым:
Р4 + 5О2 Р4О10,
Опять увеличение концентрации кислорода повысило интенсивность горения неметалла.
Если предварительно нагреть кусочек древесного угля на горелке, чтобы он начал тлеть с одного конца, и внести уголек в колбу с кислородом, то в кислородной атмосфере уголь сильно раскаляется:
С + О2 СО2.
Интересно, что при таком взаимодействии не образуется пламени: уголек, постепенно раскаляясь, как бы исчезает.
Можно сжечь в кислороде один из самых обычных металлов - железо. Для этого закрепляют на железной проволоке спичку и все это укрепляют на железной ложечке. Подожженная спичка, сгорая в кислороде, разогревает железо, которое загорается и горит очень интенсивно - может даже загореться ложечка, к которой прикреплена проволока (если хватит кислорода):
3Fe + 2О2 Fе3O4.
Если с кислородом реагируют активные металлы (ЩМ и ЩЗМ), то образуются пероксиды и надпероксиды (см. разд. 1.3.2.1 и 2.3.1), содержащие группировки О22- и О2– соответственно.
Относительной устойчивостью обладают пероксиды только этих элементов: подвижные электронные оболочки ионов О22–, О2– сильно деформируются и разрушаются под действием ионов, обладающих более сильным поляризующим действием, чем катионы ЩЭ и ЩЗЭ.
