
- •1. Интерференция света.
- •4 Интерференция света в тонких пленках.
- •7 Дифракция света.
- •8 Разрешающая способность объектива.
- •18 Электронная теория дисперсии.
- •19 Фазовая и групповая скорости света.
- •13 Поляризация света.
- •16 Пластинки в 1/4 и 1/2 длины волны.
- •23 Формула Рэлея-Джинса.
- •25 Законы фотоэффекта
- •29 Давление света
- •28 Эффект Комптона и его теория.
- •26 Тормозное рентгеновское излучение и его коротковолновая граница.
- •41 Рентгеновские характеристические спектры. Закон Мозли.
- •31 Боровская теория атома.
- •32 Волновые свойства частиц.
- •35 Волновая функция и ее статистический смысл.
- •47 Строение атомного ядра.
- •50 Радиоактивность. Ядерные реакции.
41 Рентгеновские характеристические спектры. Закон Мозли.
При достаточно большой энергии электронов на фоне сплошного спектра появляются резкие линии- линейчатый спектр определяемый материалом анода и называемый характеристическим рентгеновским спектром.
![]() v-
частота соответствующая данной линии,
R-
постоянная Ридберга,
- постоянная экранирования
v-
частота соответствующая данной линии,
R-
постоянная Ридберга,
- постоянная экранирования
******************************************************************
31 Боровская теория атома.
Серии
в спектре атома водорода могут быть
описаны обобщённой формулой Бальмера
![]() R=3,29
1015
R=3,29
1015
1
постулат Бора : в атоме существуют
стационарные состояния в которых он не
излучает энергии. В стационарном
состоянии электрон , двигаясь по круговой
орбите, должен иметь дискретные
квантованные значения момента импульса
удовлетворяющие условию
![]()
2
постулат Бора : при переходе электрона
с одной стационарной орбиты на другую
излучается (поглощается) один фотон с
энергией
![]() (при Em<En
– излучение). набор возможных дискретных
частот квантовых переходов и определяет
линейчатый спектр атома.
(при Em<En
– излучение). набор возможных дискретных
частот квантовых переходов и определяет
линейчатый спектр атома.
Боровская теория водородного атома.
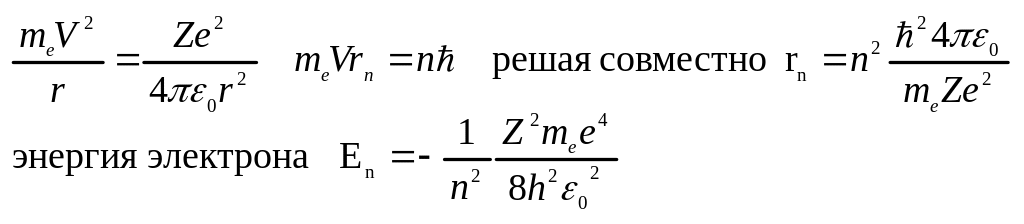
n – главное квантовое число, n=1 – основное энергетич. состояние.
n>1 – возбуждённое состояние.
32 Волновые свойства частиц.
Гипотеза де Бройля. Длина волны де Бройля.
де
Бройль утверждал что не только фотоны,
но и электроны и любые другие частицы
материи наряду с корпускулярными
обладают также волновыми свойствами.
таким образом любой частице обладающей
импульсом сопостовляют волновой процесс
с длиной волны
![]()
35 Волновая функция и ее статистический смысл.
необходимость
вероятностного подхода к описанию
микрочастиц является важнейшей
отличительной особенностью квантовой
теории. По волновому закону меняется
не сама вероятность , а величина названная
амплитудой вероятности (
(x,y,z,t))
эту величину называют также волновой
функцией. Амплитуда вероятности может
быть комплексной и вероятность W
пропорциональна квадрату её модуля.
![]() .
описание состояния микрообъекта с
помощью волновой функции имеет
статистический , вероятностный характер.
.
описание состояния микрообъекта с
помощью волновой функции имеет
статистический , вероятностный характер.
Уравнение Шредингера.

47 Строение атомного ядра.
Атомное ядро состоит из протонов и нейтронов. протоны и нейтроны называются нуклонами общее число нуклонов называется массовым числом. Ядро характеризуется зарядом Ze где Z – зарядовое число равное числу протонов и совпадающее с порядковым номером в системе Менделеева.
![]()
ядра с одинаковыми Z но разными А наз. изотопами. , а ядра с одинаковыми А но разными Z – изобарами
Радиус ядра R = R0 A1/3 (R0 = (1.3 – 1.7)10-15)
48 Энергией связи ядра называется энергия которую необходимо затратить чтобы расщепить ядро на отдельные нуклоны.
![]()
Удельная энергия связи – энергия связи отнесённая к одному нуклону. Она характеризует устойчивость атомных ядер, зависит от массового числа А.

50 Радиоактивность. Ядерные реакции.
Радиоактивность. Закономерности - и - распадов атомных
ядер.Закон радиоактивного распада. Активность. Ядерные реак-
ции и законы сохранения.
радиоактивность – испускание радиоактивного излучения. также под радиоактивностью понимают способность некоторых атомных ядер самопроизвольно превращаться в другие ядра с испусканием различных видов радиоактивных излучений и элементарных частиц.
закон радиоактивного распада
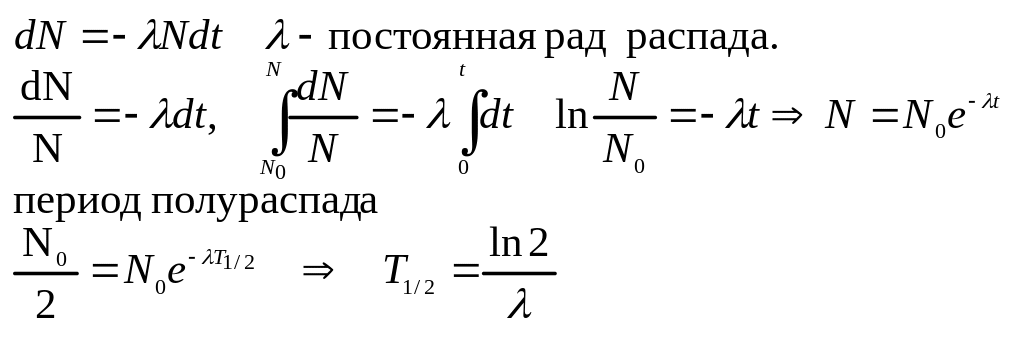
Активностью А нуклида в радиоактивном источнике называется число распадов происходящих с ядрами образца в 1 сек.
![]()
правила смещения
![]()
Ядерные реакции – это превращения атомных ядер при взаимодействии с элементарными частицами.
