
- •Влияние химического состава, фазового и структурного состояния на свойства материалов Учебное пособие
- •Введение
- •1. Некоторые вопросы строения веществ.
- •1.1 Межатомное взаимодействие.
- •1.2 Типы химических связей.
- •1.3 Кристаллическая структура твердых тел.
- •1.4. Дефекты кристаллических решеток.
- •1.4.1 Точечные дефекты решетки
- •1.4.2 Линейные дефекты кристаллической решетки.
- •1.4.3 Поверхностные дефекты кристаллической решетки.
- •1.4.4 Объёмные дефекты кристаллической решетки.
- •1.4.5 Энергетические дефекты кристаллической решетки.
- •1.5 Основы теории сплавов
- •1.6 Диаграммы состояния сплавов и закономерности Курнакова.
- •Формирование структуры материалов.
- •Кристаллизация жидкостей Условия образования зародышей в жидкости
- •Рост зародышей кристаллов
- •Формирование структуры материалов при кристаллизации.
- •Формирование структуры при конденсации.
- •Особенности воздействия на структуру материалов в твердом состоянии.
- •Превращения с изменением состава твердых фаз.
- •Распад пересыщенных растворов или старение.
- •Эвтектоидное превращение.
- •Мартенситное превращение
- •Рекристаллизация
- •Отжиг для снятия внутренних напряжений
- •1.7 Элементы зонной теории твердых тел
- •2.1 Электропроводность диэлектриков
- •2.1.1 Влияние температуры на электропроводность диэлектриков
- •2.1.2 Влияние напряженности поля на электропроводность диэлектриков
- •2.2 Поляризация диэлектриков
- •2.2.1 Упругая поляризация
- •2.2. 2 Виды поляризации релаксационного типа.
- •2.2.3 Особенности поляризации в активных диэлектриках
- •2.3 Диэлектрические потери
- •2 3.1 Влияние температуры на тангенс угла потерь неполярных диэлектриков
- •2.3.2 Влияние частоты электрического поля на тангенс угла потерь неполярных диэлектриков.
- •2.3.3 Влияние температуры на тангенс угла потерь в полярных диэлектриках
- •2.3.4. Влияние частоты электрического поля на тангенс угла диэлектрических потерь для полярных диэлектриков
- •2.4 Пробой диэлектриков
- •2.4.1 Электрический пробой газов
- •2.4.1.1 Влияние частоты электрического поля на электропрочность газов
- •2.4.2 Электрический пробой твердых диэлектриков
- •2.4.4 Электрохимический пробой диэлектриков.
- •3. Магнитные материалы
- •3.1 Общие положения
- •3.2. Природа ферромагнетизма.
- •3.2.1 Доменная структура ферромагнетиков.
- •3.2.2 Кривая намагничивания
- •3.3 Основные классы магнитных материалов.
- •3.3.1 Промышленные магнитомягкие материалы
- •3.3.1.1 Материалы для работы в постоянных и низкочастотных полях Железо
- •Электротехническая сталь
- •3.3.2 Магнитомягкие материалы для работы в слабых полях
- •3.3.3 Магнитомягкие материалы, предназначенные для работы в высокочастотных полях.
- •3.4 Магнитотвердые материалы
- •3.4.1 Промышленные магнитотвердые материалы.
- •3.4.2. Дисперсионно твердеющие сплавы
- •3.4.3 Деформируемые магнитотвердые материалы.
- •3.4.4 Магнитотвердые ферриты
- •3.4.5 Высококоэрцитивные магниты.
- •4. Проводниковые материалы
- •4.1 Материалы высокой электропроводности.
- •4.2 Материалы высокого удельного сопротивления.
- •4.2.1 Сплавы на основе меди.
- •4.2.2 Никель-хромовые сплавы.
- •4.2.3 Железохромалюминиевые сплавы
- •4.2.4 Сплавы на основе благородных металлов.
- •4.3 Материалы электрических контактов
- •4.3.1 Зажимные контакты
- •4.3.2 Цельнометаллические контакты
- •4.3.3 Материалы разрывных контактов.
- •4.3.4 Материалы скользящих контактов.
- •5. Полупроводниковые материалы
- •5.1 Элементарные полупроводники.
- •5.2 Полупроводниковые химические соединения.
- •5.2.1 Соединения типа aivbiv.
- •5.2.2 Полупроводниковые соединения типа аiiiвv.
- •5.2.3 Полупроводниковые соединения типа аiiвvi
- •Список использованной литературы
- •1. Некоторые вопросы строения веществ. 4
- •2. Диэлектрические материалы 48
- •3. Магнитные материалы 74
- •4. Проводниковые материалы 88
- •5. Полупроводниковые материалы 95
Кристаллизация жидкостей Условия образования зародышей в жидкости
Объемную составляющую свободной энергии можно определить следующим образом:
![]() (3)
(3)
где U - внутренняя энергия системы, TS - связанная энергия системы, представляющая собой произведение температуры T на энтропию S.
С ростом температуры свободная энергия любой системы снижается по кривой направленной выпуклостью вверх. Это вызвано тем, что хотя при росте температуры внутренняя энергия системы растет, связанная энергия растет еще быстрее, поскольку оба сомножителя увеличиваются.
Одни и те же атомы можно расположить упорядоченно (в этом случае имеем дело с кристаллом) или в беспорядке ( этом случае имеем дело с жидкостью). Очевидно, что энтропия жидкости выше энтропии кристаллов, поэтому производная от свободной энергии по температуре для жидкости будет больше.
В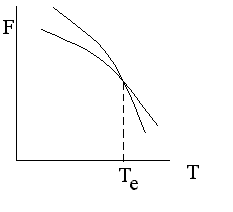 ыше
температуры равновесия Те
термодинамически
устойчивой будет жидкая фаза, а ниже
температуры равновесия устойчивой
будет твердая фаза.
ыше
температуры равновесия Те
термодинамически
устойчивой будет жидкая фаза, а ниже
температуры равновесия устойчивой
будет твердая фаза.
Важно отметить, что тепловые колебания атомов приводят к тому, что в жидкости постоянно образуются и разрушаются участки с упорядоченным расположением атомов – микрокристаллы. Аналогичным образом, в кристаллической фазе появляются микрообласти с беспорядочным строением атомов или микрообласти жидкой фазы. Образующиеся микрообласти твердой фазы в жидкости или жидкой в кристалле термодинамически не равновесны, поскольку их рост приводит к увеличению энергии системы. Более того, даже при температуре равновесия, когда свободные энергии кристаллической и твердой фаз равны, фазовое превращение развиваться не может, поскольку при фазовом превращении происходит образование поверхности раздела, а, следовательно, энергия системы растет. Поэтому для начала кристаллизации необходимо переохлаждение, а для начала плавления необходим перегрев. Только в этом случае уменьшение объемной составляющей свободной энергии превысит увеличение поверхностной составляющей свободной энергии.
Итак, кристаллизация жидкости возможна при условии:
![]() (4)
(4)
Изменение объемной компоненты свободной энергии можно записать следующим образом:
![]() (5)
(5)
где: и М – плотность и молекулярная масса зародыша кристалла; /М – число молей в единице объема; FКР и FЖД - молекулярные свободные энергии кристаллической и жидкой фаз.
Изменение свободной энергии связанное с поверхностной составляющей можно записать как
![]() (6)
(6)
где S - площадь поверхности раздела жидкой и твердой фаз, а тв-ж - поверхностное натяжение на границе раздела.
Составляющая FS всегда положительна, поскольку при всех условиях создание новой поверхности раздела требует затраты энергии. Что касается объемной составляющей свободной энергии, то ее величина и знак зависят от температуры. При температуре равновесия FV равна нулю. При температуре меньшей температуры равновесия FV отрицательна, а при температурах превышающих FV – положительна.
Совершенно очевидно, что кристаллизация будет происходить лишь в том случае, когда уменьшение объемной компоненты свободной энергии системы превысит увеличение поверхностной компоненты. Для этого требуются два условия:
1. Температура должна быть ниже температуры кристаллизации
2. Объем, самопроизвольно образующегося зародыша, должен быть достаточно большим.
Найдем минимальный объем зародыша устойчивый при кристаллизации. Для этого предположим, что форма зародыша в процессе эго роста остается неизменной. Тогда площадь поверхности зародыша можно представить как S=KV2/3 , где K - коэффициент, учитывающий форму зародыша. Изменение свободной энергии запишем как:
![]() (7)
(7)
Максимальное значение свободной энергии найдем, продифференцировав свободную энергию по объему и приравняв производную нулю:
![]() (8)
(8)
Обозначим объем зародыша кристалла, способного к росту как V и энергию системы, необходимую для образования данного кристалла как F.
Умножим последнее равенство на V:
![]() .(9)
.(9)
Тогда можно записать:
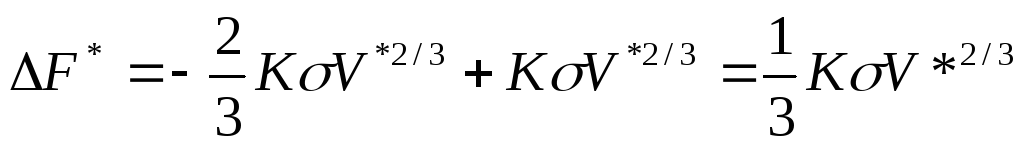
и поскольку
![]() ,
,
имеем
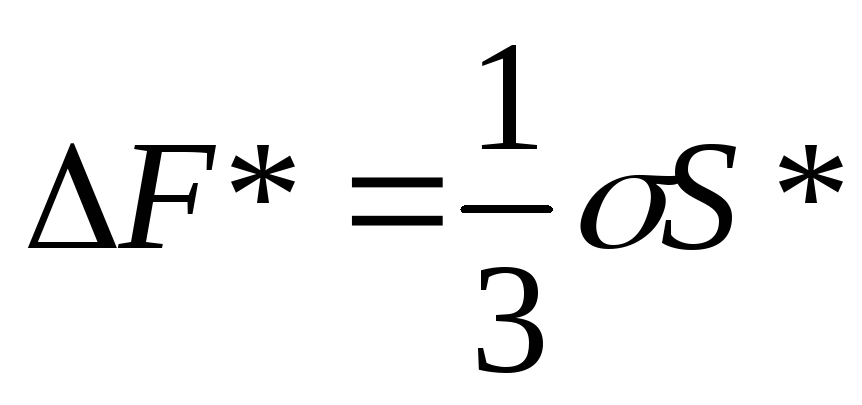 .
.
Для случая огранения зародыша разными кристаллографическими плоскостями
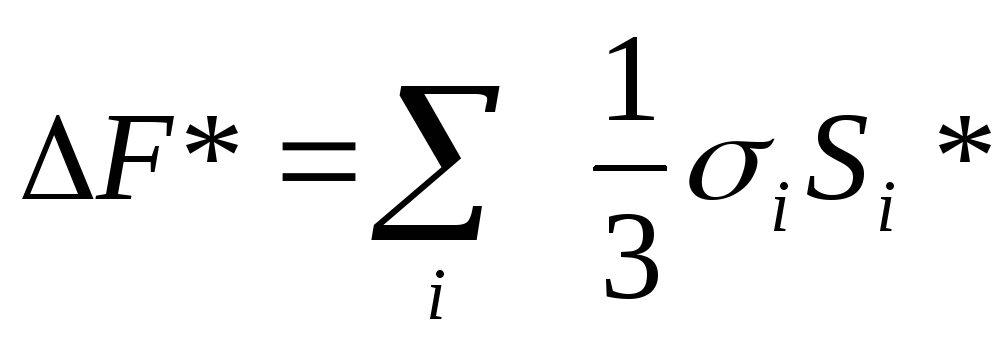 .
.
Таким образом, работа образования устойчивого зародыша критического размера равна одной трети его поверхностной энергии. Остальные две трети компенсируются выигрышем объемной свободной энергии.
Объем критического зародыша можно определить как:
![]()
В полученном выражении нет явной зависимости критического размера зародыша от температуры, а точнее от величины переохлаждения Т, равной разности между температурой равновесия жидкой и твердой фаз и фактической температурой кристаллизации.
Эту зависимость можно вывести следующим образом:
Из FV=U-TS следует, что FV=(UЖ – TSЖ)-(UТВ – TSТВ). При температуре плавления FV = 0, тогда UЖ - UТВ =Тпл(SЖ- SТВ). Или, пренебрегая зависимостью разницы энтропий и внутренних энергий от температуры:
![]()
Разница UЖ - UТВ - это теплота фазового превращения (в нашем случае теплота плавления) или в пересчете на 1 моль скрытая теплота кристаллизации L. Тогда:
![]()
( )
Таким образом, минимальный объем зародыша кристаллизации можно определить как:
![]()
Следовательно, критический объем зародыша тем меньше чем больше величина переохлаждения.
Те микрокристаллические области, которые образуются в жидкости, флуктационным путем будут расти, если их объем больше критического. Если размер микрообластей будет меньше критического, то их рост увеличит энергию системы, а, следовательно, их рост будет невозможен и они разрушатся. Рассмотрим влияние переохлаждения на скорость образования устойчивых зародышей кристаллов подробнее.
Как отмечалось выше, образование зародышей критического размера требует энергетических флуктуаций. Вероятность таких флуктуаций будет равна:
С![]() увеличением величины переохлаждения
критический объем зародыша уменьшается
и, следовательно, увеличивается
вероятность его образования.
увеличением величины переохлаждения
критический объем зародыша уменьшается
и, следовательно, увеличивается
вероятность его образования.
Важно отметить, что с понижением температуры (или с увеличением переохлаждения) уменьшается подвижность молекул, что затрудняет образование зародышей. Иначе говоря, помимо термодинамического фактора нужно учитывать и фактор кинетический.
Последний учитывается при помощи множителя exp (-Eакт/kT), где Eакт - энергия активации процесса, контролирующего подвижность атомов.
Итак, в окончательном виде зависимость скорости образования зародышей (n)от температуры будет иметь вид:
и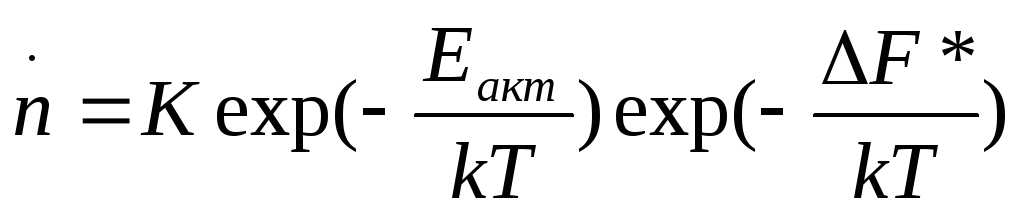 ее зависимость от величины переохлаждения
имеет вид кривой с максимумом.
ее зависимость от величины переохлаждения
имеет вид кривой с максимумом.
Расчеты показывают, что величина переохлаждения чистых жидкостей малого объема, при которых активно образуются устойчивые зародыши кристаллов, достаточно велика 0,2 Тпл. Иначе говоря, именно при таких переохлаждениях должна начаться кристаллизация. Однако, опыт показывает, что в действительности кристаллизация жидкостей начинается при существенно меньших переохлаждениях. Это связано с тем, что жидкости, как правило, содержат примеси. Наличие поверхностно-активных примесей, растворенных в жидкости, снижает поверхностное натяжение на границе раздела «кристалл-жидкость», и, тем самым, уменьшает объем критического зародыша. Наличие в жидкости нерастворенных частиц, обеспечивает появление готовых поверхностей раздела, от которых начинается кристаллизация.
