
16.2 Установление первичной структуры пептидов
Первичная структура пептидов и белков определяется путем последовательного отщепления α-аминокислот с какого-либо конца макромолекулярной цепи и их идентификации.
В настоящее время разработано много методов определения аминокислотной последовательности. Остановимся на некоторых из них :
Метод Сенгера - один из первых методов с 2,4-динитрофторбензолом (ДНФБ)

2) Метод Эдмана с фенилизотиоцианатом (ФТГ)
Преимуществом этого метода является то, что при отщеплении каждой N-концевой α-аминокислоты, остальная часть пептидной молекулы не разрушается. Такие же операции можно повторять дальше до полного определения первичной структуры и этот метод получил название деградации по Эдману (1950 год)
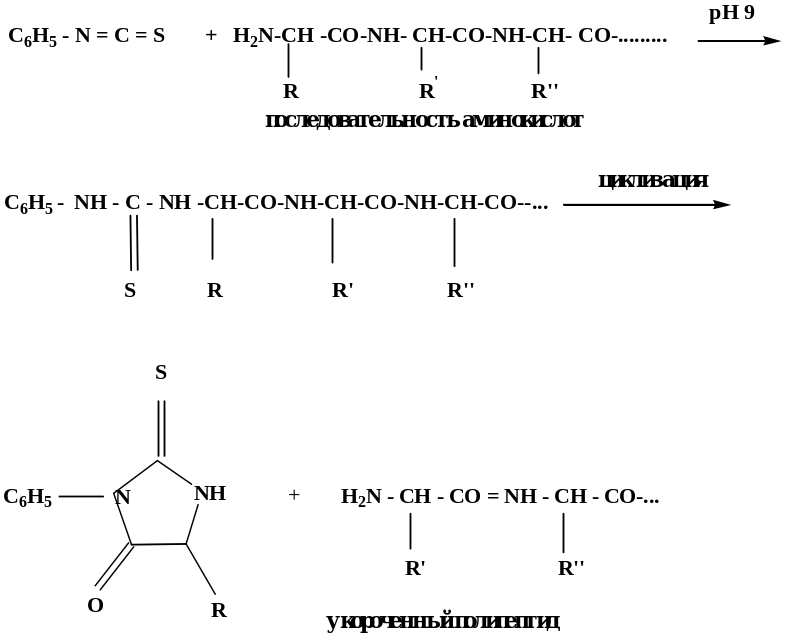
Метод Эдмана лежит в основе автоматического прибора - секвенатора (sequence от английского - последовательность). Полученное на каждой стадии производное идентифицируется либо ГЖХ либо ТСХ или жидкостной хроматографией.
16.3 Стратегия пептидного синтеза.
Схематично рассмотрим синтез дипептида ГЛИ –ЛЕЙ.
Для осуществления синтеза пептида с заданной последовательностью α-аминокислот необходимо выполнить ряд последовательных операций.
Первый этап синтеза - защита амино группы одной аминокислоты. С помощью реакций ацилирования в аминогруппу вводят электроноакцепторный заместитель. По окончанию синтеза эту защиту снимают.
В качестве реагентов для защиты чаще всего используют карбоксибензилхлорид С6Н5СН2ОСОСl или трет-бутоксикарбонилхлорид – (СН3)3СОСОСl
H 3C
3C
Н3С – С – О – СOCl + НООС – СН2 – NH2 → HOOC-CH2-NH-CO-O-C(CH3)3
H 3C
3C
БОК-защита
Это защищенное соединение обычно записывают таким образом
БОК – NH – CH2 – COOH
Второй этап синтеза – активация карбокси– N –защищенного глицина.
O
PCl5 //
БОК – NH – CH2 – COOH → БОК – NH – CH2 – C
\
Cl
Третий этап синтеза - защита карбоксильной группы второй аминокислоты можно осуществить с помощью реакции этерификации:
O
H+ //
(СН3)2СН-СН2-СН-СООН + С2Н5ОН ↔ (СН3)2СН-СН2-СН-С
│ - H2o │ \
NH2 NH2 OC2H5
Четвертый этап синтеза – образование пептидной (амидной) связи:
O
//
БОК – NH – CH2 – C + H2N – CH – COOC2H5 →
\ │
Cl CH2CH(CH3)2
БОК – NH – CH2 – CО – NH – CH – COOC2H5
│
CH2CH(CH3)2
 Защищенный
дипептид ГЛИ-ЛЕЙ
Защищенный
дипептид ГЛИ-ЛЕЙ
Пятый этап синтеза - завершающий – снятие защиты
(СН3)3С – О - СО – NH – CH2 – CО – NH – CH – COOC2H5
│
CH2CH(CH3)2
↓ HBr, CH3COOH ↓ H2O, OH‾
(CH3)2C ═ CH2 + CO2 С2Н5ОН
изобутилен H2N – CH2 – CО – NH – CH – COOH
│
CH2CH(CH3)2
ГЛИ-ЛЕЙ
Пептиды и белки являются полиэлектролитами. Рассмотрим простейшие примеры дипептидов:
ГЛИ - АЛА
H2N–CH2–CО–NH–CH–COOH ↔ H 3N+–CH2–CО–NH–CH–COO‾
│ │
CH3 СН3
ИЭТ находится в области рН≈7
ГЛИ - ГЛУ
H2N–CH2–CО–NH–CH–COOH ↔ H 3N+–CH2–CО–NH–CH–COO‾
│ │
(CH2)2 -СООН (СН2)2 - СООН
ИЭТ находится в области рН<7
ГЛИ - ЛИЗ
H2N–CH2–CО–NH–CH–COOH ↔ H 3N+–CH2–CО–NH–CH–COO‾
│ │
(CH2)4 –NН2 (СН2)4 – NН2
ИЭТ находится в области рН>7
