- •Билет №13
- •1. Дислокационная теория процесса холодной сварки
- •2. Сварочная дуга с плавящимся электродом.
- •3. Факторы влияющие на технологическую прочность при сварке
- •4. Рафинирование металла сварного шва
- •Билет №14
- •1. Ультразвуковая сварка
- •2. Расчетные схемы нагреваемого тела.
- •3.Способы повышения сопротивляемости сплавов холодным трещинам
- •4.Распределение температуры на поверхности полубескнечного тела от движущегося источника тепла.
- •Билет №15
- •1.Сварка трением
- •2. Законы теплопроводности.
- •3. Природа и механизм возникновения холодных трещин при сварке
- •4.Образование сварочной ванны и формирование шва при сварке плавлением.
- •Билет №16
- •1. Физические явления при прохождении тока через контакт. Контактная сварка.
- •2. Краевые условия дифференциального уравнения теплопроводности.
- •3. Основы металлургических процессов при сварке плавлением. Газовая фаза в зоне сварки
- •Константа равновесия процесса диссоциации при постоянном давлении р например для водорода н:
- •4. Химическая неоднородность сварного шва.
- •Билет №17
- •1. Термодинамические условия образования сварного
- •3. Основы металлургических процессов при сварке плавлением. Газовая фаза в зоне сварки
- •2. Дифференциальное уравнение теплопроводности.
- •4.Электрическая дуга.
- •Билет №18
- •4. Потоки в сварочных дугах.
- •1. Термодинамические условия образования сварного
- •2. Классификация сварочных источников тепла.
- •3. Основы металлургических процессов при сварке плавлением. Газовая фаза в зоне сварки
- •Влияние азота на свойства стали
- •Билет №19
- •1. Физическая и технологическая свариваемость
- •2. Распределение температуры на поверхности полубескнечного тела от движущегося источника тепла.
- •3. Основы металлургических процессов при сварке плавлением. Газовая фаза в зоне сварки
- •Влияние водорода на свойства стали
- •4.Силы в дуге при спэ.
- •Билет №20
- •1. Кинетика процесса сварки металлов и их сплавов в твердой фазе
- •2. Температурное поле от движущегося линейного источника тепла в бесконечной пластине.
- •3. Основы металлургических процессов при сварке плавлением. Газовая фаза в зоне сварки
- •Влияние окиси углерода на свойства стали
- •Карбидообразование
- •4. .Сварка в среде инертных газов
3. Основы металлургических процессов при сварке плавлением. Газовая фаза в зоне сварки
Физико-химические процессы (диссоциация газов, их растворение в жидком металле, химические реакции в газовой среде и при взаимодействии с металлом) оказывают большое влияние на процесс сварки и качество сварного соединения.
Диссоциация газов происходит при высоких температурах с поглощением тепла
2Н ↔ Н2 + 432,5 кДж/моль
2О ↔ О2 + 492 кДж/моль
2N ↔ N + 709 кДж/моль – молекула наиболее прочная
Константа равновесия процесса диссоциации при постоянном давлении Р например для водорода Н:
Кр = Р2Н /РН2
Для оценки диссоциации используют понятие степень диссоциации α – отношение диссоциировавших молекул к их первоначальному числу, которую определяют по уравнению Нернста:
LgKPH2=22570/Т – 1,504*lgT – 0,767
Задаваясь Т при Р=const определяем Кр ,а затем и степень диссоциации α.
Важность диссоциации при сварке:
газы в атомарном состоянии более химически активны и мало взаимодействуют с расплавленным металлом капель и сварочной ванны;
диссоциация газов в области высоких температур дуги с поглощением тепла идет одновременно с обратным процессом вблизи сварочной ванны с выделением тепла. Т.е. существует перенос тепла.
Влияние кислорода на свойства стали
Изучение особенностей растворения О, О2 в железе способно раскрыть взаимодействия его со сталью, основой которой является железо.
Железо с кислородом образует три оксида:
2Fe + O2 ↔ 2FeO ( закись, содержащая 22,7% О2).
6FeO +O2 ↔ 2Fe3O4 ( закись-окись, содержащая 27,64% О2).
4Fe3O4 + O2 ↔6Fe2O 3 (окись, содержащая 30,06% О2).
Из них только закись FeO растворима в железе и наиболее сильно влияет на его свойства. Остальные оксиды в железе не растворяются, могут присутствовать только в виде включений и легко разлагаются при высоких температурах.
Растворимость кислорода:
при температурах от комнатных до 300º составляет 0,001%;
при температуре плавления составляет 0,16%.
Наличие в стали легирующих элементов влияет на растворимость кислорода (С и Si сильно сжимают растворимость О2 ). Кислород может окислять легирующие элементы:
С + О → СО;
Мn + O → MnO;
Si + 2O → SiO2.
Закись железа может взаимодействовать с легирующими элементами:
FeO + C ↔ CO + Fe;
FeO + Mn ↔ Mn + Fe;
2Fe O + Si ↔ SiO2 + 2Fe.
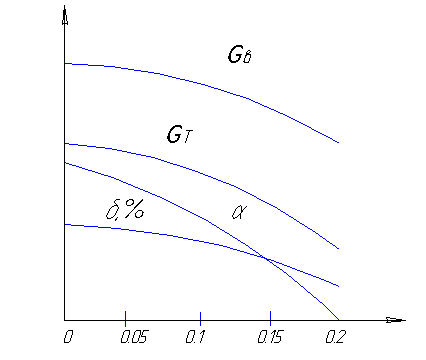
Кислород в стали ухудшает все свойства: пределы прочности σв и текучести σт , относительное удлинение δ,% и ударная вязкость α.
С ростом кислорода :
уменьшается стойкость против коррозии;
растет склонность к старению;
при О2 >0,08% возникает хладно и красноломкость;
усиливается рост зерен при нагреве;
ухудшается обрабатываемость резанием и ковка;
понижается магнитная проницаемость и увеличивается электрическое сопротивление.