
- •Основные законы геометрической оптики. Полное внутреннее отражение. Принцип Ферма.
- •Зеркала, тонкие линзы, основные оптические приборы.
- •Фотометрические величины. Интенсивность, световой поток, поверхностная яркость, освещенность.
- •Принцип Гюйгенса. Когерентные волны. Интерференция волн. Оптическая разность хода.
- •П олосы равного наклона и равной толщины. Кольца Ньютона. Интерферометры Майкельсона и Фабри-Перо.
- •Дифракция Фраунгофера и дифракция Френеля. Принцип Гюйгенса-Френеля. Зоны Френеля.
- •Дифракция от круглого отверстия, круглого диска, щели.
- •Дифракционная решетка. Угловая дисперсия. Разрешающая сила.
- •Голография.
- •Поляризованный свет. Поляризатор. Степень поляризации. Закон Малюса. Поляризация при отражении и преломления. Закон Брюстера.
- •Поляризация при двойном лучепреломлении. Призма Николя. Вращение плоскости поляризации. Эффект Фарадея.
- •Дисперсия света. Групповая скорость электромагнитных волн. Элементарная электронная теория дисперсии.
- •Поглощение света. Закон Бугера-Ламберта. Спектры излучения и поглощения.
- •Рассеяние света. Закон Рэлея. Эффект Вавилова-Черенкова.
- •Тепловое излучение. Энергетическая светимость. Испускательная и поглощательная способности. Абсолютно черное тело. Закон Кирхгофа. Закон Стефана-Больцмана.
- •Закон Вина. Формула Рэлея-Джинса. Формула Планка.
- •Закон фотоэффекта. Ток насыщения. Формула Эйнштейна. Красная граница фотоэффекта. Фотоны. Опыт Боте. Эффект Комптона.
- •Закономерности атомных спектров. Модели атома Томсона и Резерфорда. Постулаты Бора. Атом водорода по Бору.
- •Гипотеза де-Бройля. Опыты по дифракции корпускулярных пучков. Соотношение неопределенностей Гейзенберга.
- •Волновая функция. Уравнение Шредингера. Стационарные состояния.
- •Частица в одномерной прямоугольной потенциальной яме. Прохождение частицы через потенциальный барьер.
- •Атом водорода. Потенциалы возбуждения и ионизации. Квантовые числа. Вырожденные состояния.
- •Ширина спектральных линий. Мультиплетность спектров. Спин электрона. Магнетон Бора.
- •Спин орбитальное взаимодействие. Эффект Зеемана. Принцип Паули. Расположение элементов в системе Менделеева.
- •Ионная и ковалентная связи атомов в молекуле. Энергия диссоциации. Полная энергия молекулы. Вращательные, колебательно-вращательные полосы.
- •В ынужденное излучение. Мазеры. Лазеры. Накачка метастабильных уровней. Свойства лазерного излучения.
- •Фазовое пространство. Функция распределения. Понятие о квантовой статистике Бозе-Эйнштейна и Ферми-Дирака.
- •Колебания кристаллической решетки. Теория Дебая теплоемкости кристаллов. Энергия нулевых колебаний.
- •Квантовая теория свободных электронов в металле. Уровень Ферми. Запрещенные зоны. Валентная зона. Зона проводимости.
- •Электропроводность металлов. Сверхпроводимость. Температурные зависимости проводимости.
- •Дырочная проводимость. Примесная проводимость. Запрещенные зоны. Валентная зона. Зона проводимости.
- •Работа выхода. Термоэлектронная эмиссия. Контактная разность потенциалов.
- •Контактные явления в полупроводниках.
- •Термоэлектрические явления.
- •Основные свойства атомного ядра.
- •Масса и энергия связи. Дефект массы. Деление тяжелых и синтез легких ядер.
- •Ядерные силы. Модели ядра. Мезоны.
- •Радиоактивность. Постоянная распада. Альфа, бета и гамма-излучения.
- •Альфа-распад. Бета-распад. Правила смещения.
- •Реакция деления ядра. Цепная реакция деления.
- •Космическое излучение. Типы взаимодействия элементарных частиц. Частицы и античастицы.
- •Классификация элементарных частиц. Кварки.
Закономерности атомных спектров. Модели атома Томсона и Резерфорда. Постулаты Бора. Атом водорода по Бору.
Согласно модели Дж. Дж. Томсона (1903), атом представляет собой непрерывно заряженный положительным зарядом шар радиусом порядка 10–10 м, внутри которого около своих положений равновесия колеблются электроны; суммарный отрицательный заряд электронов равен положительному заряду шара, поэтому атом в целом нейтрален. Через несколько лет было доказано, что представление о непрерывно распределенном внутри атома положительном заряде ошибочно.
Резерфорд в 1911 г. предложил ядерную (планетарную) модель атома. Согласно этой модели, вокруг положительного ядра, имеющего заряд Zе (Z — порядковый номер элемента в системе Менделеева, е — элементарный заряд), размер 10–15—10–14 м и массу, практически равную массе атома, в области с линейными размерами порядка 10–10 м по замкнутым орбитам движутся электроны, образуя электронную оболочку атома. Так как атомы нейтральны, то заряд ядра равен суммарному заряду электронов, т. е. вокруг ядра должно вращаться Z электронов.
Исследования спектров излучения разреженных газов (т. е. спектров излучения отдельных атомов) показали, что каждому газу присущ определенный линейчатый спектр, состоящий из отдельных спектральных линий или групп близко расположенных линий. Самым изученным является спектр наиболее простого атома — атома водорода.
Первый постулат Бора (постулат стационарных состояний): в атоме существуют стационарные (не изменяющиеся со временем) состояния, в которых он не излучает энергии. Стационарным состояниям атома соответствуют стационарные орбиты, по которым движутся электроны. Движение электронов по стационарным орбитам не сопровождается излучением электромагнитных волн.
В стационарном состоянии атома электрон,
двигаясь по круговой орбите, должен
иметь дискретные квантованные значения
момента импульса, удовлетворяющие
условию![]() (1)
где те — масса электрона,
v — его скорость
по n-й орбите радиуса
rn,
ћ = h/(2).
(1)
где те — масса электрона,
v — его скорость
по n-й орбите радиуса
rn,
ћ = h/(2).
Втором постулат Бора (правило частот):
при переходе электрона с одной
стационарной орбиты на другую
излучается (поглощается) один фотон с
энергией![]() (2)
равной разности энергий соответствующих
стационарных состояний (Еn
и Em
— соответственно энергии стационарных
состояний атома до и после излучения
(поглощения)). При Еm<Еn
происходит излучение фотона (переход
атома из состояния с большей энергией
в состояние с меньшей энергией, т. е.
переход электрона с более удаленной
от ядра орбиты на более близлежащую),
при Еm>Еn
— его поглощение (переход атома в
состояние с большей энергией, т. е.
переход электрона на более удаленную
от ядра орбиту). Набор возможных дискретных
частот
= (En—Em)/h
квантовых переходов и определяет
линейчатый спектр атома.
(2)
равной разности энергий соответствующих
стационарных состояний (Еn
и Em
— соответственно энергии стационарных
состояний атома до и после излучения
(поглощения)). При Еm<Еn
происходит излучение фотона (переход
атома из состояния с большей энергией
в состояние с меньшей энергией, т. е.
переход электрона с более удаленной
от ядра орбиты на более близлежащую),
при Еm>Еn
— его поглощение (переход атома в
состояние с большей энергией, т. е.
переход электрона на более удаленную
от ядра орбиту). Набор возможных дискретных
частот
= (En—Em)/h
квантовых переходов и определяет
линейчатый спектр атома.
Д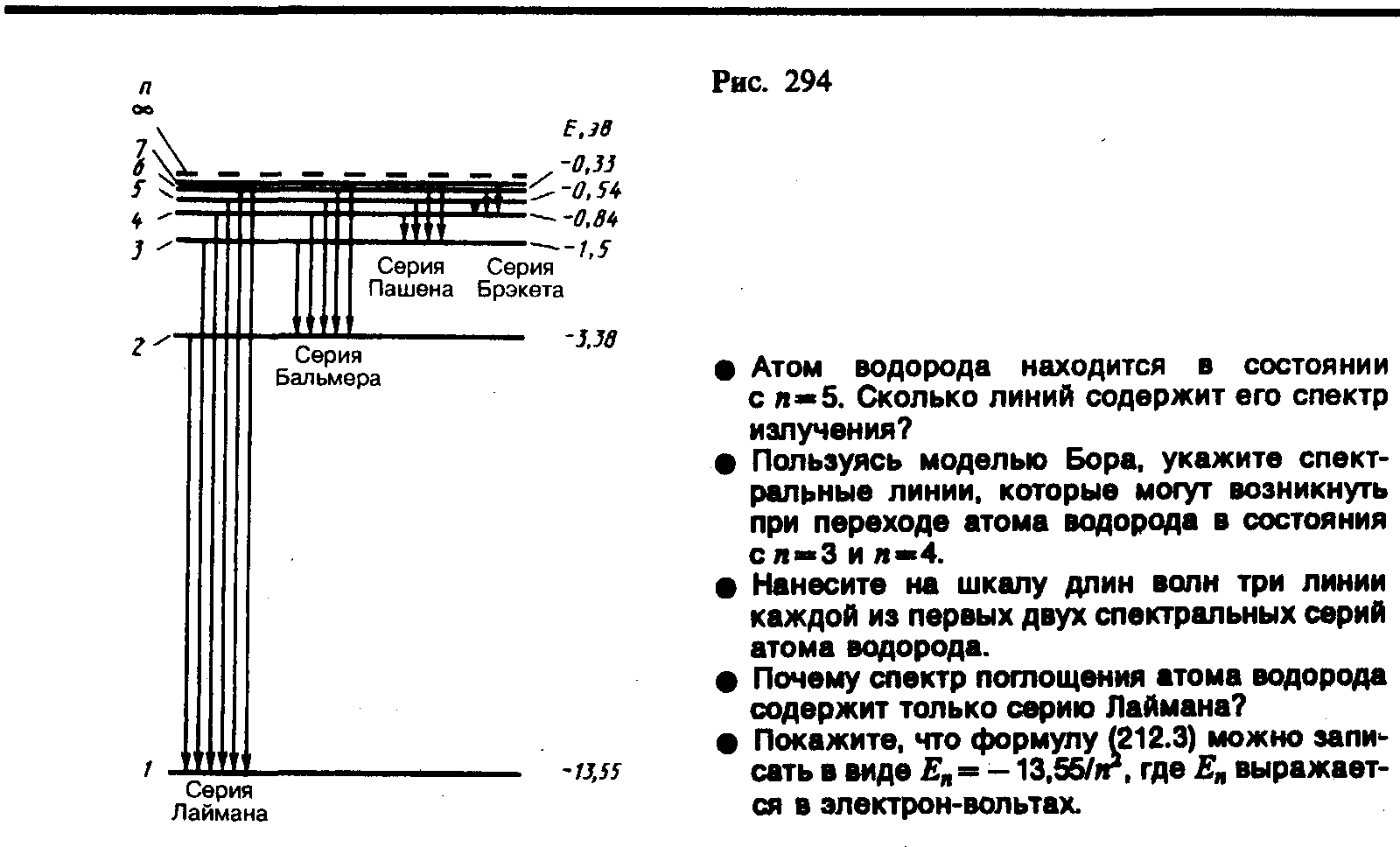 ля
атома водорода (Z = 1)
радиус первой орбиты электрона при n
= 1, называемый первым боровоским
радиусом (а), равен
ля
атома водорода (Z = 1)
радиус первой орбиты электрона при n
= 1, называемый первым боровоским
радиусом (а), равен![]() (3),
что соответствует расчетам на основании
кинетической теории газов.
(3),
что соответствует расчетам на основании
кинетической теории газов.
Энергия электрона может принимать
только следующие дозволенные дискретные
значения:![]() (4),
где знак минус означает, что электрон
находится в связанном состоянии.
(4),
где знак минус означает, что электрон
находится в связанном состоянии.
Из формулы (4) следует, что энергетические состояния атома образуют последовательность энергетических уровней, изменяющихся в зависимости от значения n. Целое число n в выражении (4), определяющее энергетические уровни атома, называется главным квантовым числом. Энергетическое состояние с n=1 является основным (нормальным) состоянием; состояния с n > 1 являются возбужденными. Энергетический уровень, соответствующий основному состоянию атома, называется основным (нормальным) уровнем; все остальные уровни являются возбужденными
