
- •Г.А.Масленникова курс лекций по органической химии
- •1 Функциональные производные карбоновых кислот
- •2 Галоидангидриды карбоновых кислот
- •Номенклатура
- •Химические свойства
- •3 Ангидриды карбоновых кислот
- •4 Сложные эфиры
- •Способы получения
- •Номенклатура
- •Физические свойства
- •Сложные эфиры
- •Химические свойства
- •Фруктовые эссенции
- •Жиры и масла
- •Значение и применение жиров и растительных масел
- •5 Амиды карбоновых кислот
- •Физические свойства
- •Химические свойства
- •6 Пероксиды ацилов. Надкислоты.
- •2 . Перекиси алкилов
- •С пособы получения
- •Химические свойства
- •3. Гидроперекиси алкилов
- •Химические свойства
- •8 Оксикислоты
- •Номенклатура
- •Изомерия
- •Химические свойства
- •9 Оксокислоты
- •Номенклатура
- •Альдегидокислоты о бщая формула
- •К етокислоты
- •Реакции в кетонной форме
- •Реакции в енольной форме
- •Реакции, не имеющие ясного отношения к таутомерии
- •10 Нитросоединения
- •I Предельные мононитросоединения.
- •Номенклатура
- •Получение
- •Строение и свойства
- •Химические свойства
- •II. Полинитроалканы
- •I II. Ароматические нитросоединения
- •11 Амины
- •Классификация
- •Номенклатура
- •Физические свойства
- •Получение
- •С троение и основность
- •I. Алифатические амины
- •Химические свойства
- •4 Токсичных амина:
- •12 Диазосоединения
- •Соли диазония
- •15 Изонитрилы (изоцианиды) (карболамины)
- •Химические свойства
- •16 Элементоорганические соединения (э – с)
- •Методы получения
- •Магнийорганические соединения
- •Получение
- •Гриньяровских реактивов
- •Алюминийорганические соединения
- •Кремнийорганические соединения
- •Получение
- •Сероорганические соединения
- •Номенклатура
- •Физические свойства
- •Химические свойства
- •Физические свойства
- •Химические свойства
- •Применение
- •Физические свойства
- •Химические свойства
- •Нуклеофильное замещение
- •17 Гетероциклические соединения
- •Классификация
- •Номенклатура
- •Химические свойства
- •1. Химические свойства, в которых отличия:
- •2. Общие химические свойства
- •Пиридин
- •18 Углеводы (ув)
- •Номенклатура
- •Классификация
- •Углеводы
- •I. Моносахариды Некоторые способы получения моноз
- •Строение
- •Стереохимия моноз Оптическая Число ассиметрических атомов углерода в оксо-форме – 4
- •Пространственная
- •II Полисахариды (полиозы)
- •Список использованных источников
2 . Перекиси алкилов
Симметричные перекиси алкилов представляют собой жидкости с эфирным, несколько резким запахом.
С пособы получения
1.
Перекиси низших спиртов очень непрочные соединения, при нагреве взрываются.
Химические свойства
1 .
Термическое или фотохимическое разложение
с образованием свободных радикалов
.
Термическое или фотохимическое разложение
с образованием свободных радикалов
3. Гидроперекиси алкилов
Г![]() идроперекиси
жирных радикалов – маслянистые жидкости
с неприятным запахом, напоминающим
запах озона, обжигающие кожу, подобно
перекиси водорода высокой концентрации.
Низшие члены этого ряда растворимы в
воде, высшие – обладают ограниченной
растворимостью.
идроперекиси
жирных радикалов – маслянистые жидкости
с неприятным запахом, напоминающим
запах озона, обжигающие кожу, подобно
перекиси водорода высокой концентрации.
Низшие члены этого ряда растворимы в
воде, высшие – обладают ограниченной
растворимостью.
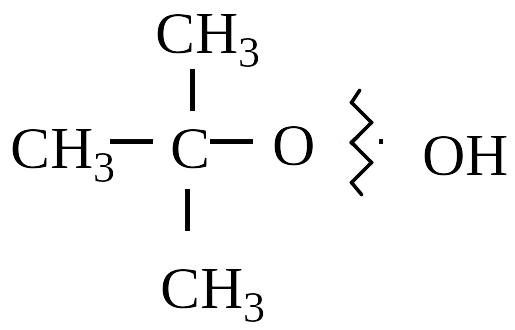
гидроперекись третичного бутила устойчива.
Получение
1 .
При окислении кетонов
.
При окислении кетонов
2 .
.
3 .
.

Химические свойства
1 .
Ионизация в полярных растворителях
.
Ионизация в полярных растворителях
2![]() .
.
3![]() .
Нуклеофильное замещение гидрокси-группы
.
Нуклеофильное замещение гидрокси-группы
4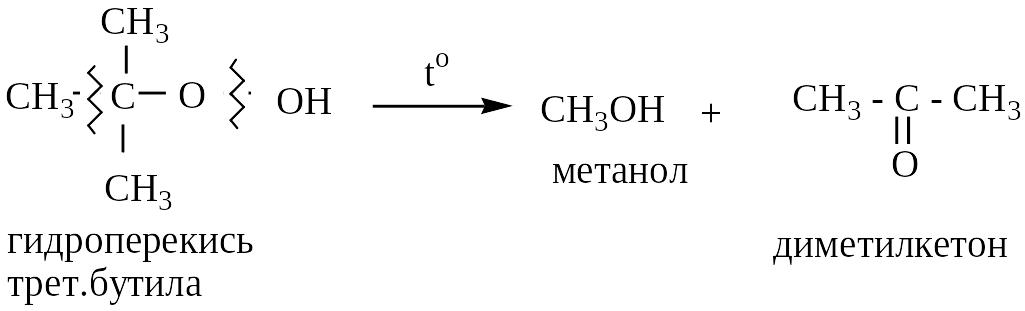 .
Термическое разложение
.
Термическое разложение
5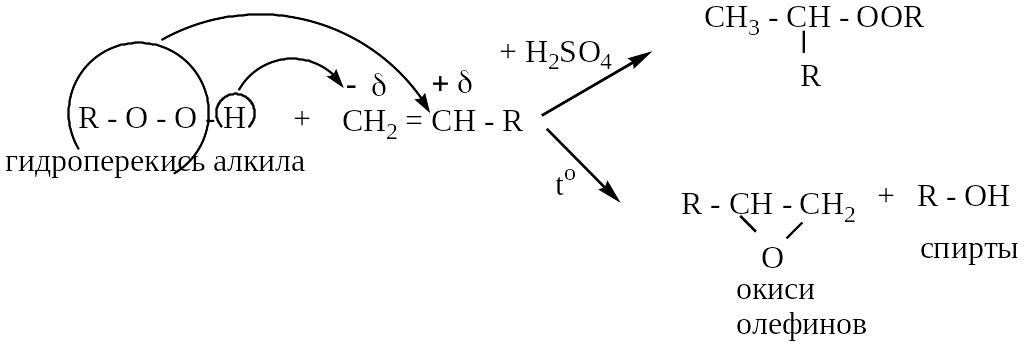 .
Взаимодействие с этиленовыми углеводородами
.
Взаимодействие с этиленовыми углеводородами
7 Галоидзамещенные карбоновые кислоты
Это карбоновые кислоты, в которых атомы водорода (один или несколько) в углеводородном радикале R замещены на атом Hal.
Классификация
1. По количеству замещенных атомов водорода на галоген (предельные, непредельные, ароматические; линейные,разветвленные).
2 .
положением галогена по отношению к
карбоксилу:
.
положением галогена по отношению к
карбоксилу:
3. Видом галогена.
Номенклатура
С
2- бромпропановая кислота
Рациональная -бромпропионовая кислота
Методы получения
1. Непосредственное галогенирование
а )
Фторирование
)
Фторирование
б )
Хлорирование
)
Хлорирование
в )
бромирование
)
бромирование
г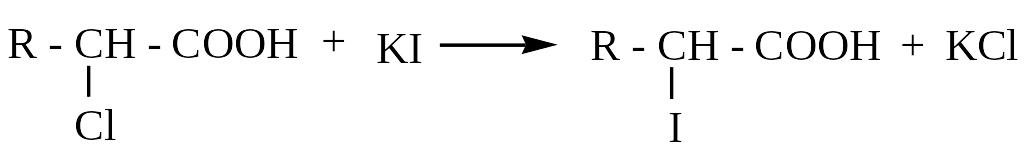 )
Йодирование (нуклеофильное замещение
атомов Cl2
или Br2
)
Йодирование (нуклеофильное замещение
атомов Cl2
или Br2
2. Получение -галоидзамещенных карбоновых кислот
Р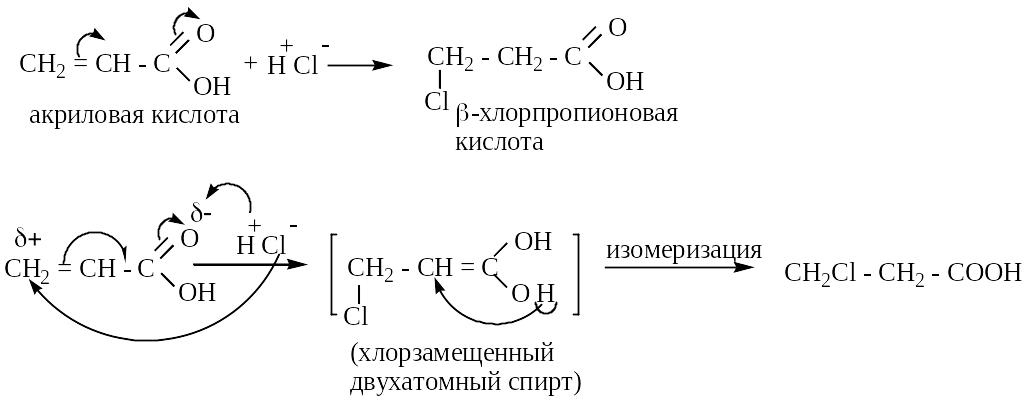 еакция
протекает не по правилу Марковникова,
т.е. всегда образуя -галоидзамещенные
производные кислот /1/.
еакция
протекает не по правилу Марковникова,
т.е. всегда образуя -галоидзамещенные
производные кислот /1/.
3. -замещенные карбоновые кислоты получают реакцией теломеризации олефинов с полигалогенпроизводными в присутствии перекисных инициаторов.
Р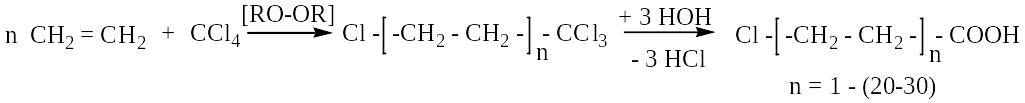 еакция
теломеризации
– частный случай цепной реакции
непредельных соединений или циклических
мономеров в присутствии веществ -
переносчиков цепи (телогенов – предельных
или непредельных соединений), образующих
концевые группы.
еакция
теломеризации
– частный случай цепной реакции
непредельных соединений или циклических
мономеров в присутствии веществ -
переносчиков цепи (телогенов – предельных
или непредельных соединений), образующих
концевые группы.
Механизм:
I – инициирование
– инициирование
II – рост цепи
п![]() ока
не израсходуется весь мономер
ока
не израсходуется весь мономер
III – передача чепи
![]()
Химические свойства
I – По карбоксильной группе
II – По галогену
III – По радикалу
I. Галогензамещенные кислоты являются более сильными кислотами по сравнению с предельными кислотами, особенно сильны -замещенные.
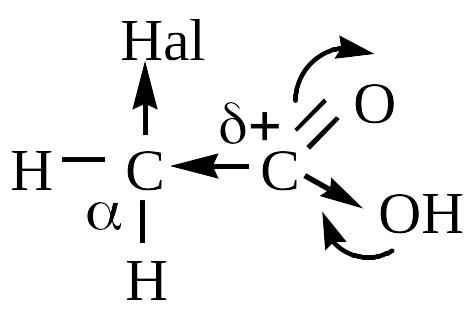 -углерод,
связанный с галогеном, особенно со
фтором, становится более электроположительным
и оттягивает на себя е-
-ную пару карбоксильного углерода.
-углерод,
связанный с галогеном, особенно со
фтором, становится более электроположительным
и оттягивает на себя е-
-ную пару карбоксильного углерода.
Влияние галогена затухает по мере удаления его от карбоксильной группы, уже при -замещении оно мало сказывается.
Галогензамещенные кислоты вступают во все реакции, свойственные карбоновых кислотам. Они образуют соли, сложные эфиры, галоидангидриды, ангидриды, амиды.
II. По галогену:
а) замещение галогена;
б) отщепление HHal
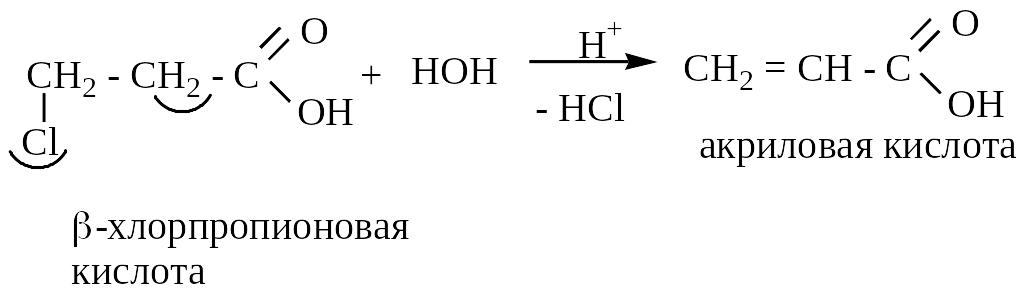
1. Гидролиз
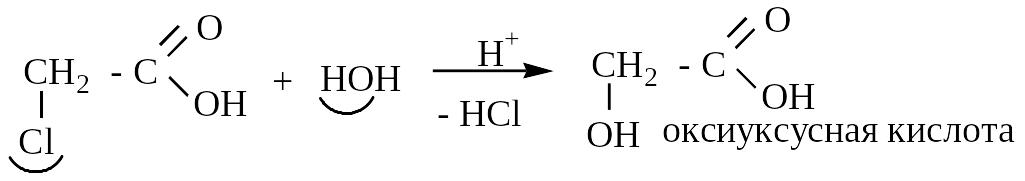 -замещенные
-замещенные
- замещенные
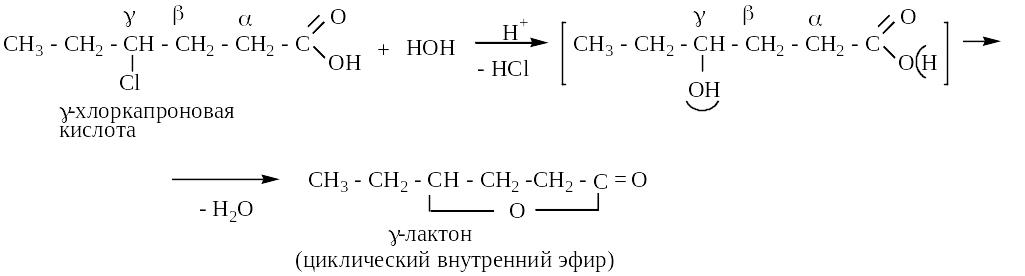 - замещенные
- замещенные
2. Действие алкоголятов
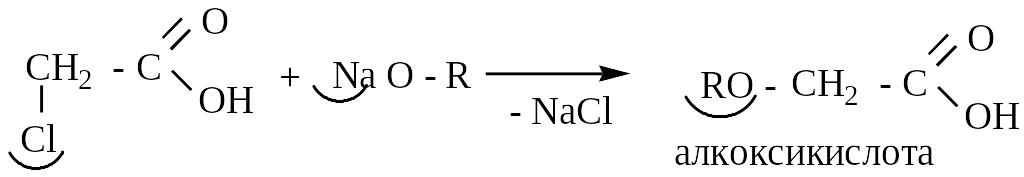

3. Действие KCN
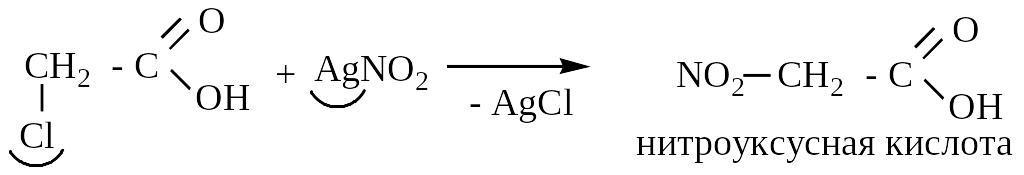
4. Действие AgNO2
III. По радикалу – свойства соответствующих классов УВ – предельных, непредельных…
