
- •2. Воспламенение
- •2.1. Адиабатические химические превращения
- •2.2. Два типа воспламенения
- •2.3. Стационарная теория теплового воспламенения
- •2.4. Нестационарная теория теплового взрыва
- •2.5. Тепловой взрыв в динамических условиях /4/
- •2.6. Вынужденное воспламенение (зажигание)
- •2.7. Тепловая теория зажигания
- •Процесс горения
- •Диффузионное и кинетическое горение
- •Диффузионное пламя
- •Расход воздуха на горение
- •После преобразования получим
- •Продукты сгорания. Дым
- •Определяем объем влажных продуктов сгорания метана
- •Теплота сгорания
- •Температура горения
- •Оценка пожарной опасности веществ и материалов
- •Превращение горючих веществ при нагревании
- •Теория окисления горючих веществ
- •Цепь Разветвление
- •Теория самовоспламенения
- •Температура самовоспламенения
- •Процесс возгорания и воспламенения
2.5. Тепловой взрыв в динамических условиях /4/
Рассмотренное случая соответствуют постоянству температуры стенки, равной начальной температуре смеси Тс = То=const. В работах А.Г. Мержанова с сотрудниками развита теория теплового взрыва в условиях линейного изменения To (нагрев и охлаждение), основанная на решении системы уравнений- (1.23)-(1.25), дополненных законом изменения температуры окружающей среда:
![]() :, (2.39)
:, (2.39)
где
![]() -
скорость изменения температуры.
-
скорость изменения температуры.
При
нагреве (при To<<T*,
где Т* - критическая температура
теплового взрыва в статических условиях)
система ведет себя
сначала как инертное вещество, и
температура в ней стационарно
запаздывает по сравнению с Тс.
В
дальнейшем начинает проявляться
тепловыделение от реакции, и запаздывание
исчезает,
а температура в системе обгоняет
температуру в окружающей среде.
Для реакции нулевого порядка тепловой
взрыв неизбежен, В реальных системах
из-за выгорания вещества существует
критическое значение скорости нагрева
![]() (при
(при
![]() )
реакция
протекает
спокойно с небольшим перегревом, при
)
реакция
протекает
спокойно с небольшим перегревом, при
![]() реакция завершается
тепловым взрывом). Вблизи
существует
область квазистационарного
протекания химической реакции,
характеризующиеся
большими глубинами предвзрывного
превращения вещества
реакция завершается
тепловым взрывом). Вблизи
существует
область квазистационарного
протекания химической реакции,
характеризующиеся
большими глубинами предвзрывного
превращения вещества
![]() к вырождением самого теплового взрыва
(рис.2.5).
к вырождением самого теплового взрыва
(рис.2.5).
В динамических режимах вместо То удобно использовать критическую температуру Т*. Основным параметром динамической задачи является отношение характерных времен изменения температуры и химической реакции U :
![]() (2.40)
(2.40)
и представляет собой по существу динамический аналог критериев Н.Н. Семенова и Д.А. Франк - Каменецкого.
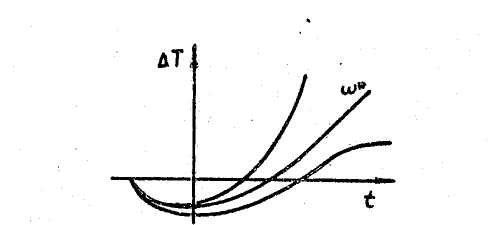
Рис. 2.5. Зависимость T ( Ts ) при различных значащих параметра U
2.6. Вынужденное воспламенение (зажигание)
Под вынужденным воспламенением (зажиганием) понимают случаи воспламенения, когда основная масса горючей среды остается холодной, а нагревание производится только в одном небольшом по объему участке среды, газа в частности. Это может быть осуществлено разнообразными способами: введением в среду накаленного тела, небольшим пламенем, электрической искрой того или иного тала и так далее. С точки зрения физической сущности процесса вынужденного зажигания, нет принципиальных отличий от процесса самовоспламенения, поскольку условия самоускорения реакций в данном случае также существенны, но их действие пространственно ограничивается лишь частью объема горючей смеси. С точки зрения расчета, явление это более сложно, чем самовоспламенение.
Видимым и практически удобным критерием зажигания является факт распространения пламени от местного источника воспламенения на весь объем среды. Поэтому факторы, определяющие критические условия в случае зажигания, должны быть связаны, с одной стороны, со свойствами источника зажигания и, с другой- с условиями распространения горения, распространения пламени.
Для
того, чтобы представить себе механизм
зажигания от накаленного тела, рассмотрим
высказанные в связи с этим соображения
В. Вант-Гоффа.. Процессом диффузии
пренебрегаем, считая,
что концентрация реагирующих веществ
везде одинакова и
равна начальной. Предположим, что на
поверхности тела произошло
повышение температуры до некоторой
величины Т1.
В сpeде
инертной, неспособной к реакции,
распределение температура изобразится
кривой T1А1
„
Для аналогичного процесса в
реакционноспособной
среде кривая температур должна быть
уже несколько
иной в силу дополнительного выделения
тепла реакция ,и ее можно
изобразить примерно в вида пунктирной
линии
![]() .
Повысим
теперь начальную температуру тела до
Т2,
.В инертной среде
это поведет к возникновению распределения
температуры Т2А2
подобного предыдущему с более резким
ее спадом. В реагирующей
среде; напротив; в силу увеличивающегося
с повышением
температуры выделения тепла, кривая
температур будет падать медленнее,
чем кривая
и можно
предвидеть, что найдется такая
температура Т2,
при которой понижение температуры, по
крайней мере вблизи источника, не
произойдет, и кривая температур
примет вид
.
Повысим
теперь начальную температуру тела до
Т2,
.В инертной среде
это поведет к возникновению распределения
температуры Т2А2
подобного предыдущему с более резким
ее спадом. В реагирующей
среде; напротив; в силу увеличивающегося
с повышением
температуры выделения тепла, кривая
температур будет падать медленнее,
чем кривая
и можно
предвидеть, что найдется такая
температура Т2,
при которой понижение температуры, по
крайней мере вблизи источника, не
произойдет, и кривая температур
примет вид
![]() .
Если после этого повысить начальную
температуру
источника, то стационарное состояние
станет невозможным,
так
как температура в окружающей среде
начнет прогрессивно
возрастать по мере удаления от источника
до тех пор, пока не произойдет воспламенения
(Т3-
.
Если после этого повысить начальную
температуру
источника, то стационарное состояние
станет невозможным,
так
как температура в окружающей среде
начнет прогрессивно
возрастать по мере удаления от источника
до тех пор, пока не произойдет воспламенения
(Т3-![]() -В)
(рис.2.6).
Температура
Т2
является
для этих условий критической предельной
температурой, т.е. температурой зажигания,
и по своему смыслу аналогична
температуре воспламенения в случае
процессов самовоспламенения.
-В)
(рис.2.6).
Температура
Т2
является
для этих условий критической предельной
температурой, т.е. температурой зажигания,
и по своему смыслу аналогична
температуре воспламенения в случае
процессов самовоспламенения.
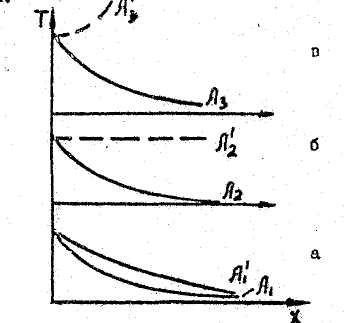
Рис. 2.5. Распределение температуры в процессе зажигания
