
- •1. Ресурсы поверхностных вод и запасы льдов
- •2. Ресурсы подземных вод.
- •3. Круговорот природных вод.
- •4. Строение молекулы воды. Структура воды.
- •5. Физические свойства воды и её аномалии
- •6. Понятие о системах фазах и компонентах.
- •7. Классификация природных вод.
- •8. Факторы формирования химического состава природных вод
- •I группа: факторы непосредственно воздействующие на воды (породы, почвы, живые организмы, деятельность человека)
- •1)Соли.
- •2) Изверженные и метаморфические породы
- •3) Глинистые породы
- •2. Почвы
- •3. Живые организмы
- •4. Деятельность человека
- •II группа: факторы, определяющие условия, в которых протекает взаимодействие вещества с водой (климат, рельеф, растительность, водный режим, взвешенные вещества, донные отложения)
- •1. Климат
- •2. Рельеф местности
- •3. Водный режим (или гидрологический режим)
- •4. Взвешенные веществ
- •Донные отложения ила
- •9. Процессы формирования химического состава природных вод
- •10. Процессы переводящие вещество в раствор.
- •11. Процессы, выводящие вещество из раствора.
- •12. Обменные процессы вещества.
- •13. Формирование ионного состава природных вод
- •5% Апатит Ca10r2(po4) (r-cl или f)
- •14 . Формрование биогенных веществ природных вод.
- •16. Формирование микроэлементного состава природных вод.
- •17. Формирование газового состава природных вод.
- •18. Влияние загрязненных веществ на химический состав прир. Вод.
- •19. Равновесные системы в природных водах.
- •21. Расчеты карбонатного равновесия для природных вод с минерализацией более 100 мг/дм3 с учетом активности ионов
- •22. Расчет концентраций отдельных форм производных угольной кислоты
- •23. Расчет степени насыщаемости природных вод СаСо3
- •24. Буферность карбонатных систем.
- •25. Сульфидное равновесие
- •26. Окислительно-восстановительные равновесия
- •27. Буферная способность почв
- •28. Кислотность почв
- •29. Миграция химических соединений
- •30 Виды миграции
- •31. Интенсивность миграции
11. Процессы, выводящие вещество из раствора.
Такими процессами являются осаждение, сорбция, соосаждение и кристаллизация солей. Удаление вещества из воды может происходить и из ненасыщенных растворов из-за процессов сорбции. Поэтому концентрации так называемых рассеянных элементов в природных водах значительно ниже расчетной концентрации. В процессах сорбции большую роль играет адсорбция. Этот процесс является важнейшим механизмом перевода многих элементов из раствора в твердую фазу. Различают аДсорбцию, когда растворенный ион или молекула присоединяются к поверхности существовавшей твердой фазы и аБсорбцию, когда поглощение осуществляется всей массой. К хорошим сорбентам относятся глины, органическое вещество, входящее в состав горных пород, почв, донных отложений, а также коллоидные формы кремнезема, гидроксиды Mn, Fe. Al. Сорбция может быть полярной и неполярной.
Полярная сорбция. Отрицательно заряженные сорбенты (глины, орг.вещество) поглощают из воды катионы, а положительно заряженные (гидроксиды Al, Mn, Fe) – анионы. Полярная сорбция обычно носит обменный характер. Разновидность полярной сорбции – ионный обмен. Но обменное поглощение почти всегда сопровождается необменным, при котором часть ионов закрепляется на сорбенте. В почвах необменного К и Mn всегда больше чем Са.
Неполярная сорбция заключается в поглощении из р-ров молекул в-ва.(глины и почвы поглощают газы и водяные пары).
Адсорбция таких металлов как Al, Fe, Mn очень сильно зависит от рН среды. Такая адсорбция становится значительной в интервале значений рН, которые соответствуют гидролизу поглощаемого металла. Гидроксиды Mn, Fe являются тонкозернистыми, имеют большую удельную поверхность (порядка 200 м2/гр). Поэтому гидроксиды Mn хар-ся высокой адсорбционной емкостью и высоким сродством к тяжелым металлам. Но процесс поглощения на оксидах и гидроксидах Mn нельзя рассматривать как простую адсорбцию. Такое поглощение включает фазовые переходы оксидов Mn и каталитические окисл-восстановительные реакции. Там где концентрация рассеянных элементов контролируется адсорбцией можно ожидать, что концентрация растворенных веществ зависит от значений Eh и рН. Если оксиды растворяются из-за восстановления, то все адсорбированные металлы высвобождаются.
-
Сорбцию загрязняющих веществ почвой описывают уравнением Ленгмюра.
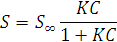
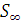 - максимальная предельная сорбция.
Она характеризует поверхность
адсорбента.
- максимальная предельная сорбция.
Она характеризует поверхность
адсорбента.К – пок-ль способности в-ва сорбироваться. Это отношение скоростей процессов сорбции и десорбции вещества.
С – равновесная концентрация.
S - количество сорбированного вещества.
Значение количеств. показателей сорбции загрязняющих в-в позволяет прогнозировать уровень их конц-ии в почв.р-ре, прочность связи с тв. фазами и позволяет оценивать макс. сорбционную способность почв в отношении этих в-в и способность загрязняющих в-в к миграции.
Соосаждение – вкл-е растворенных эл-тов в кач-ве второстеп. комп-тов в тв.фазу в момент ее осаждения. В прир.сист.вкл-щих MnOH2,FeOH2,часто нельзя различить адсорбцию и соосаждение.
Кристаллизация солей из воды способствует изменению геохимической обстановки за счет чего концентрации ионов солей достигают ПР. к таким изменениям геохимической обстановки относятся концентрирование, выделение газов, сдвиг термодинамического, кислотно-щелочного и окислительно-восстановительного равновесия, а также смешения водных масс различного состава. При испарении или вымораживании океанических, морских, озерных и других видов вод происходит концентрирование, приводящее к выпадению солей. С увеличением концентрации выпадение солей происходит в следующей последовательности: 1)Карбонатные соли; 2)Сульфидные соли; 3)Хлоридные соли. Выпадение карбонатов большей частью связано с дегазацией природных вод, изменением T, увеличением степени испарения. Общий эффект испарения состоит в удалении из р-ра чистой воды, поэтому конц-ии всех растворенных компонентов при испарении возрастает. Испарение происходит во всех климатических зонах, но в теплых засушливых зонах (аридные зоны) испарение - главный процесс, контролирующий состав природной воды. Кристаллизация солей в процессе концентрирования природных вод аридной зоны сопровождается выпадением карбонатов, сульфатов, хлоридов Ca, Mg, Na. Что приводит к образованию солончаков.
