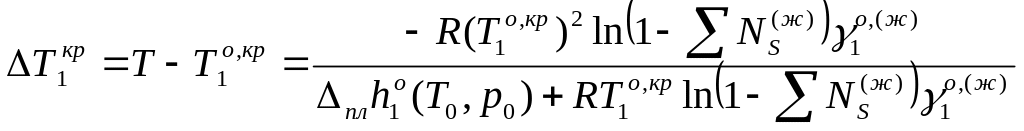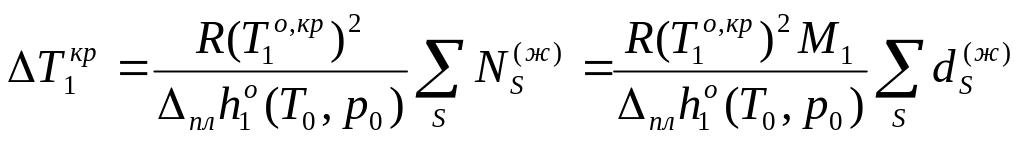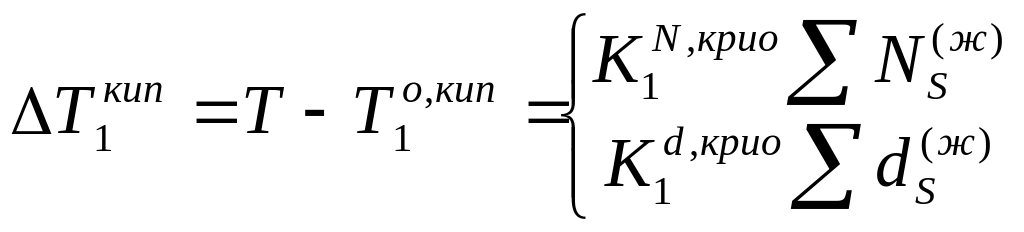- •Модуль 5.
- •Тема 10. Смещения равновесий двух фаз в многокомпонентных системах.
- •10.1. Изобарическое смещение равновесия жидкость-пар.
- •10.1.1. Общий случай равновесия: каждый компонент присутствует в каждой фазе.
- •10.1.2. Частный случай равновесия: раствор. В-ва ж. Фазы отсутствует в п. Фазе из-за
- •10.2. Изотермическое смещение равновесия жидкость-пар.
- •10.2.1. Общий случай равновесия: каждый компонент присутствует в каждой фазе.
- •10.2.2. Частный случай равновесия: раствор. В-ва ж. Фазы отсутствует в п. Фазе из-за
- •10.3. Изобарическое смещение равновесия твёрдое – жидкость.
- •10.3.1. Общий случай: каждый компонент присутствует в каждой фазе.
- •10.3.2. Частный случай равновесия: т. Фаза содержит лишь чистый компонент k.
10.3. Изобарическое смещение равновесия твёрдое – жидкость.
10.3.1. Общий случай: каждый компонент присутствует в каждой фазе.
1. Особенности системы: |
||
1) 2)
|
3
плавление кристаллизация
компонента k 4)NЗСФР = К(ж, п) (А-1) = К(2-1) = К. |
|
2. Дифф. форма ЗСФР |
||
Аналит. выражение
Исследование:
–
возр. нелин. ф.,
т.к.
|
Граф. образ функции
В
озможные
расчёты: определение
|
|
3. Интегр. форма ЗСФР |
||
Аналит. выражение
Приближение:
Исследование: – убыв. лин. ф. |
Граф. образ функции
В озможные расчёты: 1)
Определение
или
2)
Определение
или
3) Определение Т по остальным; 4)
Определение
|
|
10.3.2. Частный случай равновесия: т. Фаза содержит лишь чистый компонент k.
1. Особенности системы: |
||||
k(т)
и k(ж) k(ж) 1) = , k и k Є {k}
* 2)
|
3
плавление кристаллизация
компонента k 4)NЗСФР = К(ж, п) (А-1) = 1(2-1) = 1. |
|||
2. Дифф. форма ЗСФР для компонента k’. |
||||
Аналит. выражение:
Исследование
т.к.
|
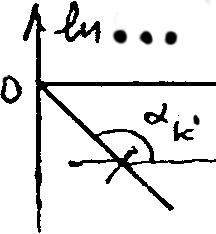
Граф. образ
функции
Возможные
расчёты: определение |
|||
3. Интегр. форма ЗСФР для компонента k’. |
||||
Аналит. выражение:
Приближение:
Исследование
|
Граф. образ
функции
Возможные расчёты: 1)
Определение
2)
Определение
3) Определение Т по остальным; 4)
Определение
|
|||
4. Уравнение Шредера и правила растворимости Гильдебранда. |
||||
Если ж. фаза
близка к сов. р-ру (
Исследование Правила растворимости Гильдебранда: 1)
2)
чем меньше
3)
чем меньше
|
Граф. образы
функции
Возможные расчёты: 1)
Определение
2) Определение Т по остальным; 3) Определение по tg αk графически. |
|||
5. Понижение температуры кристаллизации компонента k. |
||||
А налит. выражение: Пусть k=1 – растворитель ж. фазы. Тогда по п.3 имеем:
1) ; 2) Решение относительно Т
Исследование – убыв. нелин. ф-я.
|
Граф. образ функции
В озможные расчёты: 1) Определение по остальным; 2)
Определение
3) Определение Т по остальным; 4)
Определение
|
|||
6. Линейные законы понижения температуры кристаллизации растворителя ж. фазы |
||||
Ф
ормирование
I ) ж. фаза – разбавленный раствор ( ): 1)
2)
3) II ) ж. фаза – идеал. Раствор в узком понимании: =1
1)
2)
– линейные
законы повышения т-ры кипения р-ля ж.
фазы в N-
и d-шкалах:
Граф. образы
лин. законов:
Ns(ж)
или
ds(ж) Возможные расчёты: 1) Определение по остальным; 2) Определение по остальным; 3) Определение по остальным. |
||||




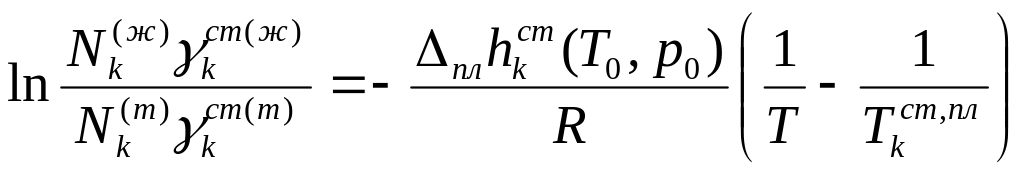

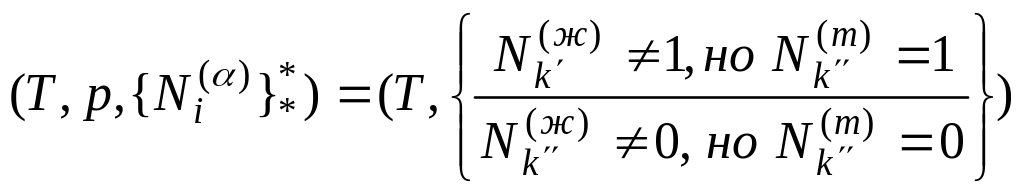 ,
p= const
,
p= const
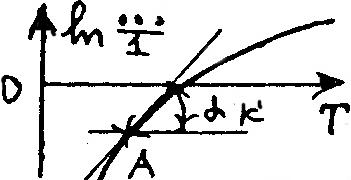
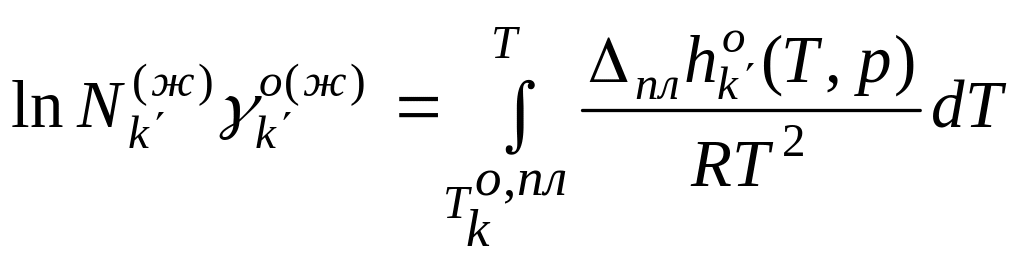

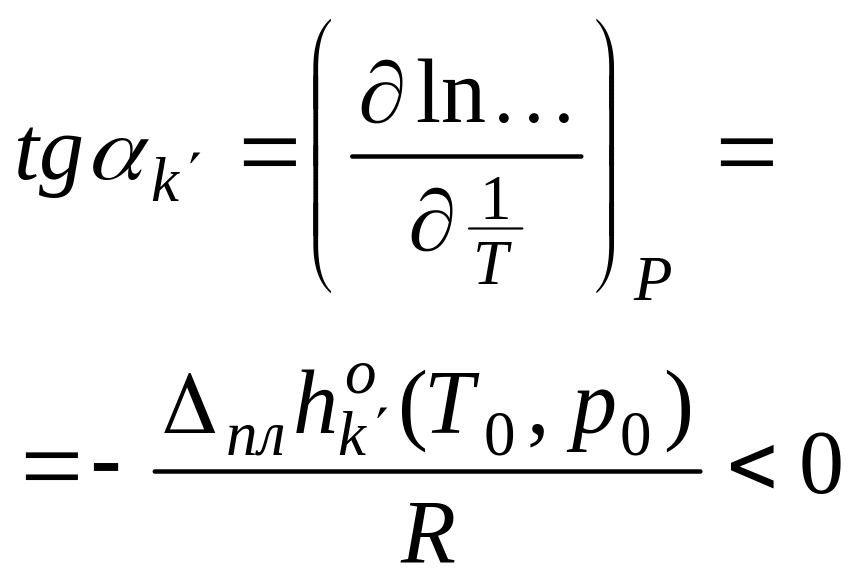

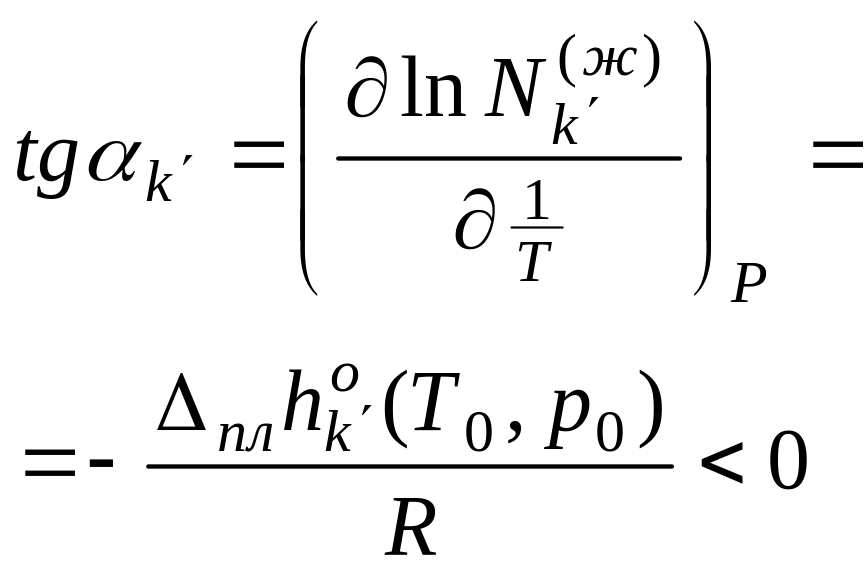



 изменение
т-ры кристаллизации растворителя ж.
фазы из-за присутствия в ней нелетучих
раствор. веществ s.
изменение
т-ры кристаллизации растворителя ж.
фазы из-за присутствия в ней нелетучих
раствор. веществ s.