
- •Глава 6. Твердые тела
- •6.1. Аморфное и кристаллическое состояние вещества
- •6.2. Классификация кристаллов по типу молекул, составляющих кристалл
- •6.3. Анизотропия кристаллов
- •6.4. Кристаллические решетки Браве
- •6.5. Потенциальная энергия взаимодействия ионных кристаллов
- •6.6. Плавление, кристаллизация и возгонка твердых тел
- •6.7. Теплоемкость кристаллов
- •Приложение а основные понятия теории вероятностей
- •1. Понятие вероятности события
- •2. Простейшие теоремы теории вероятностей
- •3. Интегральная функция распределения случайной величины
- •4. Плотность вероятности
- •5. Среднее значение
- •6. Свойства среднего значения
- •7. Дисперсия и ее свойства
- •8. Неравенство Чебышева
- •9. Теорема Чебышева
- •10. Теорема Бернулли
- •11. Плотность вероятности ординат монотонной функции случайного аргумента
- •Приложение b интегралы, встречающиеся при применениях распределения максвелла.
6.5. Потенциальная энергия взаимодействия ионных кристаллов
Будем рассматривать
ионы в кристалле как недеформируемые
шары с зарядами
![]() и
и
![]() ,
где z1 и z2
-
зарядности ионов, e -
величина заряда электрона. К примеру,
для ионного кристалла
,
где z1 и z2
-
зарядности ионов, e -
величина заряда электрона. К примеру,
для ионного кристалла
![]() зарядности
зарядности
![]() ,
а для кристалла
,
а для кристалла
![]() зарядности
зарядности
![]()
Сила притяжения ионов определяется законом Кулона
 .
(6.5.1)
.
(6.5.1)
Потенциальная энергия притяжения двух ионов разного знака, согласно формуле (15) введения
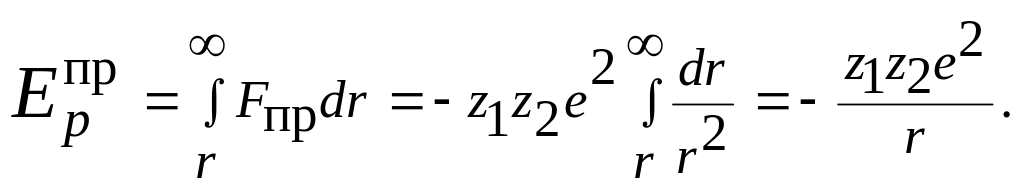 (6.5.2)
(6.5.2)
Потенциальную энергию отталкивания, обусловленную взаимодействием электронных оболочек ионов, как мы знаем, можно представить в виде:
![]() , (6.5.3)
, (6.5.3)
где
![]() ,
а величина n (коэффициент
борновского отталкивания) значительно
больше единицы, так как силы отталкивания
быстро падают с расстоянием. Силу
отталкивания
,
а величина n (коэффициент
борновского отталкивания) значительно
больше единицы, так как силы отталкивания
быстро падают с расстоянием. Силу
отталкивания
![]() найдем, воспользовавшись формулой
(B.14):
найдем, воспользовавшись формулой
(B.14):
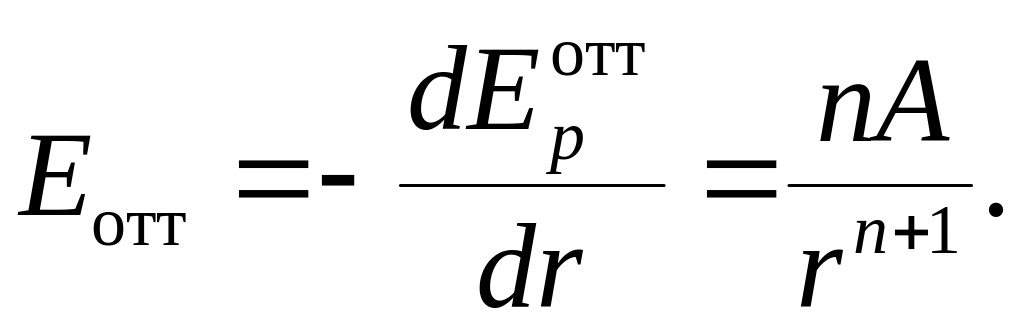 (6.5.4)
(6.5.4)
На равновесном расстоянии r0 сила притяжения равна силе отталкивания, т. е.
 .
(6.5.5)
.
(6.5.5)
Откуда определяем постоянную A:
![]() ,
(6.5.6)
,
(6.5.6)
Из выражений (6.5.6) и (6.5.3) при r = r0 получим
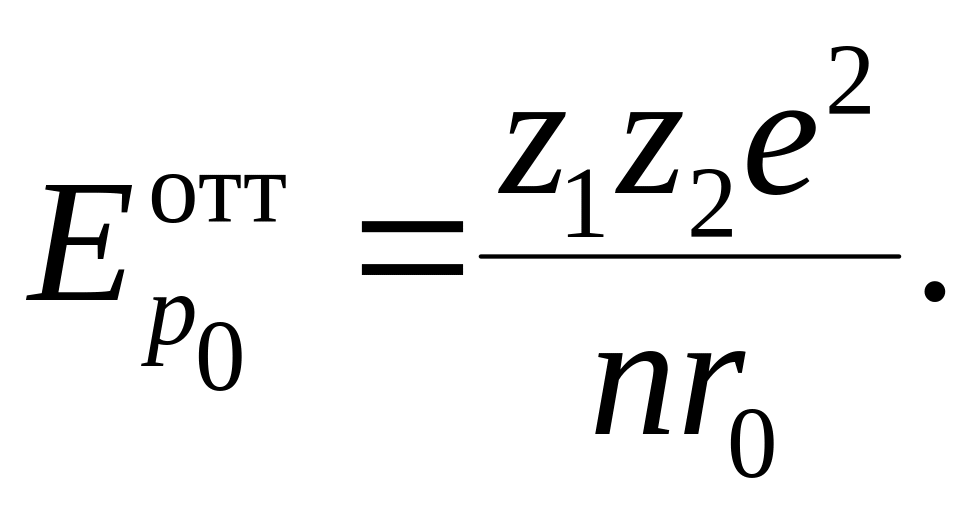 (6.5.7)
(6.5.7)
Полная энергия взаимодействия двух ионов (ионной молекулы)
![]() . (6.5.8)
. (6.5.8)
Из последнего выражения при r = r0 получаем известную формулу Борна, которая дает величину минимальной потенциальной энергии взаимодействия ионной молекулы:
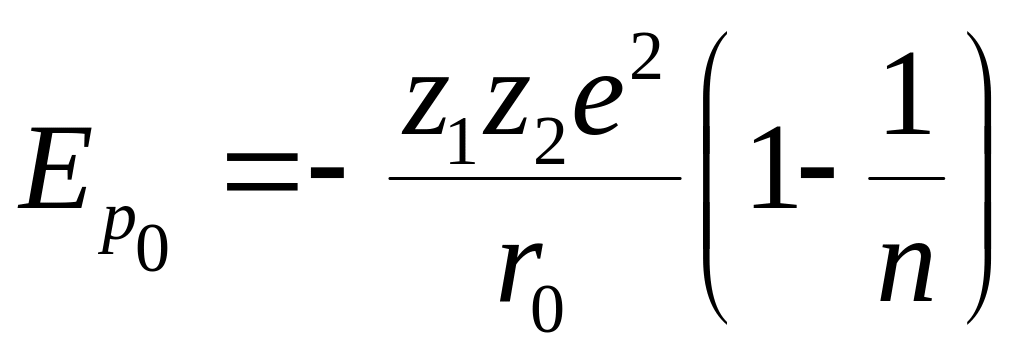 . (6.5.9)
. (6.5.9)
Чтобы вычислить потенциальную энергию взаимодействия кристалла, нужно учесть, что каждый ион взаимодействует не с одним ионом противоположного знака, а с достаточно большим количеством положительных и отрицательных ионов, находящихся на различных расстояниях от рассматриваемого иона. Поясним метод вычисления указанной энергии кристалла на примере ионного кристалла NaCl. Рассмотрим ион натрия, расположенный в центре рис. 83, б. Этот ион имеет своими ближайшими соседями 6 ионов хлора, находящихся на расстоянии r. Суммарная энергия кулоновского взаимодействия с этими ионами будет, согласно формуле (6.5.1),
![]() (6.5.10)
(6.5.10)
Так как структура
решетки NaCl кубическая,
то на расстоянии
![]() от рассматриваемого иона находится еще
12 ионов натрия, суммарная энергия
взаимодействия с которыми,
от рассматриваемого иона находится еще
12 ионов натрия, суммарная энергия
взаимодействия с которыми,
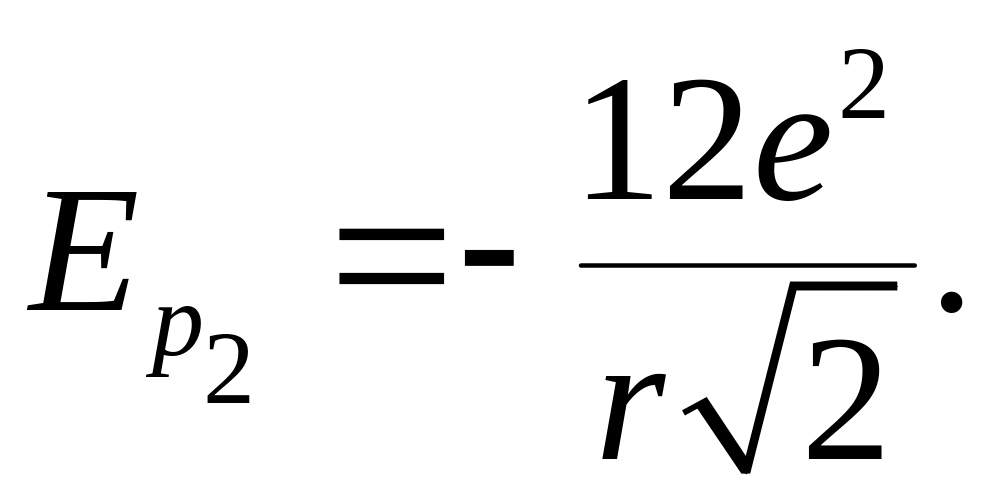 (6.5.11)
(6.5.11)
Далее на расстоянии
![]() от рассматриваемого иона располагаются
восемь ионов хлора, вклад которых в
энергию взаимодействия составит
от рассматриваемого иона располагаются
восемь ионов хлора, вклад которых в
энергию взаимодействия составит
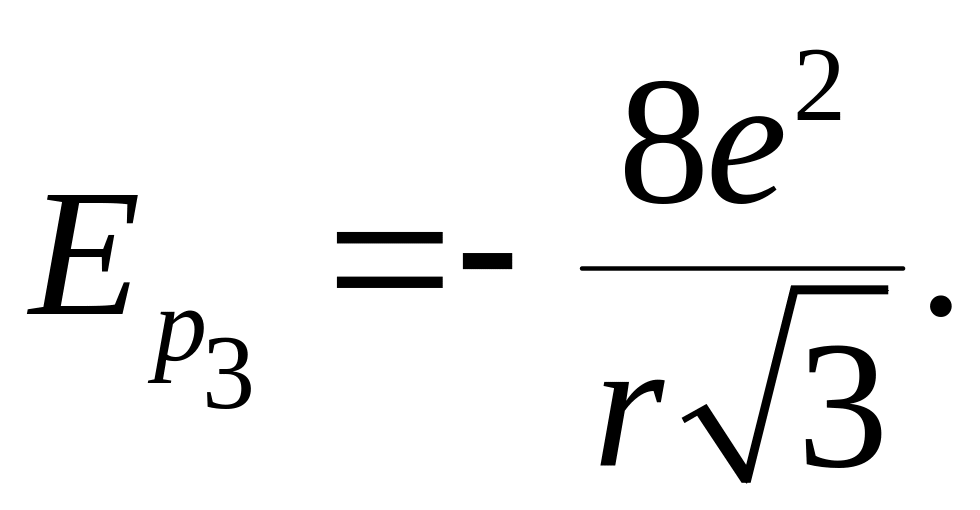 (6.5.12)
(6.5.12)
Этот процесс вычисления все меньших вкладов в энергию взаимодействия нетрудно продолжить. В результате суммарная энергия взаимодействия выделенного иона с остальными в решетке
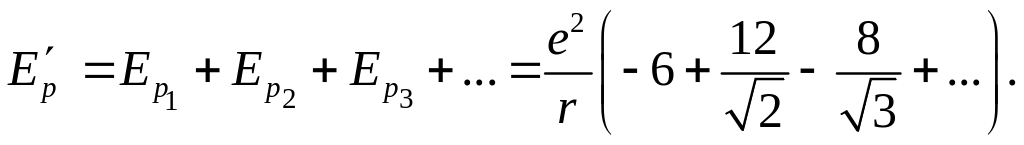
Можно доказать, что данный знакопеременный ряд является сходящимся и его сумма равна
![]() (6.5.13)
(6.5.13)
Коэффициент a = 1,7475 называют постоянной Маделунга, которая определяется величиной взаимодействия выделенного иона с ближайшими соседями в решетке. Следовательно, с учетом этого взаимодействия потенциальная энергия одного моля частиц кристалла должна быть записана в виде (см. 6. 5. 8):
![]() (6.5.14)
(6.5.14)
Коэффициент Маделунга a для других кристаллов вычисляется так же, как мы это сделаем для кристалла NaCl.
Коэффициент борновского отталкивания n, входящий в выражение (6.5.14), может быть найден из экспериментальных данных по изотермической сжимаемости кристаллов:
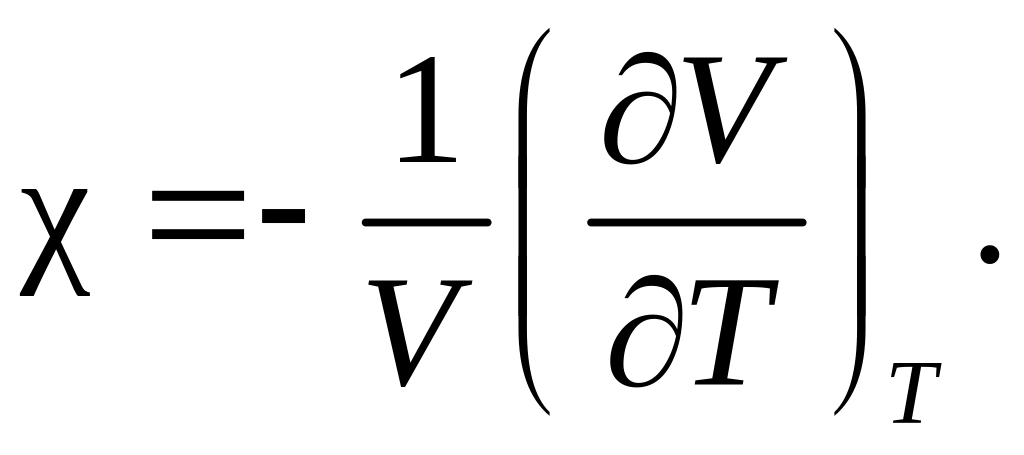 (6.5.15)
(6.5.15)
Как мы знаем, при абсолютном нуле температуры, когда отсутствует тепловое движение частиц кристалла, энтропия постоянна. Поэтому из основного уравнения термодинамики (2.14.3)
![]() (6.5.16)
(6.5.16)
находим ![]() (6.5.17)
(6.5.17)
Поскольку внутренняя энергия кристалла
![]()
то ![]() ,
(6.5.18)
,
(6.5.18)
так как при
отсутствии теплового движения частиц
![]()
Подставляя (6.5.18) в (6.5.17) и затем дифференцируя, получим
![]() (6.5.19)
(6.5.19)
При сжатии кристалла происходит сближение ионов, уменьшается r, входящее в уравнение (6.5.14). Очевидно, объем моля кристалла пропорционален кубу межионного расстояния r, т. е.
![]() (6.5.20)
(6.5.20)
Коэффициент
пропорциональности нетрудно найти из
геометрических соотношений, если
известен тип структуры кристалла. Для
кристаллов типа NaCl
![]() ,
где NA
число
Авогадро.
,
где NA
число
Авогадро.
Используя соотношения (6.5.1415) и (6.5.196.5.20), можно получить выражение для нахождения коэффициента борновского отталкивания n для кристаллов типа NaCl:
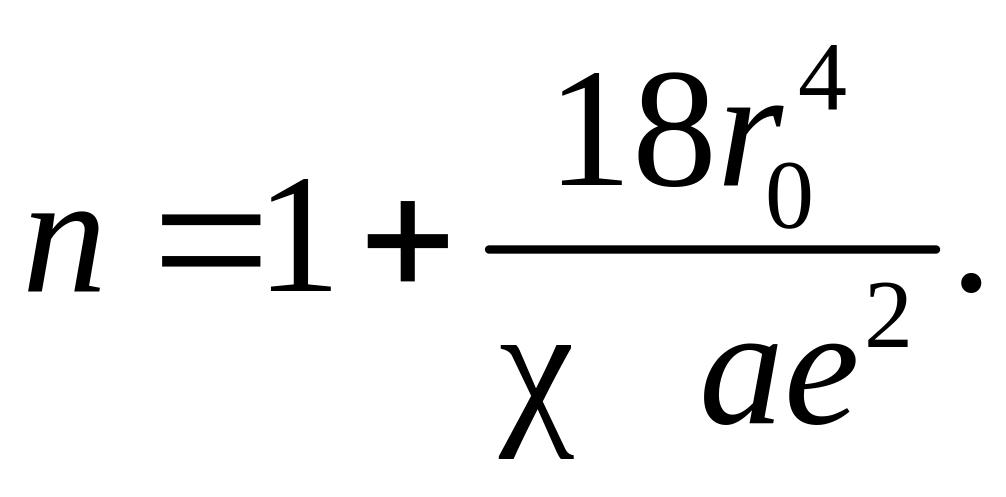 (6.5.21)
(6.5.21)
Отсюда можно вычислить n, если известны , r0 и коэффициент Маделунга a.
Ниже приведены значения n, соответствующие коэффициентам сжимаемости , полученным экспериментально для некоторых кристаллов (табл. 6.5.1).
Таблица 6.5.1
Кристалл |
LiF |
LiCl |
NaCl |
NaBr |
n |
5,9 |
8,0 |
9,1 |
9,5 |
