
Вопрос №33
Биосинтез мочевины. Связь орнитинового цикла с превращениями фумаровой и аспарагиновой кислот. Происхождение атомов азота мочевины.
Мочевина является главным конечным продуктом обмена аминокислот. Синтезируется мочевина из аммиака, который постоянно образуется в организме при окислительном и неокислительном дезаминировании аминокислот, при гидролизе амидов глутаминовой и аспарагиновой кислот, а также при распаде пуриновых и пиримидиновых нуклеотидов.
Процесс синтеза мочевины получил название "орнитиновый цикл", или "цикл Кребса-Гензелейта".
М![]() очевина
(карбамид) - полный амид угольной кислоты
- содержит 2 атома азота. Источником
одного из
них является аммиак, который
в печени связывается с диоксидом углерода
с образованием карбамоилфосфата
под действием карбамоилфосфатсинтетазы
I.
очевина
(карбамид) - полный амид угольной кислоты
- содержит 2 атома азота. Источником
одного из
них является аммиак, который
в печени связывается с диоксидом углерода
с образованием карбамоилфосфата
под действием карбамоилфосфатсинтетазы
I.

Далее под действием орнитинкарбамоилтрансферазы карбамоильная группа карбамоилфосфата переносится на α-аминокислоту орнитин, и образуется другая α-аминокислота - цитруллин
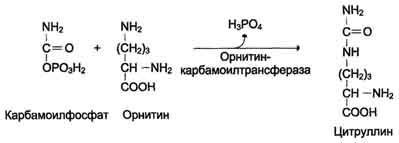
В следующей реакции аргининосукцинатсинтетаза связывает цитруллин с аспартатом и образует аргининосукцинат (аргининоянтарную кислоту). Этот фермент нуждается в ионах Mg2+. В реакции затрачивается 1 моль АТФ, но используется энергия двух макроэргических связей. Аспартат - источник второго атома азота мочевины
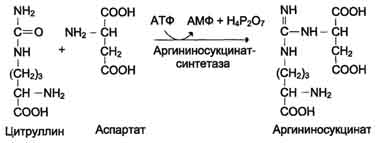
Далее фермент аргининосукцинатлиаза (аргининосукциназа) расщепляет аргининосукцинат на аргинин и фумарат, при этом аминогруппа аспартата оказывается в молекуле аргинина
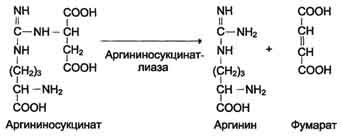
Аргинин подвергается гидролизу под действием аргиназы, при этом образуются орнитин и мочевина. Кофакторами аргиназы являются ионы Са2+ или Мn2+. Высокие концентрации орнитина и лизина, являющихся структурными аналогами аргинина, подавляют активность этого фермента:
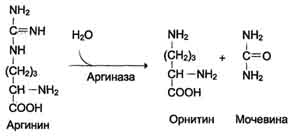
Образующийся орнитин взаимодействует с новой молекулой карбамоилфосфата, и цикл замыкается.
Первые две реакции процесса происходят в митохондриях гепатоцитов. Затем цитруллин, являющийся продуктом этих реакций, транспортируется в цитозоль, где и осуществляются дальнейшие превращения.
Вопрос №34
Нарушение синтеза и выделения мочевины. Гипераммониемия.
Нарушение реакций обезвреживания аммиака может вызвать повышение содержания аммиака в крови - гипераммониемию, что оказывает токсическое действие на организм. Причинами гипераммониемии могут выступать как генетический дефект ферментов орнитинового цикла в печени, так и вторичное поражение печени в результате цирроза, гепатита и других заболеваний.
Нарушение орнитинового цикла наблюдается при гепатитах различной этиологии и некоторых других вирусных заболеваниях. Например, установлено, что вирусы гриппа и других острых респираторных вирусных инфекций снижают активность карбамоилфосфатсинтетазы I. При циррозе и других заболеваниях печени также часто наблюдают гипераммониемию.
Снижение активности какого-либо фермента синтеза мочевины приводит к накоплению в крови субстрата данного фермента и его предшественников. Так, при дефекте аргининосук-цинатсинтетазы повышается содержание цитруллина (цитруллинемия); при дефекте аргиназы - концентрация аргинина, аргининосукцината, цитруллина и т.д. При гипераммониемиях I и II типа вследствие дефекта орнитинкарбамоилтрансферазы происходит накопление карбамоилфосфата в митохондриях и выход его в цитозоль. Это вызывает увеличение скорости синтеза пиримидиновых нуклеотидов (вследствие активации карбамоилфосфатсинтетазы II), что приводит к накоплению оротата, уридина и урацила и выведению их с мочой. Содержание всех метаболитов повышается, и состояние больных ухудшается при увеличении количества белков в пище. Тяжесть течения заболевания зависит также от степени снижения активности ферментов.
Все нарушения орнитинового цикла приводят к значительному повышению в крови концентрации аммиака, глутамина и аланина.
Гипераммониемия сопровождается появлением следующих симптомов:
тошнота, повторяющаяся рвота;
головокружение, судороги;
потеря сознания, отёк мозга (в тяжёлых случаях);
отставание умственного развития (при хронической врождённой форме).
Таблица 9-4. Наследственные нарушения орнитинового цикла и основные их проявления
Заболевание |
Дефект фермента |
Тип наследования |
Клинические проявления |
Метаболиты |
|
кровь |
моча |
||||
Гиперам- мониемия, тип I |
Карбамоил- фосфат- синтетаза I |
Аутосомно- рецессивный |
В течение 24-48 ч после рождения кома, смерть |
Глн Ала NH3 |
Оротат |
Гиперам- мониемия, тип II |
Орнитин- карбамоил- трансфераза |
Сцепленный с Х-хромосомой |
Гипотония, снижение толерантности к белкам |
Глн Ала NH3 |
Оротат |
Цитрул- линемия |
Аргинино- сукцинат- синтетаза |
Аутосомно- рецессивный |
Гипераммониемия тяжёлая у новорождённых. У взрослых - после белковой нагрузки |
Цитруллин NH3 |
Цитруллин |
Аргинино- сукцина- турия |
Аргинино- сукцинат- лиаза |
Аутосомно-рецессивный |
Гипераммонимия, атаксия, судороги, выпадение волос |
Аргини- носукцинат NH3 |
Аргини- носукци- нат, Глн, Ала, Лиз |
Гиперар- гининемия |
Аргиназа |
Аутосомно-рецессивный |
Гипераргининемия |
Apr NH3 |
Apr Лиз Орнитин |
Все симптомы гипераммониемии - проявление действия аммиака на ЦНС (см. выше подраздел IV, Б).
Для диагностики различных типов гипераммониемии производят определение содержания аммиака в крови, метаболитов орнитинового цикла в крови и моче, акгивности фермента в биоптатах печени.
Основной диагностический признак - повышение концентрации аммиака в крови. Содержание аммиака в крови может достигать 6000 мкмоль/л (в норме - 60 мкмоль/л). Однако в большинстве хронических случаев уровень аммиака может повышаться только после белковой нагрузки или в течение острых осложнённых заболеваний.
Лечение больных с различными дефектами орнитинового цикла в основном направлено на снижение концентрации аммиака в крови за счёт малобелковой диеты, введения кетоаналогов аминокислот в рацион и стимуляцию выведения аммиака в обход нарушенных реакций:
путём связывания и выведения NH3 в составе фенилацетилглутамина и гишгуровой кислоты;
повышением концентрации промежуточных метаболитов цикла (аргинина, цитруллина, глутамата), образующихся вне блокируемых реакций.
Вводимый больным с дефектом карбамоил-фосфатсинтетазы I в качестве пищевой добавки фенилацетат в результате его конъюгации с глутамином образует фенилацетилглутамин, который экскретируется почками. Состояние больных при этом улучшается, так как происходит активация синтеза глутамина и снижение концентрации аммиака в крови.
Аналогичное действие оказывает введение бензоата, который связывает молекулу глицина. Образующаяся пшпуровая кислота выводится с мочой. В составе гиппурата происходит выделение азота из организма. Недостаток глицина компенсируется либо путём синтеза его из серина, либо за счёт образования из NH3 и СО2 в реакции, катализируемой глицинсинтетазой. При этом образование глицина сопровождается связыванием одной молекулы аммиака.
При гипераммониемии II типа (дефект орнитинкарбамоилтрансферазы) введение больших доз цитруллина стимулирует синтез мочевины из аспартата (рис. 9-19, В), что также приводит к вьшедению азота из организма. Введение больших доз аргинина при аргининосукцинатурии (дефект аргининосукцинатлиазы) стимулирует регенерацию орнитина и выведение азота в составе цитруллина и аргининосукцината.
Вопрос №35
Витамины. Классификация. Номенклатура.
Классификация.
Водорастворимые: В1(тиамин, антиневритный), В2(рибофлавин, витамин роста), РР(В3, ниацин, никотиновая кислота, никотинамид, антипеллагрический), В5(пантотеновая кислота), В6(пиридоксин, пиридоксаль, антидерматитный), В9(Вс, фолиевая кислота, витамин роста), В12(кобаламин, антинемический), Н(биотин, антисеборейный), С(аскорбиновая кислота, антицинготный).
Жирорастворимые: А(ретинол, антиксерофтальмический), D(кальциферол, антирахитический), К(нафтохиноны, антигеморрагический), Е(токоферол, антистерильный).
Также выделяют витаминоподобные вещества:
жирорастворимые – Q (убихинон),
водорастворимые – B4 (холин), P (биофлавоноиды), Bт (карнитин), B8 (инозит), U (S-метилметионин), N (липоевая кислота), B13 (оротовая кислота), B15 (пангамовая кислота).
Вопрос №36
Гипер-, гипо-, авитаминозы. Причины.
Гиповитаминозы
Нехватка витаминов ведет к развитию патологических процессов в виде специфическихгиповитаминозов или авитаминозов.
Широко распространенные скрытые формы витаминной недостаточности не имеют ярко выраженных внешних проявлений и симптомов, но оказывают отрицательное влияние на работоспособность, общий тонус организма и его устойчивость к разным неблагоприятным факторам. Витамины проявляются не наличием, а отсутствием!
Гипервитаминозы
Жирорастворимые витамины при увеличении дозы накапливаются и могут вызывать гипервитаминозы с рядом общих симптомов (потеря аппетита, расстройство ЖКТ, сильные головные боли, повышенная возбудимость нервной системы, выпадение волос, шелушение кожи) и со специфическими признаками. Яркая картина гипервитаминозов отмечается только для витаминов А и D.
Гиповитаминозы
Причины нехватки витаминов могут быть экзогенными (внешние факторы) и эндогенными(состояние организма):
Экзогенные гиповитаминозы:
гельминтозы, лямблиозы, дизентерия,
дисбактериоз кишечника,
нерациональное питание, т.е. недостаточное потребление с пищей.
Эндогенные гиповитаминозы:
нарушение всасывания (энтероколиты, гастроэнтериты различного происхождения). Например, пернициозная анемия Аддисон-Бирнера при В12-зависимой макроцитарной анемии,
заболевания печени, дискинезия желчного пузыря (для жирорастворимых витаминов),
повышенная потребность (беременность, лактация, физические нагрузки),
генетические дефекты кофермент-образующих ферментов.
Провитамины
Некоторые витамины поступают в организм в виде провитаминов. В организме провитамины превращаются в активные формы, например:
каротиноиды превращаются в витамин А,
пищевой эргостерол или 7-дегидрохолестерол под действием ультрафиолетовых лучей превращаются соответственно в эргокальциферол (D2) и холекальциферол (витамин D3).
Авитамино́з — заболевание, являющееся следствием длительного неполноценного питания, в котором отсутствуют какие-либо витамины.
Признаки авитаминоза
шелушение кожного покрова.
ломкость ногтей.
выпадение волос.
нежелание работать.
Впоследствии авитаминоз может привести к гораздо более плохим последствиям: проблемам с желудочно-кишечным трактом, ухудшению зрения.
Причины, вызывающие авитаминоз
Нарушение поступления витаминов с пищей при неправильном питании, недостаточном или некачественном питании.
Нарушение процессов пищеварения или нарушение работы органов, связанных непосредственно с пищеварением.
Поступление в организм антивитаминов, например лекарственных препаратов синкумар, дикумарол, применяющихся при лечении повышенной свертываемости крови.
Особенности детского обмена веществ
Особенности обмена веществ у пожилых людей
Некоторые заболевания:
цинга — при отсутствии витамина С
бери-бери — Витамин B1
рахит — Витамин D
пеллагра — Витамин PP
Часто встречается полиавитаминоз, одновременная недостаточность нескольких витаминов.
Вопрос №37 Антивитамины
Вещества, которые замещают витаминные коферменты в биохимических реакциях, или препятствуют синтезу кофермента или еще каким-либо образом препятствуют действию витамина, получили название антивитамины, например:
дикумарол (антивитамин К) – препятствует образованию активной формы витамина К, что блокирует синтез факторов свертывания крови,
изониазид (антивитамин РР) – образует "неправильные" коферменты, аналогичные НАД и НАДФ, что блокирует протекание окислительно-восстановительных реакций,
птеридины (антифолаты) – вытесняют витамин В9 из реакций и препятствуют синтезу пуриновых и пиримидиновых оснований и, как следствие, нуклеиновых кислот,
авидин (антивитамин Н) – связывается с витамином в кишечнике и не допускает его всасывания в кровь.
Вопрос №40
Классификация минеральных веществ по В.И. Вернандскому:
1. Макроэлементы. Это элементы, содержание которых в организме выше 10-2 %. К ним относятся кислород, углерод, водород, азот, кальций, фосфор, калий, натрий, магний, сера и хлор.
2. Микроэлементы. Это элементы, содержание которых в организме находится в пределах от 10-3 до 10-5 %. К ним относятся железо, марганец, йод, цинк, кремний, медь, селен, бор, молибден, фтор, хром, кобальт, ванадий, германий.
3. Ультрамикроэлементы. Это элементы, содержание которых в организме ниже 10-5 %. К ним относятся алюминий, никель, олово, литий, свинец, бром, ртуть, мышьяк, кадмий, серебро, золото.
В настоящее время ультрамикроэлементы объединяют с микроэлементами в одну группу. В табл. 3.2 приведены уточнённые данные по содержанию химических элементов в организме человека. Однако эта классификация отражает только содержание элементов в живых организмах, но не указывает на биологическую роль и физиологическое значение того или иного элемента.
Макроэлементы сконцентрированы, как правило, в одном типе тканей живого организма (соединительные ткани, мышцы, кости, кровь). Они составляют пластический материал основных несущих тканей, обеспечивают свойства всей среды организма в целом: поддерживают определённые значения pH, осмотического давления, сохраняют в нужных пределах кислотно-основное равновесие, обеспечивают устойчивость коллоидных систем в организме.
Микроэлементы неравномерно распределены между тканями и часто обладают сродством к определённому типу тканей и органов. Так цинк аккумулируется в поджелудочной железе; молибден – в почках; барий – в сетчатке глаза; стронций – в костях; йод – в щитовидной железе и др.
Содержание макроэлементов в организме достаточно постоянно, но даже сравнительно большие отклонения от нормы совместимы с жизнедеятельностью организма. Напротив, уже незначительные отклонения содержания микроэлементов от нормы вызывают тяжёлые заболевания. Анализ на содержание отдельных микроэлементов в органах и тканях – чувствительный диагностический тест, позволяющий обнаруживать и лечить различные заболевания. Так, снижение содержания цинка в плазме крови – обязательное следствие инфаркта миокарда. Уменьшение содержание лития в крови – показатель гипертонического заболевания.
Ещё одно различие в характере макро- и микроэлементов проявляется в том, что макроэлементы, как правило, входят в организме в состав органических соединений, тогда как микроэлементы либо образуют сравнительно простые неорганические соединения, либо входят в состав комплексных (координационных) соединений в качестве активных центров. Академик К. Б. Яцимирский назвал комплексообразующие микроэлементы «организаторами жизни».
Классификация минеральных веществ по В. В. Ковальскому
В. В. Ковальский, исходя из значимости для жизнедеятельности, подразделил химические элементы на три группы:
1. Жизненно необходимые (незаменимые) элементы. Они постоянно содержатся в организме человека, входят в состав ферментов, гормонов и витаминов: H, O, Ca, N, K, P, Na, S, Mg, Cl, C, I, Mn, Cu, Co, Fe, Zn, Mo, V. Их дефицит приводит к нарушению нормальной жизнедеятельности человека.
2. Примесные элементы. Эти элементы постоянно содержатся в организме животных и человека: Ga, Sb, Sr, Br, F, B, Be, Li, Si, Sn, Cs, Al, Ba, Ge, As, Rb, Pb, Ra, Bi, Cd, Cr, Ni, Ti, Ag, Th, Hg, U, Se. Биологическая роль их мало выяснена или неизвестна.
3. Примесные элементы (Sc, Tl, In, La, Pr, Sm, W, Re, Tb и др.). Обнаружены в организме человека и животных. Данные о количестве и биологическая роль не выяснены.
Большинство микроэлементов незаменимо для функционирования многих жизненно важных ферментов, их коферментов или простетических групп. Поскольку они используются в ферментах миллионы раз, потребности организма в микроэлементах, как и в витаминах, крайне незначительны. Однако без них обмен веществ невозможен.
В некоторых ферментах, так называемых металлоферментах, металлы (например, железо, медь, цинк и молибден) в неизмененном виде, в виде ионов или компонентов простетических групп прочно связаны в активном центре. При удалении этих металлов металлоферменты теряют свою функциональную активность. В активном центре металлы помогают связывать субстрат, переносить электроны и обеспечивать оптимальную пространственную конфигурацию фермента для эффективного катализа.
Железо участвует главным образом в реакциях переноса электронов, катализируемых оксидоредуктазами.
По крайней мере 90 ферментов содержат цинк. Цинксодержащие ферменты контролируют, например, образование СО2 и процесс переваривания белков. Цинк влияет на работу алкогольдегидрогеназы печени и ферментов, участвующих в передаче генетической информации.
Медь входит в основном в состав более десяти гидроксилаз. Медьсодержащий фермент тирозиназа катализирует, например, образование темного пигмента кожи и волос, меланина. Отсутствие или блокирование тирозиназы приводит к альбинизму. Другой медьсодержащий фермент аскорбатоксидаза - ответствен за быстрое расщепление витамина С при производстве сушеных продуктов из картофеля, яблок и овощей.
Биологическая роль кобальта состоит прежде всего в том, что он входит в состав витамина В12 и образующихся из него коферментов. Кроме того он участвует в ферментативных процессах синтеза наследственного материала клетки и аминокислотного обмена.
В отличие от металлоферментов у других ферментов те же ионы металлов связаны непрочно. Они часто находятся далеко от активного центра. Однако ионы металлов повышают активность ферментов и поэтому называются активаторами. С помощью активаторов в организме может осуществляться прямое управление различными ферментативными процессами.
Кроме вышеупомянутых микроэлементов многие ферменты активируются также марганцем, магнием, хромом, никелем, селеном и алюминием. Активность ферментов может также повышаться и регулироваться ионами электролитической среды клетки, такими, как ионы натрия, калия, кальция и хлора.
Вопросы 38-39 и частично 40 можно найти в таблицах по витаминам и минералам!!!
