

Химические свойства спиртов
Кислотные свойства спиртов выражены очень слабо. Низшие спирты бурно реагируют с щелочными металлами с образованием алкоголятов (в данном примере – этилалкоголята калия):
![]()
Спирты вступают в реакции замещения с галогеноводородами:
![]()
С кислотами (органическими или неорганическими) спирты вступают в реакцию этерификации в присутствии серной кислоты с образованием сложных эфиров:
O О
// H+ //
H3C—С—OH + HO—C2H5 → H3C—C—O—C2H5 + H2O
При нагревании спирта в присутствии сильной кислоты происходит отщепление молекулы воды от двух молекул спирта в результате межмолекулярной дегидратации и образуется простой эфир (в данном примере – диэтиловый эфир):
![]()
Амины
Амины - производные аммиака, полученные замещением атомов водорода на углеводородные радикалы.
По числу замещённых атомов водорода различают соответственно первичные, вторичные и третичные амины:
первичные (R–NH2),вторичные (R–NH–R') и третичные (R–N–R") амины.
I
R
Четвертичная аммониевая соль вида [R4N]+Cl- является органическим аналогом аммониевой соли.
По характеру органического радикала R амины подразделяют на алифатические (насыщенные, ненасыщенные) и ароматические амины.
По числу NH2-групп в молекуле амины делят на моноамины, диамины, триамины и т. д.
Построение названий аминов производится прибавлением приставки амино- к названию соответствующего углеводорода (первичные амины) или окончания -амин к перечисленным названиям радикалов, связанных с атомом азота (для любых аминов).
Амины, являясь производными аммиака, имеют сходное с ним строение и проявляют подобные ему свойства. Амины, как и аммиак, обладают основными свойствами, а значит, способны взаимодействовать с кислотами с образованием соответствующих аммониевых солей.
Амины вступают в реакции алкилирования с галогеналканами с образованием вторичных и третичных аминов. Алкилирование – это реакция введения в молекулу R- алкильного радикала.
CH3-NH2 + C2H5Br = CH3-NH-C2H5 +НBr (метилэтиламин)
Окисление аминов. Качественные реакции на амины.
Качественной реакцией на амины является реакция с азотистой кислотой с выделением газа азота и спирта.
C2H5NH2 + HNO2 → C2H5OH + N2↑+H2O
В ароматических аминах аминогруппа ориентирует другие заместители в орто- и пара-положения бензольного кольца. Поэтому галогенирование анилина происходит быстро и в отсутствие катализаторов, причем замещаются сразу три атома водорода бензольного кольца, и выпадает белый осадок 2,4,6-триброманилина (о,о,п-триброманилина):

Эта реакция бромной водой используется как качественная реакция на анилин.
Алифатические амины окисляются под действием сильных окислителей. В отличие от аммиака, низшие газообразные амины способны воспламеняться от открытого пламени. Реакция горения (полного окисления) аминов на примере метиламина:
4СH3NH2 + 9O2 -> 4CO2 + 10H2O + 2N2
Альдегиды и кетоны. РЕакция присоединения.
О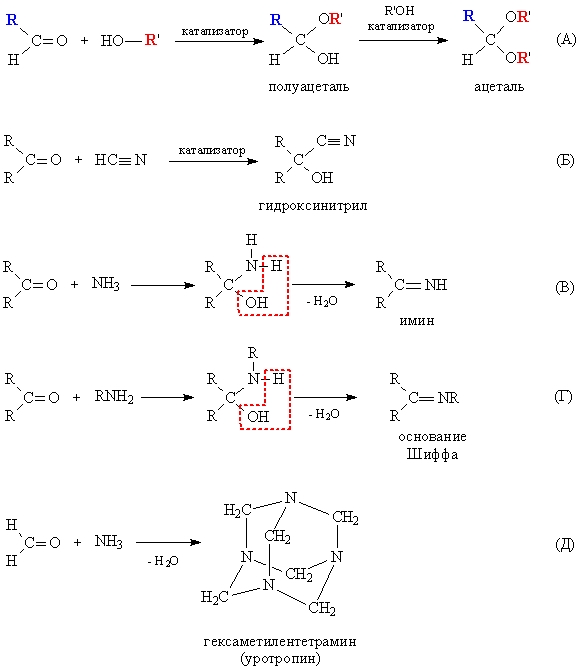 рганические
соединения, в молекуле которых имеется
карбонильная группа >С=O, называются
карбонильными соединениями, или
оксосоединениями. Карбонильные
соединения делятся на две большие
группы — альдегиды и кетоны.
рганические
соединения, в молекуле которых имеется
карбонильная группа >С=O, называются
карбонильными соединениями, или
оксосоединениями. Карбонильные
соединения делятся на две большие
группы — альдегиды и кетоны.
Альдегиды
содержат в молекуле карбонильную
группу, связанную с атомом водорода,
т. е. альдегидную группу — СН=O. Кетоны
содержат карбонильную группу, связанную
с двумя углеводородными радикалами,
т. е. кетонную группу
![]() .
.
В зависимости от строения углеводородных радикалов альдегиды и кетоны бывают алифатическими, алициклическими и ароматическими.
Изомерия альдегидов связана только со строением радикалов. Изомерия кетонов связана со строением радикалов и с положением карбонильной группы в углеродной цепи.
Номенклатура. Для альдегидов часто используют тривиальные названия, соответствующие названиям кислот (с тем же числом углеродных атомов), в которые альдегиды переходят при окислении. При составлении названия альдегида указывается название соответствующего углеводорода, к которому добавляется суффикс «аль», например, метаналь Н2С=О, этаналь Н3СС(Н)=О, пропаналь Н3ССН2С(Н)=О.
В более сложных случаях углеродную цепь группы R нумеруют, начиная с карбонильного углерода, затем с помощью числовых индексов указывают положение функциональных групп и различных заместителей.
![]()
В отличие от альдегидной, кетонная группа >C=O может находиться также в середине углеводородной цепи, поэтому в простых случаях указывают названия органических групп (упоминая их в порядке увеличения) и добавляют слово «кетон»: диметилкетон CH3–CO–CH3, метилэтилкетон CH3CH2–CO–CH3. В более сложных случаях положение кетонной группы в углеводородной цепи указывают цифровым индексом, добавляя суффикс «он». Нумерацию углеводородной цепи начинают с того конца, который находится ближе к кетонной группе.
![]()
В молекуле кетона радикалы могут быть одинаковыми или разными. Поэтому кетоны, как и простые эфиры, делятся на симметричные и смешанные.
Реакция с синильной кислотой. Одной из типичных реакций нуклеофильного присоединения альдегидов является присоединение синильной (циановодородной) кислоты, приводящее к образованию ά- оксинитрилов:
Реакция присоединения и отщепления.
Реакция взаимодействия с аммиаком и аминами идет по типу «присоединение-отщепление», на первой стадии происходит присоединение аммиака или амина, а на второй стадии происходит отщепление воды с образованием двойной связи между карбонильным атомом углерода и атомом азота аминогруппы. Таким образом, образуются соединения, называемые основаниями Шиффа – соединения, содержащие фрагмент >C=NR. Соединения, образованные присоединением аминов, называются имином, гидроксиламином – оксимом, гидразином – гидразоном.
Продукт взаимодействия формальдегида с аммиаком несколько иной – это результат циклизации трех промежуточных молекул, в результате получается каркасное соединение гексаметилентетрамин, используемое в медицине как препарат уротропин.
Окисление и восстановление альдегидов и кетонов.
Восстановление – это процесс увеличения числа атомов водорода в молекулах органических соединений и уменьшения числа атомов кислорода. Присоединение водорода к альдегидам осуществляется в присутствии катализаторов (Ni, Co, Pd и др.) и приводит к образованию первичных спиртов (А). Присоединение водорода к кетонам приводит к образованию вторичных спиртов (Б).
Реакции окисления. Альдегиды и кетоны по-разному относятся к действию окислителей. Альдегиды легко (значительно легче, чем спирты) окисляются в соответствующие карбоновые кислоты. (В).
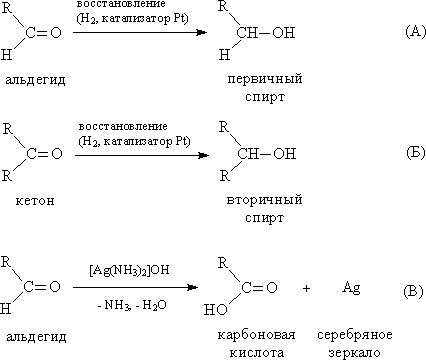
Кетоны окисляются значительно труднее, чем альдегиды. В мягких условиях кетоны не окисляются. При действии сильных окислителей в жестких условиях углеродная цепь молекулы кетона разрушается рядом с карбонильной группой и образуются кислоты с меньшим числом атомов углерода.
Химические свойства карбоновых кислот. Реакция замещения.
1. Диссоциация кислот. В водном растворе карбоновые кислоты диссоциируют:
![]()
Однако это равновесие диссоциации сильно сдвинуто влево, поэтому карбоновые кислоты, как правило, слабые кислоты.
Вследствие взаимного влияния атомов в молекулах дикарбоновых кислот они являются более сильными, чем одноосновные.
2. Образование солей. Карбоновые кислоты обладают всеми свойствами обычных кислот: реагируют с активными металлами, основными оксидами, основаниями:
![]()
3. Образование
функциональных производных. Для
карбоновых кислот характерны реакции
замещения гидроксильной группы в
![]() с образованием
функциональных производных кислот,
имеющие общую формулу R—СО—X; здесь R
означает алкильную, арильную, амино-
группы, группы галогенов.
с образованием
функциональных производных кислот,
имеющие общую формулу R—СО—X; здесь R
означает алкильную, арильную, амино-
группы, группы галогенов.
а![]() )Хлорангидриды
получают действием хлорида фосфора
(V) на кислоты:
)Хлорангидриды
получают действием хлорида фосфора
(V) на кислоты:
б) Сложные эфиры образуются при нагревании кислоты со спиртом в присутствии серной кислоты - реакция этерификации:
![]()
в) Реакции хлорангидридов карбоновых кислот с аммиаком приводят к образованию амидов:
![]()
4. Окислительно-восстановительные реакции карбоновых кислот.
Карбоновые кислоты при действии восстановителей способны превращаться в альдегиды или спирты:
![]()
Муравьиная кислота — сильный восстановитель и легко окисляется до СО2. Она дает реакцию “серебряного зеркала”:
![]()
Кроме того, муравьиная кислота окисляется хлором:
![]()
Аминоспирты. Основные представители, их производные и биороль.
Аминоспиртами
называют соединения, содержащие в
молекуле одновременно амино- и
гидроксигруппы. У одного атома углерода
эти группы удерживаются непрочно -
происходит отщепление аммиака с
образованием карбонильного соединения
или воды с образованием имина. Поэтому
простейшим представителем аминоспиртов
является 2-аминоэтанол — соединение,
в котором две функциональные группы
расположены у соседних атомов углерода.
С сильными кислотами 2-аминоэтанол
образует устойчивые соли.
![]()
Производное 2-аминоэтанола — димедрол — оказывает противоаллергическое и слабое снотворное действие. Обычно применяется в виде гидрохлорида.
Холин (триметил-2-гидроксиэтиламмоний) — известен как структурный элемент сложных липидов. Имеет большое значение как витаминоподобное вещество, регулирующее жировой обмен. В организме холин может образовываться из аминокислоты серина.
Сложный эфир холина и уксусной кислоты — ацетилхолин — наиболее распространенный посредник при передаче нервного возбуждения в нервных тканях (нейромедиатор).
Важную роль в организме играют аминоспирты, содержащие в качестве структурного фрагмента остаток пирокатехина. Они носят общее название катехоламинов. К этой группе относятся представители биогенных аминов, т. е. аминов, образующихся в организме в результате процессов метаболизма. К катехоламинам относятся дофамин, норадреналин и адреналин, выполняющие, как и ацетилхолин, роль нейромедиаторов.
Гидрокскикислоты.Основные представители, их производные и их биороль.
Гидроксикислоты – гетерофункциональные соединения, содержащие карбоксильную и гидроксильную группы. По взаимному расположению функциональных групп различают ά -,β -, γ - и т.д. гидроксикислоты.
![]()
К гидроксикислотам, имеющим большое биологическое значение, относятся:
Гликолиевая кислота HOCH2COOH содержится во многих растениях, например, свекле и винограде.
Молочная кислота CH3CH(OH)COOH. Соли называются лактаты. Широко распространена в природе, является продуктом молочнокислого брожения углеводов.
Я![]() блочная
кислота HOOCCH(OH)CH2COOH.
Соли называются малаты.Содержится в
незрелых яблоках, рябине, фруктовых
соках.
блочная
кислота HOOCCH(OH)CH2COOH.
Соли называются малаты.Содержится в
незрелых яблоках, рябине, фруктовых
соках.
Лимонная кислота.
Соли называются цитраты.Содержится в плодах цитрусовых, винограде, крыжовнике.
Винная кислота (соли тартраты) HOOCCH(OH)CH(OH)COOH.
Бета-гидроксимасляная кислота CH3-CН(ОН)-CН2-CООН как промежуточный продукт окисления жирных кислот накапливается в организме у больных сахарным диабетом, являясь, в свою очередь, предшественником ацетоуксусной кислоты.
Гамма-гидроксимасляная кислота (ГОМК) НО-CH2-CН2-CН2-CООН оказывает наркотическое действие, практически нетоксична. Применяется в виде натриевой соли как снотворное средство а также в анестезиологии в качестве наркотическою средства при операциях.
Биологически важные реакции а-аминокислот. Декарбоксилирование. Образование биогенных аминов.
Аминокислоты — это органические бифункциональные соединения, в состав которых входят карбоксильная группа —СООН и аминогруппа —NH2.
Аминокислоты реагируют как с кислотами, так и с основаниями:
![]()
Трансаминирование - одна из реакций метаболизма аминокислот, которая заключается в переносе аминогруппы (NH2) из аминокислоты в кетокислоты; в результате образуется другая кетокислота и аминокислота.
Дезаминирование - это отщепление аминогруппы (—NH2) из молекулы органического соединения. Дезаминирование играет важную роль в процессах обмена веществ, в частности в катаболизме аминокислот. Доказано существование 4 типов дезаминирования аминокислот (отщепление аминогруппы)
Декарбоксилирование – это процесс отщепления карбоксильной группы аминокислот в виде СО2 получил название декарбоксилирования. Несмотря на ограниченный круг аминокислот и их производных, подвергающихся декарбоксилированию в животных тканях, образующиеся продукты реакции – биогенные амины – оказывают сильное фармакологическое действие на множество физиологических функций человека и животных. Например, в животных тканях с высокой скоростью протекает декарбоксилирование гистидина под действием специфической декарбоксилазы.
![]()
Общая качественная реакция α-аминокислот – это реакция с нингидрином. Все аминокислоты окисляются нингидрином с образованием продуктов, окрашенных в сине-фиолетовый цвет. Эта реакция может быть использована для количественного определения аминокислот спектрофотометрическим методом.
Крахмал, строение, биороль.
Крахмал – полисахарид растительного происхождения. Крахмал представляет собой смесь двух полисахаридов – амилозы (10-20%) и амилопектина (80-90%) Крахмал набухает и растворяется в воде, образуя вязкие растворы (гели). Химические свойства крахмала аналогичны свойствам моно- и дисахаридов. Крахмал гидролизуется под действием кислот (но не щелочей) и фермента амилазы. Конечным продуктом гидролиза крахмала является D-глюкоза.
(C6H10O5)n ---> (C6H10O5)m ---> C12H22O11 ---> C6H12O6
крахмал - декстрины - мальтоз - D-глюкоза
За счет спиралеобразной конформации амилоза способна образовывать соединения включения с молекулярным иодом. Комплексы крахмала с иодом имеют интенсивную синюю окраску. Реакция используется как качественная на иод и крахмал.
Хондроитинсульфаты, строение.
Хондроитинсульфаты — полимерные сульфатированные гликозаминогликаны. Являются специфическими компонентами хряща. Вырабатываются хрящевой тканью суставов, входят в состав синовиальной жидкости. Необходимым строительным компонентом хондроитинсульфата является глюкозамин, при недостатке глюкозамина в составе синовиальной жидкости образуется недостаток хондроитинсульфата, что ухудшает качество синовиальной жидкости и может вызвать хруст в суставах.
Как свидетельствует само их название, хондроитинсульфаты являются эфирами серной кислоты (сульфатами). Сульфатная группа образует эфирную связь с гидроксильной группой N-ацетил-D-галактозамина, находящейся либо в 4-м, либо в 6-м положении. Соответственно различают хондроитин-4-сульфат и хондроитин-6-сульфат.
![]()
Пятичленные гетероциклические соединения c одним гетероатомом.
К пятичленным гетероциклам с одним гетероатомом относят пиррол, фуран, тиофен.
Фуран - пятичленный гетероцикл с одним атомом кислорода:
![]()
Производное фурана 5-нитрофурфурол является родоначальником лекарственных средств - фурадонин, фуросемид, фуразолидон.
Ф![]() урадонин
- противомикробное средство. Эффективен
при заболеваниях мочевых путей.
урадонин
- противомикробное средство. Эффективен
при заболеваниях мочевых путей.
Тиофен обладает выраженными ароматическими свойствами. В реакциях электрофильного замещения (галогенирование, нитрование и др.) тиофен значительно активнее бензола.
![]()
Тиофен содержится в ихтиоловой мази. Производные тиофена – норсульфазол, витамин В1, биотин (витамин Н) – регулирует обмен веществ.
Пиррол - пятичленный гетероцикл с одним атомом азота.
![]()
Пиррол — бесцветная жидкость с запахом, напоминающим запах хлороформа. Пиррол слабо растворим в воде (< 6%), но растворим в органических растворителях. На воздухе быстро окисляется и темнеет.
Пятичленные гетероциклы с двумя гетероатомами
Имидазол и пиразол – пятичленные ароматические гетероциклы, содержащие два атома азота.
![]()
Имидазол входит в состав гистидина, являющегося α-аминокислотой, входящей в состав многих белков, в том числе гемоглобина; в составе ферментов осуществляет кислотный и основной катализ за счет амфотерных свойств имидазольного цикла.
Тиазол
![]()
Важнейшее производное тиазола - тиамин (витамин В1). Многие производные тиазола -лекарственные препараты, например, норсульфазол и фталазол. Тиазолидиновое кольцо - структурный фрагмент пенициллина и разнообразных полусинтетических пенициллинов.
Оксазол
![]()
Производные оксазола - оксазолоны -важные промежуточные соединения в синтезе аминокислот и пептидов.
Шестичленные азотсодержащие гетероциклы с одним гетероатомами.
Пиридин – шестичленный ароматический гетероцикл с одним атомом азота.
![]()
Производными пиридина являются никотиновая кислота и ее амид - никотинамид - две формы витамина РР.
К пиридиновым алкалоидам относят производные тропана. Представитель этой группы — тропан, является конденсированным бициклическим соединением, в состав которого входят пирролидиновое и пиперидиновое кольца.
Производными тропана являются атропин и кокаин — ценные лекарственные средства, используемые в медицине.
Х![]() инолин
и изохинолин – ароматические
гетероциклические соединения, содержащие
конденсированные бензольный и
пиридиниевый циклы.
инолин
и изохинолин – ароматические
гетероциклические соединения, содержащие
конденсированные бензольный и
пиридиниевый циклы.
хинолин изохинолин
Биологически активные производные хинолина и изохинолина
8-Гидроксихинолин и его производные – 8-гидрокси-5-нитрохинолин (5-НОК) и 8-гидрокси-7-иод-5-хлорхинолин (энтеросептол) – обладают сильным бактерицидным действием и используются как противовоспалительные и антисептические средства.
Хинин - алкалоид коры хинного дерева, эффективное противомалярийное средство.
Алкалоид опия - папаверин - спазмолитическое и сосудорасширяющее средство.
Шестичленные азотсодержащие гетероциклы с двумя гетероатомами
Пиримидин – 6-членный ароматический гетероцикл с двумя атомами азота.
![]()
Важную биологическую роль играют гидрокси- и аминопроизводные пиримидина.
![]()
Урацил, тимин и цитозин – нуклеиновые основания; входят в состав нуклеозидов, нуклеотидов, нуклеиновых кислот.
Наиболее стабильными являются оксо-форма для цитозина и диоксо-формы для урацила и тимина. Оксо-формы нуклеиновых оснований образуют прочные межмолекулярные водородные связи.
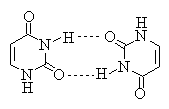
Ассоциация такого типа играет важную роль в формировании структуры ДНК.
Тиамин (витамин В1) содержит два гетероцикла – пиримидин и тиазол.
![]()
Тиамин является предшественником кофермента кокарбоксилазы, принимающего участие в декарбоксилировании a -кетокислот и синтезе кофермента А.
Конденсированные гетероциклы.
Индол – ароматическое гетероциклическое соединение, содержащее конденсированные бензольный и пиррольный циклы.
![]()
Цикл индола входит в триптофан, который является незаменимой (не синтезируется в организме человека) α-аминокислотой, входящей в состав животных и растительных белков.
![]()
Хинолины – ароматические гетероциклические соединения, содержащие конденсированные бензольный и пиридиниевый циклы.
хинолин Биологически активные производные хинолина.
8-Гидроксихинолин и его производные – 8-гидрокси-5-нитрохинолин (5-НОК) и 8-гидрокси-7-иод-5-хлорхинолин (энтеросептол) – обладают сильным бактерицидным действием и используются как противовоспалительные и антисептические средства.

Хинин - алкалоид коры хинного дерева, эффективное противомалярийное средство.
