
- •Экспериментальное получение нанослоистых дисульфидов вольфрама и молибдена
- •Методика эксперимента и описание экспериментальной установки
- •2 Исследование процессов получения и свойств нанослоистых дисульфидов вольфрама и молибдена
- •2.1 Свойства исходных нанодисперсных порошков вольфрама
- •2.2 Морфология нанослоистых дисульфидов вольфрама и молибдена
- •2.3 Трибологические свойства нанослоистых дисульфидов вольфрама и молибдена
- •Список литературы
2 Исследование процессов получения и свойств нанослоистых дисульфидов вольфрама и молибдена
2.1 Свойства исходных нанодисперсных порошков вольфрама
Согласно результатам просвечивающей микроскопии электровзрывные наночастицы вольфрама представляют собой сферические частицы средним диаметром 80…150 нм покрытой оксидной оболочкой, средняя толщина которой составляет 2-4 нм. Микрофотография частиц, исследованных с помощью просвечивающей электронной микроскопии показана на рисунке 4. Структура металлического ядра представляет собой упорядоченную кристаллическую решетку характерную для обычных металлов. При этом поверхностные слои частицы представляет собой аморфизированную оксидную оболочкунесплошной структуры (рисунок 4).

Рисунок 4 - Микрофотография наночастиц вольфрама, полученные с помощью просвечивающей электронной микроскопии.

Рисунок 5 - Рентгенограмма электровзрывного нанопорошка вольфрама.
Такая структура частицы связана, вероятно, с двухстадийностью процесса получения самой частицы. Первая стадия включает процесс электрического взрыва проводника, вещество проводника может находиться одновременно в четырех агрегатных состояниях: твердом, жидком, газообразном и плазмоподобном. Вторая стадия процесса приготовления электровзрывных наночастиц заключается в медленной пассивации (несколько часов) только что полученных наночастиц сначала во взрывной камере, а затем в специальном герметичном боксе в токе смеси аргона и воздуха. Такой режим получения обусловлен необходимостью снижения пирофорности частиц и сохранения их активности в метастабильном состоянии за счет образования оксидной оболочки с наличием двойного электрического слоя на ее поверхности. Эксперимент показал, что оксидная оболочка имеет аморфизированую структуру, на поверхности которой адсорбированы различные газы (воздух, водяной пар, аргон).
На основе результатов рентгеноструктурного анализа были проведены расчеты параметра элементарной ячейки электровзрывных наночастиц вольфрама. Кристаллическая решетка вольфрама представляет собой ГЦК. Для проведения сравнительного анализа кристаллической структуры эталонного вольфрама (картотека JCPDS) и полученного электровзрывного вольфрама был осуществлен расчет параметра кристаллической решетки согласно формуле (1). Было обнаружено увеличение параметра решетки рассчитанного для всех рентгеновских рефлексов эталона и исследуемого образца нанопорошка вольфрама. Наибольшее отклонение было обнаружено для пика со сто процентной интенсивностью (110) и составило 0.002 . Таким образом, исследуемый образец нанопорошка вольфрама имеет несколько увеличенные значение параметра кристаллической решетки по сравнению с эталонным вольфрамом.
2.2 Морфология нанослоистых дисульфидов вольфрама и молибдена
Продукты синтеза представляют собой легко разрушающиеся спеки, которые после измельчения и отмывки следов серы в керосине (с одновременной обработкой в ультразвуковых волнах) представляют собой нанослоистый порошок (НСП) (рисунки 6, 7). Агломераты WS2 и MoS2 представляет собой множество слипнувшихся нанослоистых пластин. Толщина наиболее тонких частиц нанослоистых порошков дисульфида молибдена и вольфрама составляет десятки нанометров, а ширина - сотни нанометров.
Повышенная интенсивность стопроцентного пика на рентгенограмме дисульфида вольфрама указывает на протяженную структуру кристаллов (рисуноки8), наличие которых также можно наблюдать на микрофотографиях WS2 и MoS2, полученных с помощью сканирующего микроскопа. При этом результаты рентгенофазового анализа показывают, что в конечных продуктах синтеза содержится, скорее всего, не менее 95% дисульфида металла.

а
б

Как показано в таблице 1 и 2, размеры областей когерентного рассеяния t (размеров кристаллитов в порошке) для дисульфидов молибдена и вольфрама лежат в пределах от 40 до 70 нм. Расчет толщины частиц произведен основе формулы Шеррера (8) из рентгенограмм (рисунке 8 и 9):
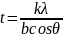 (8)
(8)
 (9)
(9)
где,
k
– постоянная зависящая от формы
кристаллита;
 – длина волны рентгеновского излучения;
b
- ширина на полувысоте;
– длина волны рентгеновского излучения;
b
- ширина на полувысоте;
 - угол Брэгга. Данные, полученные из
таблицы 1 и 2, были получены при значениях
k
= 0.89 и
=
1.54
- угол Брэгга. Данные, полученные из
таблицы 1 и 2, были получены при значениях
k
= 0.89 и
=
1.54 (
( ).
).
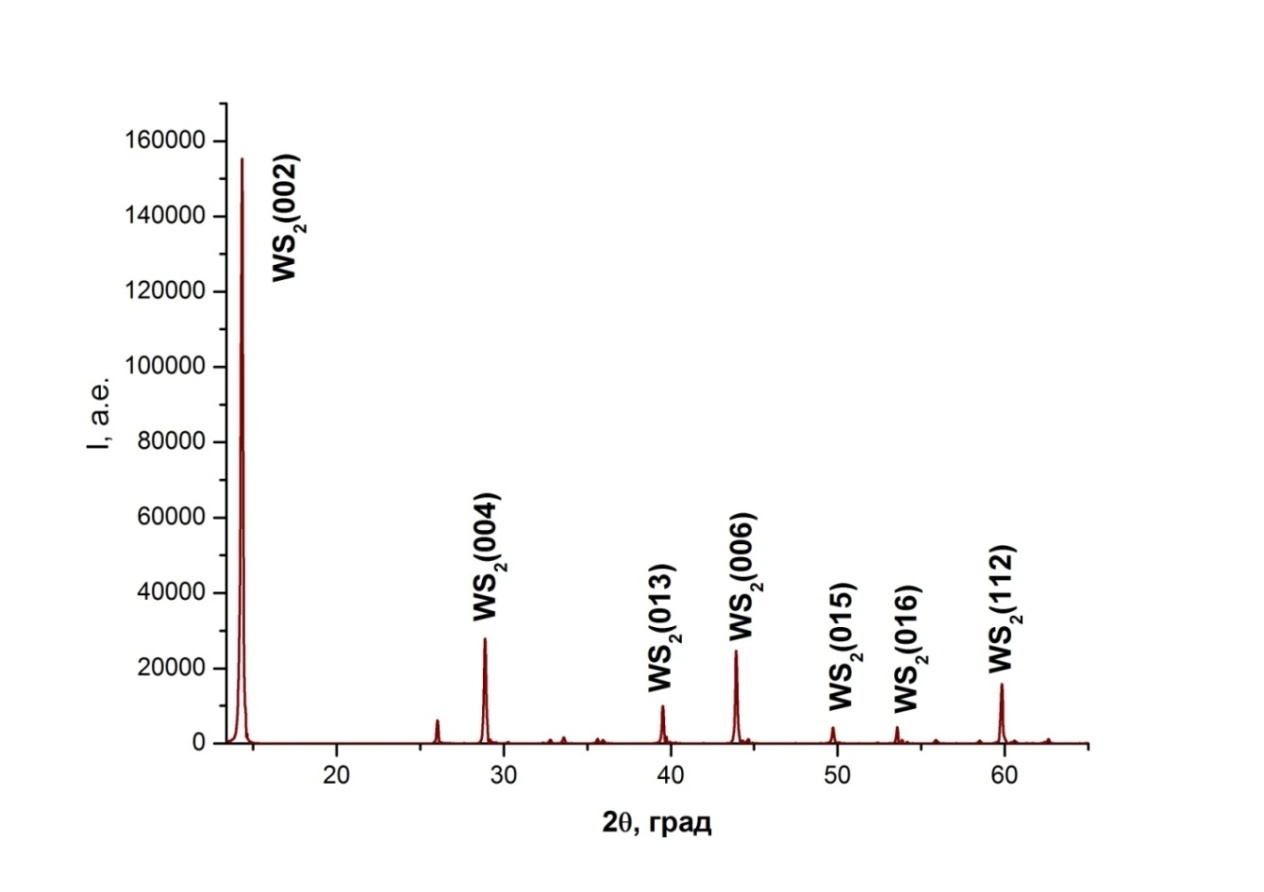
Рисунок 8 - Рентгенограмма дисульфида молибдена.

Рисунок 9 - Рентгенограмма дисульфида вольфрама.
Таблица 1 - Расчет размеров областей когерентного рассеяния t для нанопорошка дисульфида вольфрама
№ |
Абс. ед. |
I,% |
2θ1 |
2 θ2 |
2 θ |
θ , град |
θ, рад |
b, рад |
h |
k |
l |
Cosθ |
t, нм |
1 |
156064 |
100 |
14,25 |
14,41 |
14,33 |
7,16 |
0,13 |
0,00283 |
0 |
0 |
2 |
0,992 |
51,76 |
2 |
27975 |
17,93 |
28,81 |
28,94 |
28,88 |
14,44 |
0,25 |
0,00238 |
0 |
0 |
4 |
0,968 |
60,92 |
3 |
9997 |
6,41 |
39,45 |
39,59 |
39,52 |
19,76 |
0,34 |
0,00119 |
1 |
0 |
3 |
0,941 |
60,91 |
4 |
24910 |
15,96 |
43,86 |
44,01 |
43,93 |
21,97 |
0,38 |
0,00249 |
0 |
0 |
6 |
0,927 |
58, 52 |
5 |
4325 |
2,77 |
49,64 |
49,79 |
49,72 |
24,86 |
0,43 |
0,00262 |
1 |
0 |
5 |
0,907 |
68, 35 |
6 |
4284 |
2,75 |
53,50 |
53,63 |
53,56 |
26,78 |
0,47 |
0,00223 |
1 |
0 |
6 |
0,893 |
66,41 |
7 |
15934 |
10,21 |
59,89 |
59,74 |
59,82 |
29,91 |
0,52 |
0,00260 |
1 |
1 |
2 |
0,867 |
67,013 |
Таблица 2 - Расчет размеров областей когерентного рассеяния t для нанопорошка дисульфида молибдена
№ |
Абс. ед. |
I,% |
2θ1 |
2 θ2 |
2 θ |
θ , град |
θ, рад |
b, рад |
h |
k |
l |
Cosθ |
t, нм |
1 |
149296 |
100 |
14,40 |
14,53 |
14,46 |
7,23 |
0,13 |
0,00228 |
0 |
0 |
2 |
0,992 |
61,15 |
2 |
4994 |
3,35 |
29,10 |
29,24 |
29,17 |
14,58 |
0,25 |
0,00238 |
0 |
0 |
4 |
0,968 |
60,16 |
3 |
2828 |
1,89 |
32,97 |
33,16 |
33,06 |
16,53 |
0,29 |
0,00317 |
1 |
0 |
1 |
0,959 |
45,67 |
4 |
2368 |
1,59 |
34,06 |
34,24 |
34,15 |
17,07 |
0,30 |
0,00313 |
1 |
0 |
2 |
0,956 |
46,36 |
5 |
2946 |
1,97 |
38,16 |
38,36 |
38,26 |
19,13 |
0,33 |
0,00348 |
1 |
0 |
4 |
0,945 |
42,13 |
6 |
3742 |
2,51 |
41,00 |
41,20 |
41,10 |
20,55 |
0,36 |
0,00351 |
0 |
1 |
5 |
0,936 |
42,21 |
7 |
18139 |
12,15 |
44,30 |
44,48 |
44,39 |
22,20 |
0,39 |
0,00310 |
0 |
0 |
9 |
0,926 |
48,32 |
8 |
3028 |
2,03 |
47,92 |
48,12 |
48,02 |
24,01 |
0,41 |
0,00356 |
1 |
0 |
7 |
0,913 |
42,59 |
9 |
2634 |
1,76 |
51,87 |
52,08 |
51,97 |
25,99 |
0,45 |
0,00369 |
0 |
1 |
8 |
0,898 |
41,79 |
10 |
4361 |
2,92 |
54,05 |
54,15 |
54,10 |
27,05 |
0,47 |
0,00178 |
1 |
0 |
6 |
0,891 |
87,27 |
11 |
2181 |
1,46 |
58,50 |
58,25 |
58,37 |
29,13 |
0,51 |
0,00422 |
1 |
1 |
0 |
0,874 |
37,57 |
Таким образом, значения размеров частиц, определенных с помощью СЭМ (рисунки 6, 7) сравнимы со значениями, рассчитанными по формуле Шеррера на основании рентгеновских данных.
Таблица 3 - Расчет значений а и с для решетки НСП WS2
№ |
I, % |
h |
k |
l |
2θ, град. |
θ, рад |
sinθ |
d, Å |
а, Å |
с, Å |
1 |
100 |
0 |
0 |
2 |
14,34 |
0,125 |
0,125 |
6,170 |
|
12,3394 |
2 |
17,93 |
0 |
0 |
4 |
28,92 |
0,252 |
0,250 |
3,084 |
|
12,3348 |
3 |
19,86 |
1 |
0 |
0 |
32,72 |
0,286 |
0,282 |
2,734 |
3,1568 |
|
4 |
16,83 |
1 |
0 |
1 |
33,50 |
0,292 |
0,288 |
2,672 |
3,1600 |
|
5 |
35 |
1 |
0 |
2 |
35,89 |
0,313 |
0,308 |
2,499 |
3,1562 |
|
6 |
15,96 |
0 |
0 |
6 |
43,96 |
0,384 |
0,374 |
2,057 |
|
12,3435 |
7 |
2,77 |
1 |
0 |
5 |
49,70 |
0,434 |
0,420 |
1,832 |
3,1581 |
|
8 |
2,75 |
1 |
1 |
0 |
58,38 |
0,509 |
0,488 |
1,579 |
3,1575 |
|
Таблица 4 - Расчет значений а и с для решетки НСП MoS2
№ |
I,% |
h |
k |
l |
2θ, град |
θ, рад |
sinθ |
d, Å |
c1, Å |
с2, Å |
a, Å |
1 |
100 |
0 |
0 |
2 |
14,47 |
0,126 |
0,126 |
6,114 |
12,228 |
|
|
2 |
3,35 |
0 |
0 |
4 |
29,15 |
0,254 |
0,252 |
3,060 |
12,239 |
|
|
3 |
1,59 |
1 |
0 |
2 |
34,13 |
0,298 |
0,293 |
2,624 |
|
18,407 |
|
4 |
1,97 |
1 |
0 |
4 |
38,23 |
0,334 |
0,327 |
2,351 |
|
18,368 |
|
5 |
2,51 |
1 |
0 |
5 |
41,17 |
0,359 |
0,352 |
2,190 |
|
18,25 |
|
6 |
12,15 |
0 |
0 |
6 |
44,3537 |
0,387 |
0,377 |
2,040 |
12,239 |
|
|
7 |
6,36 |
0 |
0 |
9 |
44,46 |
0,388 |
0,378 |
2,035 |
|
18,318 |
|
8 |
2,03 |
1 |
0 |
7 |
47,97 |
0,419 |
0,406 |
1,894 |
|
18,367 |
|
9 |
1,76 |
1 |
0 |
8 |
51,92 |
0,453 |
0,438 |
1,759 |
|
18,365 |
|
10 |
1,46 |
1 |
1 |
0 |
58,31 |
0,509 |
0,487 |
1,581 |
|
|
3,161 |
11 |
11,45 |
0 |
0 |
8 |
60,43 |
0,527 |
0,503 |
1,530 |
12,241 |
|
|
В таблицах 3 и 4 показаны расчеты параметров а и с для кристаллической решетки WS2 и MoS2. Расчет проводили на основе полученных рентгенограмм, которые показаны на рисунках 8 и 9. Используя значения углов 2θ, соответствующих пикам интенсивности на рентгенограмме, и индексов Миллера соответственно, можно вычислить параметры а и с, что и было сделано на основании формулы для гексагональной структуры. Для WS2а=3,158 Å и с=12,34 Å, а для MoS2 а=3,161 Å, с1=12,24 Å и с2=18,35 Å. Рентгенограмма показывает, что для дисульфида молибдена кроме гексагональной фазы есть наличие ромбоэдрической фазы и Mo2S3.
В работе Мержанова [9] сравнивались параметры решеток, электрические и антифрикционные свойства синтетических MoS2 и WS2 полученных методом СВС и природных (Таблица 5). Постоянные решетки для синтетического и природного дисульфида вольфрама практически совпадают, тогда как синтетический дисульфид молибдена представляет собой двухфазный материал по отношению к однофазному природному дисульфиду молибдена.
Таблица 5 - Характеристики кристаллической структуры дисульфидов вольфрама и молибдена
Соединение |
Постоянные решетки, Å |
||
природный |
СВС (Мержанов) |
СВС |
|
MoS2 |
a = 3.160 |
a = 3.158 |
а=3,161 |
c =12.29 |
с1 =12,29, с2 = 18,36 |
с1=12,24, с2=18,35 |
|
WS2 |
a = 3.155 |
a = 3.154 |
а=3,158 |
c = 12.35 |
c = 12.34 |
с=12,34 |
|
При горении серы с металлом во фронте волны горения может наблюдаться унос серы, основная часть дисульфида образуется в зоне прогрева исходной смеси за счет тепла, выделяющегося при реакции. Вероятно, увеличение выхода и дисперсности продукта возможно за счет снижения температуры синтеза при пониженных давлениях рабочего газа (препятствование коалесценции и спеканию вновь образующихся частиц дисульфида), а также изменяя плотность исходных смесей нанопорошков вольфрама или молибдена с серой. Также большое влияние на дисперсность получаемых дисульфидов оказывает размеры частиц исходных порошков вольфрама и молибдена. Поскольку сера в условиях синтеза должна реагировать с металлом на молекулярном уровне (в жидком или газообразном виде) и вероятно, что продукты тоже будут в ультрадисперсном состоянии, если температура процесса не превысит температуры плавления продуктов и не произойдет их спекание.
В эксперименте исследовали изменение температуры при синтезе дисульфида вольфрама и молибдена по мере добавки соли NaCl. Подготавливались таблетки без соли и с содержанием 2% соли. Для температурной зависимости для образца без соли характерен резкий рост и медленное охлаждение по времени (рисунки 10 и 11).
Из термограммы горения (рисунок 10) видно, что процесс горения имеет многостадийный характер. В переднем фронте волны синтеза, определяющем кинетику процесса, температурная «ступенька» практически совпадает с температурой кипения серы (960 С) при данном давлении. То есть можно сказать, что происходит взаимодействие вольфрама с расплавом серы при температуре ее кипения с образованием первичной пленки продукта на частицах вольфрама. Образование основной части дисульфидов происходит в высокотемпературной зоне дореагирования, которой на всех термограммах соответствует область с постепенным спадом температуры.
Как видно из рисунков 10 и 11 температура горения вольфрама с серой снижается с 1900С до 1500 С при добавлении соли в исходную шихту, тогда, как для смеси молибдена с серой при добавлении соли температура увеличивается. Это видимо, связано с тем, что при формировании дисульфида вольфрама происходит эндотермическая реакция - соль испаряясь, поглощает энергию. Об этом косвенно свидетельствует наличие игольчатых кристаллов NaCl на микрофотографиях конечных продуктов. Для дисульфида молибдена втаких кристаллов не было обнаружено, и, скорее всего, при его синтезе в присутствии соли происходит экзотермическая химическая реакция с образованием промежуточных химических соединений.

Рисунок 10 - Термограмма горения а) W и S, б) W и S с солью 2% [10].

Рисунок 11 - Термограмма горения а) Mo и S, б) Mo и S с солью 2% [10].
