
Лабораторная работа №2 / LABA_H2
.DOC
Лабораторная работа №2
Цель работы: проделать опыты , наблюдая за происходящими изменениями . Написать уравнения реакций и расставить коэффиценты ионно-электронным методом.
Опыт
1. К 5 каплям раствора соли трехвалентного
хрома по каплям добавить избыток щелочи
до получения хромита(до растворения
первоначально образуюшегося осадка).Затем
добавить бромной воды(опыт проводить
в вытяжном шкафу).Смесь нагреть.Наблюдать
изменение цвета раствора из
зеленого,характерного для иона
![]() ,в желтый, характерный для иона
,в желтый, характерный для иона
![]()

Опыт
3. В три пробирки налить по 5 капель
раствора перманганата калия.В первую
добавить 5 капель раствора кислоты , во
вторую-5 капель воды , а в третью- 5 капель
концентрированного раствора едкого
натра. Затем во все три пробирки добавить
по несколько капель сульфита натрия
![]() .Наблюдать
изменение окраски в первой и третьей
пробирках и образование осадка во второй
пробирке. Отметить влияние среды на
реакции окисления-востановления.
.Наблюдать
изменение окраски в первой и третьей
пробирках и образование осадка во второй
пробирке. Отметить влияние среды на
реакции окисления-востановления.
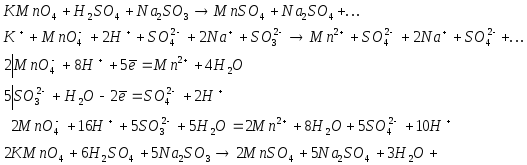
![]()

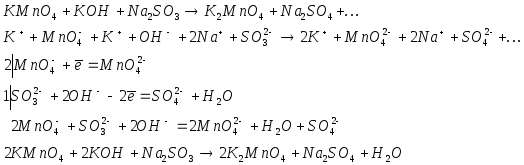
В
опыте 3,
![]() в зависимости от того с какой средой
взаимодействует в конце реакции
получается кислота, щелочь или осадок
с Mn.
в зависимости от того с какой средой
взаимодействует в конце реакции
получается кислота, щелочь или осадок
с Mn.
Опыт 5. К 5 каплям раствора соли двухвалентного марганца добавить по каплям раствор NaOH до образования осадка.Затем к этой смеси добавить несколько капель пероксида водорода.Осадок побуреет. Какие свойства проявил пероксид водорода?
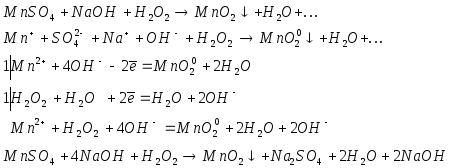
Опыт 6. К 5 каплям раствора перманганата калия прибавить несколько капель разбавленной серной кислоты для подкисления.Затем прибавить 5 капель пероксида водорода. Наблюдать выделение кислорода и обесцвечивание раствора. Какие свойства проявляет пероксид водорода?
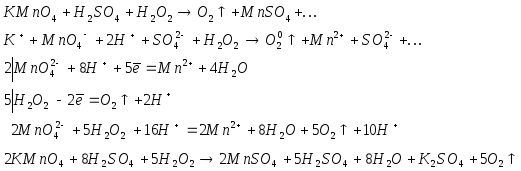
В
5 опыте
![]() взаимодействует с щелочной средой с
образованием воды и выпадением осадка
.
взаимодействует с щелочной средой с
образованием воды и выпадением осадка
.
В
6 опыте
![]() взаимодействует с кислой средой с
выделением кислорода .
взаимодействует с кислой средой с
выделением кислорода .
