
- •Основы палеогеографии
- •Предисловие
- •Глава I современная биосфера земли в космическом окружении
- •Химический состав земной коры (%)
- •Глава II методы восстановления прошлого биосферы
- •Глава III
- •Глава IV источники энергии и движение вещества в биосфере
- •Глава VII возникновение и эволюция гидросферы
- •Глава VIII возникновение и эволюция атмосферы
- •Глава IX эволюция организмов в истории биосферы
- •Глава X история формирования растительного покрова суши
- •Глава XI. Происхождение человека и его влияние на биосферу
- •Глава XII. Южные моря россии: о прошлом и современных экологических проблемах
- •Литература
Глава III
КОСМОХИМИЧЕСКИЕ ОСНОВЫ ВОЗНИКНОВЕНИЯ ЗЕМЛИ И БИОСФЕРЫ
Жизнь не является случайным явлением в мировой эволюции, но тесно с ней связанным следствием.
В.И. Вернадский
Очевидно, что свойства живого существа предопределяются оплодотворенной клеткой, так и жизнь предопределена существованием атома, таинство всего сущего заключается в самой низшей ступени.
А. Эйнштейн
РАСПРОСТРАНЕННОСТЬ ЭЛЕМЕНТОВ И ИХ КОСМОХИМИЧЕСКАЯ КЛАССИФИКАЦИЯ
Химический состав любого скопления материи определяет пути его развития и различных усложняющихся процессов, ведущих к образованию звездных структур, планетных оболочек, минералов и горных пород, и в конце концов живых организмов. Решающая роль в образовании живого вещества принадлежала немногим химическим элементам (Н, С, N, О). Коренная причина возникновения жизни в мировой эволюции состояла в создании особого сочетания химических элементов, наиболее оптимально соответствующих атомному составу организмов. Первым этапом в формировании этого сочетания был синтез атомов в космических условиях - нуклеосинтез. Вторым этапом - дифференциация вещества в соответствии со свойствами самих атомов химических элементов.
Поэтому решая основные проблемы эволюции биосферы, мы естественно, обращаемся к основным закономерностям распространенности химических элементов.
Благодаря усилиям многих поколений исследователей, применивших разные методы анализа, удалось получить надежные данные о составе звезд и Солнца, земной коры и метеоритов, горных пород поверхности Луны и некоторых планет. При обобщении этих данных построен график относительного распространения атомов в нашей Галактике, который представлен на рис. 13, как функция порядкового номера в таблице Менделеева. Эти данные относятся к 106 атомам кремния и расположены в порядке возрастания Z. Кремний выбран потому, что относится к труднолетучим и в то же время распространенным элементам. Относительная распространенность выражена в логарифмах числа атомов. Картина атомной распространенности на рис. 13 позволяет выявить следующие закономерности:
1. Логарифмическая кривая атомной распространенности является функцией заряда ядра. Распространенность элементов неравномерно убывает по мере увеличения атомного номера. Общий ход распространенности элементов как функции сначала резко падает, затем в области Z > 40 становится близким к горизонтальному. Отмеченная зависимость распространенности атомов носит общий характер, но зачастую и резко нарушается флуктациями вверх и вниз от некоторого среднего значения кривой.
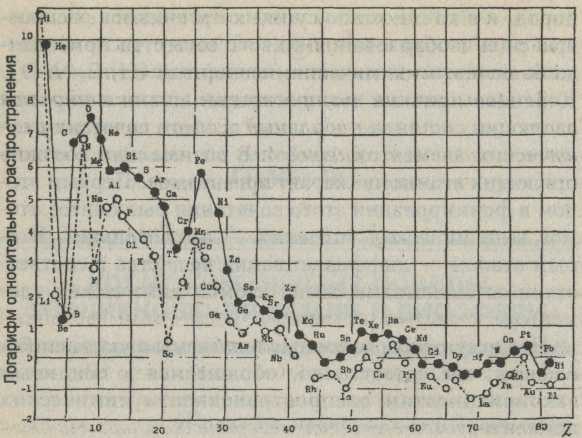
Рис. 13. Космическая распространенность химических элементов в зависимости от порядкового номера Z в таблице Менделеева. Черными кружками отмечены четные элементы, светлыми - нечетные.
2. В природе четные атомы преобладают над нечетными. Исключением из этого правила является обильно содержащийся в Космосе водород. Значение четности выражается правилом Гаркинса - элемент с четным значением 7 более распространен, чем элемент нечетный по соседству в таблице Менделеева. Более современная формулировка этой закономерности предложена Г. Зюссом: сумма космического распространения изобар с четным А (массовым числом) всегда больше суммы соседних изобар с нечетным А.
3. Повышенным распространением отличаются элементы, наиболее обильный изотоп которых имеет массовое число кратное 4. В данном случае можно привести следующий характерный пример:
А = 4 12 16 20 24 28 32
He C O Ne Mg Si S
Перечисленные элементы с указанными изотопами имеют отчетливо выраженную повышенную распространенность. Изотоп А = 8 (соответственно 8Ве) является неустойчивым и в природе отсутствует.
4. Максимальным распространением отличаются нуклиды с магическими значениями протонов и нейтронов. Эту закономерность следует понимать как значительное преобладание атомов с заполненными ядерными оболочками, которые соответствуют магическим числам. Из ядерных характеристик отчетливо выступают магические числа:
2, 8, 20, 50, 82, 126.
Менее выразительно в распространении выделяются числа: 10, 14, 28, 40, 58, 60 и 70. Магические числа относятся как к протонам, так и к нейтронам. К дважды магическим относятся изотопы 4Не, 16О, 40Са, 90Zr, 190Sn, 208Pb.
5. Максимумы распространения нуклидов определяются энергией ядерной связи (дефектом масс). Эта зависимость впервые была замечена при получении точных данных о ядерных массах. Кривая на графике, показывающая удельную энергию связи на один нуклон,
как функции А (массового числа), возрастает и дает максимум в области Mn, Fe, Co, Ni (соответственно Z = 24 - 28), а затем плавно понижается в сторону тяжелых элементов. Наиболее очевидно влияние ядерной упаковки на распространенность элементов: Мn, Fe, Co, Ni, которые образуют отчетливо выраженный «железный максимум» на кривой космической распространенности элементов.
6. Минимумы распространения связаны с неустойчивостью нуклидов в условиях термоядерных реакций. Наиболее резкие минимумы на кривой распространенности представляет триада Zi, Be, В. Термоядерные реакции между обильным в звездах водородом и указанными элементами происходит при температурах порядка 106 К. Поэтому термоядерные реакции приводят в первую очередь к выгоранию Be, В согласно:
7Zi +1H → 2 4Не
11Ве + 1H → 3 4Не.
В то же время в процессах ядерного синтеза образование вышеуказанных элементов маловероятно, поскольку 8Ве моментально распадается на два ядра гелия.
Некоторые другие минимумы связаны с резкими изменениями в составе нуклидов. В частности у элементов Z > 34 тяжелые стабильные изотопы преобладают над легкими. Имеет место также обратная зависимость между распространенностью изотопов и величиной поперечного сечения захвата нейтронов.
Таким образом, космическое распространение элементов не является случайным. Оно коррелируется с рядом их ядерных свойств, а не с одним свойством, из которых ведущее значение имеют Z и А, связанная с ними четность, состав нуклонов и наличие заполненных ядерных оболочек (магические числа). Представляется несомненным, что современная картина атомного состава Космоса обусловлена не единым универсальным процессом ядерного синтеза, а последовательным ходом различных ядерных процессов, взаимосвязанных с развитием древних космических систем, предшествующих формированию Солнечной системы.
Наиболее распространенным элементом Космоса является водород. Атом его состоит из протона и электрона, из чего следует вывод, что современная космохимия Вселенной характеризуется резким преобладанием элементарных частиц по сравнению с остальными формами их сочетаний в виде элементов.
Таким образом, и в настоящее время в Космосе преобладают элементарные частицы, которые в благоприятных термодинамических условиях могут быть строительным материалом для синтеза всех известных и трансурановых элементов. За всю историю Вселенной относительно малая часть этого материала пошла на построение элементов. Большая часть осталась за бортом нуклеосинтеза.
Однако среди продуктов космического нуклеосинтеза повышенным распространением отличаются те химические элементы, которые пригодны для образования органических соединений, как предшественников формирования живого вещества. Необычайно длительная история Вселенной, связанная с рождением атомов, подготовила химическую основу появления жизни, что затронуло, однако, ничтожную долю вещества - биосферу нашей планеты.
Формирование Солнечной системы наступило вскоре после завершения нуклеосинтеза, когда при падении температур новорожденные атомные ядра оделись электронными оболочками, что создало возможность для химических процессов и химической эволюции. Состав отдельных членов Солнечной системы оказался обусловленным этими химическими процессами.
Учитывая летучесть элементов в космических условиях, можно предложить их космохимическую классификацию, которая может быть полезной при истолковании ранней истории Солнечной системы, связанной с химическими процессами. Эта классификация представлена на рис. 14. Названия групп элементов
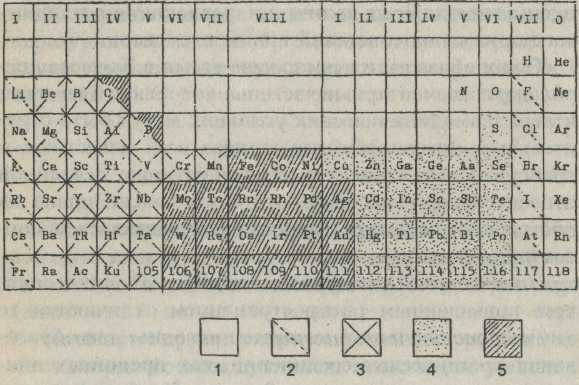
Рис. 14. Космохимическая классификация элементов.
1 - Весьма летучие атмофильные элементы.
2 - Летучие литофильные элементы.
3 - Тугоплавкие литофильные элементы.
4 - Относительно летучие халькофильные элементы.
5 - Тугоплавкие сидерофильные элементы.
были предложены видным норвежским ученым В.М. Гольдшмидтом (1888 - 1947). Классификация изображена в развернутой таблице Менделеева, которая расширена в область трансурановых элементов. Эти элементы существовали некоторое время в ранней истории Солнечной системы, но вскоре вымерли, как элементы неустойчивые. Согласно приведенной классификации элементы подразделяются на следующие группы:
Атмофильные элементы - представляют собой наиболее летучие вещества - газы в нормальных условиях. Имеют склонность создавать атмосферы планет. Некоторые другие элементы, вступая в соединения с газами, можно условно отнести к атмофильным. В частности, сидерофильный сам по себе, углерод, как твердое тело, связываясь химически с водородом и кислородом, образует летучие соединения СН4, СО, СО2, которые входят в состав планетных атмосфер.
Летучие литофильные элементы - сосредоточены преимущественно в верхних оболочках планет, в их литосферах, образуя прочные связи с кислородом. Атомы их легко образуют ионы с 8-электронной конфигурацией внешнего слоя. К летучим относятся элементы крайних групп периодической системы (1-й группы - щелочные металлы и VII группы - галоиды).
Тугоплавкие литофильные элементы - слагают основную часть каменных метеоритов и обширных мантий планет земной группы. Они образуют тугоплавкие окислы, входят в состав наиболее распространенных минералов - силикатов. К ним относятся обычные химические элементы земной коры и мантии - Al, Si, Mg, Ca, Ti.
Халькофильные элементы - имеют тенденцию соединяться с серой, т.е. ведут себя подобно меди (халькос - по-гречески медь). Атомы их образуют ионы 18-электронной конфигурации внешнего слоя. Большинство из них относится к летучим, как, например, ртуть.
Сидерофильные элементы - представлены типичными металлами. Они имеют склонность накапливаться совместно с железом (сидерос - по-гречески железо). Атомы их образуют ионы промежуточного типа с 9-17 электронной конфигурацией внешнего слоя. Они представлены металлами группы железа и платины, имеют высокую температуру плавления и кипения.
Свойства элементов перечисленных групп могут меняться в зависимости от температуры, давления и химического состава данной природной системы. Такие сидерофильные элементы как Fe, Co, Ni могут вести себя как халькофильные (с участием серы) и как литофильные (с участием) кислорода. Типичный литофильный кислород (в земной коре в качестве ведущего иона О2-) присутствует в молекулярной форме в атмосфере Земли (О2), а также в составе соединений СО, СО2 и может быть отнесен к атмофильным, как указано на рис. 14.
При остывании газа, новорожденного после последнего акта нуклеосинтеза, элементы образуют определенные соединения согласно космохимическим свойствам, указанным в таблице (см. рис. 14). При этом элементы и их соединения конденсируются обычно в порядке обратном их летучести - сначала тугоплавкие окислы и металлические конденсаты, затем несколько менее тугоплавкие соединения в виде силикатов и в конце - летучие и весьма летучие атмофильные элементы. Наиболее летучие - инертные газы - вообще избегают конденсации в пределах Солнечной системы, образуя газовые оболочки больших внешних планет.
СИНТЕЗ ЭЛЕМЕНТОВ В ЗВЕЗДАХ
Начало эволюции Вселенной знаменовалось Большим Взрывом (Big Bang), завершившим еще более ранние периоды развития Вселенной, о которых мы ничего не знаем. Теория первоначально горячей Вселенной, как теория огромного события в ее эволюции, в настоящее время получила подтверждение и является выдающимся научным достижением. На основании этой теории можно выделить две кардинальные стороны истории вещества.
Первая стадия - дозвездная и догалактическая - определила тот примитивный набор элементарных частиц и легких ядер, который в дальнейшем послужил исходным строительным материалом для создания первичных галактик из звезд первого поколения. Она была универсальной, единым процессом, охватившим всю материю Вселенной. Первая стадия образования элементов была связана с расширением изотропной вселенной, вскоре после Большого Взрыва. Она ограничивалась образованием малого набора нуклидов. После сложных взаимодействий первичных частиц с античастицами, рождения электронных пар и аннигиляции, наступило время, когда протонов и нейтронов осталось почти поровну. При дальнейшем снижении температуры нейтроны распались, превратившись в протоны, электроны и антинейтрино. На первых стадиях расширения начался также захват нейтронов протонами и образование ядер дейтерия (D), трития (3Н), гелия (4Не). Первые в истории Вселенной ядерные реакции совершались следующим образом:
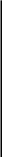

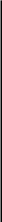
 n
+ р → D
+ γ
n
+ р → D
+ γ
D + D → 3Не + n → 3Н + р
Н + D → Не + n.
Содержание изотопа гелия 4Не достигло почти современного значения ~30% от общей массы вещества, что согласуется с астрофизическими определениями. Но на долю 3Не пришлось всего лишь 3 10 -6 от всей массы вещества. В ничтожных количествах возникали легкие нуклиды Zi, Be, В.
Вторая стадия - галактическая. Она знаменовалась возникновением и эволюцией звезд различных масс, в которых путем различных ядерных процессов создавались в различных соотношениях тяжелые элементы, включая элементы трансурановые. Возник весь набор химических элементов таблицы Менделеева. Вторая стадия знаменовалась бесчисленными индивидуальными путями развития галактик, звезд, газовых туманностей и планет, что определило широкие возможности химической эволюции.
В бесчисленных галактиках путем гравитационных стяжений возникли из водород-гелиевого вещества звезды - производители всех известных элементов. При взрывах звезд первых поколений образовались в пространстве газово-пылевые комплексы, послужившие материалом для построения звезд следующих поколений. Возник обширный космический круговорот вещества, представленный схематически на рис. 15.
Несомненно, что в него в прошлом было включено все вещество Солнечной системы. Элементарные расчеты и данные космохимии указывают на то, что в течение какого-то времени вещество нынешних планет находилось в условиях звездной эволюции, которые
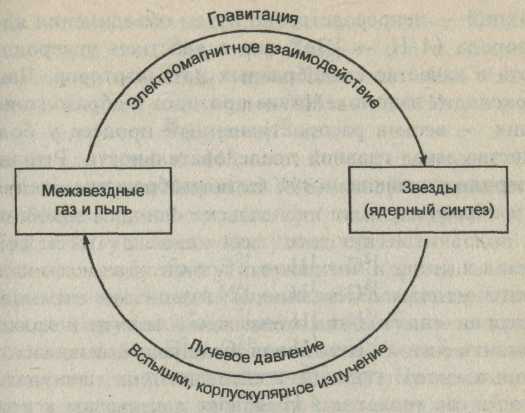
Рис. 15. Космический круговорот вещества в галактике.
знаменовались естественным синтезом атомных ядер. Эта эволюция завершилась незадолго до формирования планет, что явилось переломным событием в истории нашего вещества.
Благодаря усилиям выдающихся физиков и астрофизиков, к настоящему времени разработана достаточно полная теория происхождения химических элементов. В 1938 г. Г. Бете и С. Вейцзеккер выдвинули теорию термоядерных реакций в звездах, приводящих к синтезу гелия из водорода. Завершающим этапом исследований в данной области была работа английских астрофизиков - М. Бербидж, Дж. Бербидж, В. Фаулера и Ф. Хойла, в 1957 обосновавших теорию звездного синтеза элементов. Процессы ядерного синтеза могут быть охарактеризованы следующим образом:
1. Превращение водорода в гелий - водородное сгорание. Осуществляется в результате термоядерных реакций - непосредственно путем объединения ядер водорода (4 Н → 4Не) или с участием углерода и азота в качестве своеобразных катализаторов. Чаще происходит взаимодействие протонов с образованием гелия - весьма распространенный процесс у большинства звезд главной последовательности. Реакции углеродного цикла могут быть изображены следующим образом:
12С + 1Н → 13С + е+
13С + 1Н → 14N + γ
14N + 1H → 15 + e+
15N + 1Н → 12С + 4Не
4 Н → 4Не.
2. Превращение гелия в легкие элементы - сгорание гелия. Осуществляется путем термоядерных реакций гелия с 12С, а впоследствии и с другими легкими элементами. Таким образом могут возникать нуклиды с массовым числом кратным 4 - наиболее распространенные среди легких элементов:
12С + 4Не → 1бО
16О + 4Не → 20Ne
20Ne + 4He → 24Mg.
3. Альфа процесс ядерного синтеза происходит под действием α-частиц (ядер гелия), которые выбиваются путем фоторасщепления ранее образованных ядер жестким излучением от высоких температур, жесткая радиация возникает при высоких температурах в недрах звезд. Быстрые α -частицы реагируют с ранее образованными легкими ядрами и формируют следующие изотопы:
20Ne + α → 24Mg
24Mg + α → 28Si
28Si + α → 32S
32S + α → 36Аr
4. Равновесный процесс (е-процесс) происходит как наиболее горячий процесс при температуре 3-109 К. При этих условиях наступает статистическое равновесие между присутствующими ядрами и элементарными частицами. Возникают элементы относящиеся к группе «железного максимума» на кривой космической распространенности. К ним относятся элементы, прилегающие к железу. Процесс возможен в массивных звездах и протекает за короткое время.
5. s - процесс нейтронного захвата, при котором происходит медленный нейтронный захват уже существующими элементами с образованием элементов до висмута включительно 209Bi (Z=83). Процесс получил название от английского slow.
6. r - процесс быстрого (r - vapid) нейтронного захвата с образованием тяжелых элементов в трансвисмутовой области (Z>83), включая изотопы трансурановых элементов.
7. р - процесс, при котором возникают изотопы относительно богатые протонами при прочих равных условиях средних и тяжелых элементов. Протоны (р) ускоряются переменными магнитными полями в атмосферах звезд. Процесс протонного захвата относительно редкий процесс.
8. х - процесс, ответственный за образование легких малораспространенных изотопов, построение которых нельзя объяснить другими вышеприведенными процессами нуклеосинтеза.


 Прогресс
в построении средних и тяжелых элементов
зависел от массы звезды. Чем массивнее
звезда, тем
более высокую температуру она способна
вызвать в недрах при сжатии и тем
вероятнее рождение в ее центральных
областях все более тяжелых элементов.
В
известной степени стало традицией
образование тяжелых
элементов связывать с Сверхновыми
звездами при их
взрывах. Однако это не единственные
объекты,
которые могут быть производителями
тяжелых элементов.
Прогресс
в построении средних и тяжелых элементов
зависел от массы звезды. Чем массивнее
звезда, тем
более высокую температуру она способна
вызвать в недрах при сжатии и тем
вероятнее рождение в ее центральных
областях все более тяжелых элементов.
В
известной степени стало традицией
образование тяжелых
элементов связывать с Сверхновыми
звездами при их
взрывах. Однако это не единственные
объекты,
которые могут быть производителями
тяжелых элементов.
Вещество Земли и всей Солнечной системы имело общую судьбу в отношении ядерной эволюции, что подтверждается большой близостью изотопного состава ряда элементов разных объектов этой системы. Хронологическая последовательность основных событий в эволюции вещества Солнечной системы показана на рис. 16.
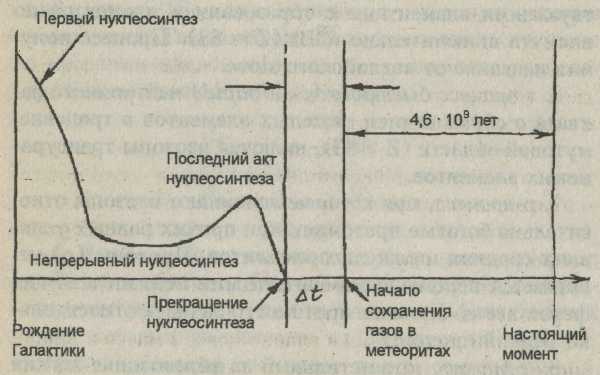
Рис. 16. Хронологическая последовательность в эволюции вещества Солнечной системы.
Вещество нашей планеты в далеком прошлом проходило стадии ядерного синтеза, газовой туманности с образованием твердых частиц, аккумуляции частиц в компактное сферическое тело, и наконец, стадию собственного развития.
ВЫМЕРШИЕ ЭЛЕМЕНТЫ В ИСТОРИИ СОЛНЕЧНОЙ СИСТЕМЫ
В процессе звездного ядерного синтеза возникали в большом количестве неустойчивые - радиоактивные изотопы. Большая их часть вскоре распалась, с периодом полураспада порядка секунд, часов и суток. Но их ничтожная часть с периодами полураспада свыше 109 лет сохранилась в настоящее время и представлена некоторыми нуклидами, из которых наиболее характерными являются 40К, 87Rb, 187Re, 232Th, 235U, 238U. Однако радиоактивные изотопы с периодами полураспада в интервале значений 106 - 108 лет вошли в состав молодой Земли на ранних стадиях развития, дожили свои «последние дни», так как это сейчас происходит с долгоживущими изотопами.
Еще в 1937 г. В.И. Вернадский говорил: «Радиоактивное изменение атомного веса урана в течение геологического времени, исчезновение его господствующего изотопа ставит другой, гораздо более общий вопрос, - не было ли времени, когда на Земле существовали атомы и химические реакции, ныне в ней отсутствующие - элементы № 61, 83, 87, 93, 94, 95, 96? Не исчезли ли они уже в главной своей массе к нашей эпохе? Во что, кроме гелия они превратились? И не было ли времени, когда поверхность планеты - в доархейское время - была расплавлена благодаря радиогенному теплу».
На большинство этих вопросов данные геохимии и космохимии изотопов, как и данные ядерной физики, дают в основном положительный ответ, хотя детали во многих отношениях остаются еще неясными и нерасшифрованными.
В настоящее время следы былой концентрации вымерших радиоактивных изотопов опознаются по изотопным аномалиям элементов - продуктов их распада. Вымерший радиоактивный изотоп оставляет признаки своего существования в виде заметного преобладания стабильного изотопа - прямого продукта распада по значению массового числа и по положению в таблице Менделеева.
В телах ранней Солнечной системы, по всей вероятности, присутствовали радиоактивные изотопы, представленные в таблице 17. Исходя из длительности распада, можно полагать, что в ранней Земле присутствовали радиоактивные изотопы: 92Nb, 129J, 146Sm, 205Pb, 236U, 244Pu, 247Cm, (Z = 112 - 114). Остальные изотопы (10Be, 2бА1, 107Pd, 237Np) не смогли дожить до стадии завершения формирования нашей планеты, ввиду своего быстрого распада (Т ~ 106 лет). Родоначальные тела метеоритов в связи с их малыми размерами формировались достаточно быстро, и поэтому в действительности мы наблюдаем в метеоритах следы вымерших изотопов с периодом полураспада порядка ~ 106 лет, по соответствующим изотопным аномалиям.
Распад некоторых короткоживущих изотопов дал возможность выяснить длительность промежутка времени между окончанием нуклеосинтеза и началом формирования твердых тел в Солнечной системе (Δt, см. рис. 16). В данном случае использовался распад изотопов по 129I → 129Хе и 244Рu → Хе. Расчеты величины Δt, проведенные многими авторами, давали значения порядка 50 - 150 млн. лет. Более точные
Таблица 17
Вымершие радиоактивные изотопы
Радиоактивный изотоп |
T Период полураспада лет |
Тип распада |
Продукт распада |
|
Бериллий |
10Ве |
2,5 Χ 106 |
β-распад |
10В |
Алюминий |
26 Аl |
0,74 Χ 10s |
+ β -распад |
26Mg |
Марганец |
53Мn |
3,7 Χ 106 |
+ β -распад |
53Сг |
Ниобий |
92Nb |
3,3 Χ 107 |
е-захват |
92Zr |
Палладий |
107Pd |
7 Χ 107 |
β -распад |
107Ag |
Йод |
129J |
1,7 Χ 107 |
β -распад |
129Хе |
Самарий |
146Sm |
5 Χ 107 |
α-распад |
142Nd |
Свинец |
205Pb |
5 Χ 107 |
е-захват |
205Tl |
Уран |
236U |
2,4 Χ 107 |
α -распад |
232Th |
Нептуний |
237Np |
2 Χ 106 |
α -распад и |
209Bi |
Плутоний |
244Pu |
8,2 Χ 107 |
осколочное |
232Th |
Кюрий |
247Cm |
1,6 Χ 107 |
деление |
207Pb |
Z = 112 - 114 |
n Χ l07(?) |
˝ |
? |
|
величины получить невозможно ввиду допущения некоторых исходных данных, которые не могли быть надежными.
Радиоактивный распад не мог совершаться необозримо долгое время, в противном случае радиоактивных элементов попросту не существовало бы в материале Солнечной системы. Очевидно, что сам по себе радиоактивный распад неизбежно указывает на процесс естественного синтеза радиоактивных и других стабильных изотопов в космической истории вещества Солнечной системы в целом. Согласно существующим расчетам возраста, это событие во времени было недалеким от эпохи образования Земли и планет (см. рис. 16). Основной вывод, вытекающий из современных геохронологических и изотопных данных представляется совершенно очевидным - происхождение Солнечной системы было органически связано с происхождением ряда химических элементов. Современная и вымершая радиоактивность Земли является прямым следствием естественного синтеза радиоактивных изотопов. По-видимому, в исторической последовательности Солнечная система образовалась на переломном этапе эволюции вещества - от ядерной эволюции к эволюции химической.
ХИМИЧЕСКАЯ ЭВОЛЮЦИЯ РАННЕЙ СОЛНЕЧНОЙ СИСТЕМЫ
После завершения ядерного синтеза, первичная туманность, окружавшая Солнце, образовалась из вещества достаточно свежего после нуклеосинтеза и была сильно радиоактивна. Первичный материал, из которого возникли планеты, был представлен сильно ионизированными разобщенными атомами, ядрами и электронами. Иначе говоря, это была плазма. Только после значительного снижения температур при остывании, ниже 2000°К, атомные ядра и многократно ионизированные атомы приобрели путем рекомбинации нормальные электронные оболочки, что создало условия для осуществления химических реакций и образования первых химических соединений. Наиболее распространенные химически активные элементы превращались в галовые молекулярные виды, а при дальнейшем охлаждении возникали твердые Частицы как конечные продукты конденсации солнечного газа.
Конденсация твердых и жидких частиц (капель) из солнечной туманности давно уже рассматривалась как один из важнейших физико-химических процессов в газовом облаке в ранней истории Солнечной системы. Первые указания на характер физико-химических процессов в протопланетном скоплении материи мы находим в химическом составе хондритов - наиболее распространенных каменных метеоритов. Важнейшей чертой химического состава этих метеоритов являются вариации степени окисления вещества - от состояния максимального окисления до полного восстановления железа у энстатитовых хондритов. Эта закономерность была замечена давно и выражена в правилах Г. Прайора.
Процессы окисления железа в веществе солнечного состава были изучены в 1950 г. В.М. Латимером, который показал, что реакция:
3 Fe + 4 Н2О ↔ Fe3O4 + 4 Н2
при константе равновесия
РН2О
К = РН2
протекает слева направо при температуре ниже 400°К. Из этого следует, что степень окисления железа в веществе хондритовых метеоритов указывает на температурные условия их формирования и, следовательно, на температурные условия ранней истории Солнечной системы. Родоначальные тела энстатитовых хондритов, содержащих металлическое железо, формировались при более высоких температурах, чем углистые хондриты, которые содержат магнетит Fe3O4.

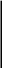 Большая
часть тел астероидного пояса по оптическим
данным
сложена материалом типа углистых
хондритов,
указывающих, что эта область солнечной
туманности знаменовалась процессами
окисления вещества с максимальной
полнотой.
Большая
часть тел астероидного пояса по оптическим
данным
сложена материалом типа углистых
хондритов,
указывающих, что эта область солнечной
туманности знаменовалась процессами
окисления вещества с максимальной
полнотой.
В области ближайших к Солнцу планет земного типа проявилось неполное окисление железа. В минимальной степени оно относится к Меркурию, а вещество более отдаленного Марса оказывается более окисленным. Отсюда нетрудно заключить, что степень окисления протопланетного материала зависит от гелиоцентрического расстояния.
Понижение температуры первоначально горячей газовой системы солнечного состава приводит к последовательной конденсации сначала нелетучих - тугоплавких, затем труднолетучих и в самом конце наиболее летучих элементов и их соединений. Процесс конденсации горячего газа солнечного состава был количественно изучен и рассчитан по уравнениям химической термодинамики Л. Гроссманом, Дж. Ларимером, Дж. Льюисом и другими авторами. Результаты расчетов этих исследователей представлены на диаграмме рис. 17. На ней приведены интервалы температур конденсации соответствующих минералов в ходе понижения температур при падении давления от 1,00 до 0,007 атм. Однако в целом последовательность выделения минералов существенно не зависит от значений давления.
Конденсация элементов и их соединений в виде оксидов, силикатов, сульфидов проходила в определенной закономерной последовательности. Первыми конденсировались высокотемпературные оксиды в виде корунда, перовскита и силиката - мелилита. Однако они реагировали с газовыми компонентами туманности и превращались в другие минералы в интервале
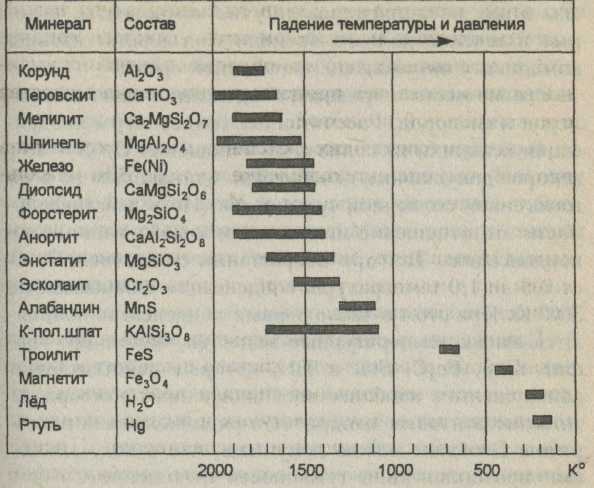
Рис. 17. Температуры конденсации элементов и их соединений при остывании газа солнечного состава.
температур 1500-1360° К. Следующим важным и распространенным конденсатом оказалось никелистое железо. Затем конденсировались силикаты, в которые вошли наиболее распространенные элементы О, Si, Mg, Ca, а последними выделились некоторые сульфиды, магнетит и ртуть. В процессе последовательной конденсации и выделения частиц твердой фазы в их состав входили и другие, менее распространенные химические элементы в соответствии со своими термодинамическими свойствами и величинами атомных, ионных радиусов. Так в состав силикатов входили преимущественно литофильные элементы, а в металлическую фазу типичные сидерофильные. Далее по мере появления низкотемпературных фаз в них накапливались летучие компоненты, которые в течение долгого времени составляли газовую компоненту окружающей остаточной среды.
Особое место в процессе конденсации занимали углерод и кислород. Рассчитанные температуры конденсации исходили из солнечного отношения С/О = 0,6, которое допускалось повсеместно одинаковым во всей гомогенной солнечной туманности. Но в действительности это отношение менялось, оказывая влияние на конденсацию. Так при возрастании отношения С/О от 0,9 до 1,0 температуры конденсации снижаются на 300°К. При этом в числе первых конденсатов появляются высокотемпературные вещества, например, графит, CaS, Fe3C, SiC и TiN, которые действительно обнаружены в наиболее восстановленных метеоритах типа энстатитовых хондритов и ряда железных метеоритов. В общем можно допустить, что в ходе эволюции протопланетной туманности отношение С/О в разных ее частях было изменчивым под влиянием разных факторов.
По мере дальнейшего охлаждения солнечной туманности до температур 400 - 300° К, происходит гидратация частиц ранее выделившихся силикатов. Она заключается во взаимодействии силикатов с парами воды. При этом взаимодействии энстатит, форстерит и диопсид превращаются в гидратированные силикаты:
Тальк Mg2Si4O10(OH)2
Серпентин Mg3Si2O5(OH)
Тремолит Ca2Mg5Si8O22(OH)2
Гидратированные силикаты являются скрытыми носителями такого важного летучего вещества как вода. В тонкодисперсном состоянии они обладают высокой адсорбционной способностью и поэтому могут из окружающей среды захватывать не только молекулы воды, но также обычные и инертные газы, а также летучие вещества вообще. Молекулы Н2О - первые соединения, возникающие в ходе охлаждения солнечного газа.
Следует также отметить, что гидратированные силикаты обладают свойствами катализаторов. Поэтому на последних стадиях охлаждения солнечной туманности они могли играть выдающуюся роль в синтезе высокомолекулярных соединений, включая органические вещества.
По данным космохимии представляется вероятным, что образование планет проходило в два этапа. Первый выразился в охлаждении газового диска и конденсации части его вещества в частицы разного состава. Таким способом возникла газово-пылевая туманность, которая оказалась неустойчивой и из-за разной скорости остывания в зависимости от расстояния до Солнца, приобрела химическую неоднородность, дополнительно усиливающуюся под влиянием давления солнечных лучей и корпускулярного истечения материи Солнца.
Второй этап выразился в аккреции - аккумуляции конденсированных частиц в отдельные сгущения - планетезимали, протопланеты. Можно полагать, что эти два этапа не были резко разделены друг от друга во времени. Наоборот, вполне вероятно, что аккумуляции в отдельных зонах протопланетного диска началась тогда, когда конденсация еще не завершилась.
Эволюция солнечной туманности схематически представлена на рис. 18. Ближе к Солнцу внутренние планеты земного типа образовались при сгущении преимущественно высокотемпературной фракции со значительным содержанием металлического железа.
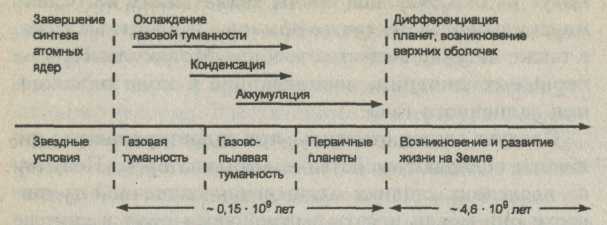
Рис. 18. Последовательность событий в истории Солнечной системы.
Так ближайший к Солнцу Меркурий состоит на 2/3 из металлического железа, а самый удаленный из внутренних планет Марс - вероятно, только на 1/4. В пределах астероидного пояса металлического железа содержится меньше, а большинство астероидов имеют полностью окисленное железо.
ОБРАЗОВАНИЕ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Жизнь на Земле связана с Космосом энергетически и по вещественному составу. В процессе жизнедеятельности организмы используют наиболее доступные атомы, которые способны к образованию устойчивых и кратных химических связей. Атомы углерода могут формировать длинные цепи, что приводит к возникновению бесчисленных полимеров. Сера и фосфор также образуют кратные связи, что создает возможность для поглощения энергии и переноса ее отдельными дозами.
В космических условиях наиболее распространенные атомы соединяются между собой, образуя молекулы, которые обнаружены методами современной радиоастрономии. К настоящему времени в облаках космического газа и в атмосферах холодных звезд обнаружено 100 видов молекул, большая часть которых состоит из атомов биофильных элементов, характерных для живого вещества. Большая часть обнаруженных космических молекул относится к углерод-содержащим, включая 10 атомные (примером может служить молекула простой аминокислоты - глицина NH2CH2COOH). Некоторые из космических молекул имеют 13 атомов. Английские астрофизики Ф. Хойл и Ч. Викрамасингх считают, что эти открытия не являются случайными и что в ближайшее время в космическом пространстве будут обнаружены и другие аминокислоты, а также детали нуклеиновых кислот.
Таким образом, в отношении состава космохимия Вселенной создает неограниченные возможности для различных комбинаций углерода с другими элементами по законам химической связи. По мнению астрофизиков, органических соединений в Космосе значительно больше, чем чисто неорганических - частиц космической пыли.
Но пути образования молекул органических веществ в Космосе еще далеко не выяснены и представляют большую научную проблему. Ввиду низкой концентрации элементов, сами химические реакции - маловероятны. Поэтому можно допустить, что в построении межзвездных молекул принимают участие частицы космической пыли. Наиболее распространенные молекулы Космоса представлены СО. Они, вероятно, возникают в условиях звездных атмосфер при достаточной плотности вещества и затем выбрасываются в космическое пространство.
При выяснении условий возникновения жизни и биосферы особое значение имеет нахождение органических веществ в метеоритах, фиксирующих далекую историю органической космохимии в процессе остывания солнечной туманности, где на завершающих стадиях эволюции создавались благоприятные условия для целого ряда химических реакций между биофильными элементами и их простейшими молекулами.
Органическое вещество в метеоритах впервые обнаружил знаменитый шведский химик И. Берцелиус в 1834 г. при анализе углистого хондрита Алаис. В дальнейшем было установлено присутствие в метеоритах твердых углеводородов, соединений С, Н, О, S. Наиболее обстоятельному исследованию подвергались углистые хондриты, в которых почти весь углерод находится в составе органического вещества. Содержание углерода и некоторых летучих веществ в углистых хондритах разного типа характеризуется следующими величинами (в %):
Углистые С S H2O хондриты С1 2,7 - 5,0 5,2 - 6,7 18 - 22 С2 1,1 - 2,8 2,3 - 3,7 8 - 17 С3 0,2 - 0,6 1,8 - 2,4 0,1 - 1,5 |
Очевидно, что максимальное содержание углерода, серы и воды встречено в углистых хондритах С1, а минимальное - в хондритах СЗ. Таким образом в настоящее время мы имеем надежные данные о том, что в родоначальных телах углистых хондритов в результате процессов их формирования возникли сложные органические соединения - закономерный итог химической эволюции ранней Солнечной системы. Углистые хондриты типа СЗ представлены непрочными темными камнями, которые при растирании пальцами рассыпаются в пыль. Мелкозернистая масса составляет в них примерно 95%. В нее включены хондры состоящие из оливина и магнетита (размером 1 - 50 мкм). Минеральный состав метеорита этого типа представлен на рис. 19. Обращает на себя внимание тесная ассоциация органического вещества с низкотемпературными гидратированными силикатами - хлоритом, серпентином и сульфатами. Углистые хондриты типа С1 наиболее богаты органическими веществами абиогенного происхождения.
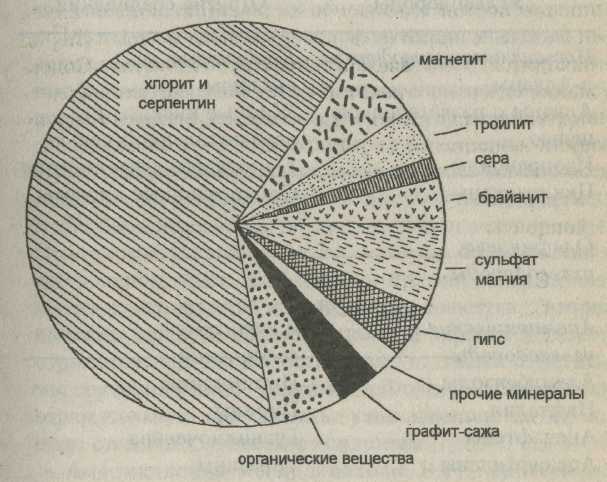
Рис. 19. Минеральный состав углистого хондрита Оргей. Площади на диаграмме пропорциональны весовым процентам содержания минералов.
К настоящему времени, благодаря исследованиям Г.П. Вдовыкина (1967, 1979), Э. Андерса, Р. Хаятсу, М. Штудира (1973, 1981), Дж. Брукса (1981), органические соединения метеоритов изучены довольно детально и обстоятельно. Наиболее тщательно изучались углистые хондриты.
Органические соединения метеоритов перечислены в таблице 18.
Таблица 18
Органические соединения метеоритов
Углеводороды |
Другие соединения |
Насыщенные углеводороды |
Карбоновые кислоты |
n-Алканы |
|
Алканы с разветвленной |
Жирные кислоты с |
цепью |
неразветвленной цепью |
Изопреноиды |
Бензолкарбоновые кислоты |
Циклоалканы |
Оксибензойные кислоты |
Олефиновые углеводороды |
|
Ароматические углеводороды |
Азотистые соединения |
Алкилбензолы |
Пиримидины |
Нафталин |
Пурины |
Аценафтены |
Гуанилмочевина |
Аценафтилены |
Триазины |
Фенантрены |
Порфирины |
Пирены |
Аминокислоты |
Нетрудно видеть, что список органических соединений в метеоритах оказывается довольно внушительным. Все эти органические соединения в той или иной мере соответствуют универсальным звеньям обмена веществ известных живых организмов: аминокислот, белкоподобных полимеров, полинуклеотидов и других соединений. Близость состава органических веществ метеоритов с составом живого вещества оказалась настолько тесной, что некоторые авторы допускали наличие в прошлом живых организмов непосредственно в самих метеоритах в какой-то период их существования. В 60-х годах по данному вопросу возникла дискуссия. Однако во всех исследованных органических соединениях метеоритов не было обнаружено оптической активности, что свидетельствует об их абиогенном происхождении.
Метеориты, содержащие органические вещества, являются осколками астероидов. Поскольку по результатам фотометрических измерений отражательной способности углистые хондриты и соответствующие астероиды оказались во многом сходны, то естественно, что все структурные, минеральные и химические особенности метеоритов, установленные в земных лабораториях, могут быть перенесены на соответствующие астероиды. Это темные астероиды С-типа, которых большинство в астероидном поясе. Естественно, что они содержат повышенное количество органического вещества, которое является одной из причин их темной окраски и низкой отражательной способности. Следует также отметить, что спутники Марса - Деймос и Фобос - обнаружили отражательную способность, указывающую на их состав, близкий к углистым хондритам.
Американские исследователи Р.Н. Заре и др. (1993) методом лазерной марс-спектрометрии изучили состав частиц космической пыли, попавших на поверхность Земли. В частицах была обнаружена различная органика - циклические ароматические соединения (углеводороды) и их алкализированные производные.
Некоторые ученые придают большое значение нахождению органического вещества в кометах, которые могли занести его на Землю. Но пока в кометах установлены лишь простейшие соединения углерода. Если ядра комет действительно состоят из смеси льда и каменного материала углисто-хондритового состава, то распространенность органического вещества будет охватывать огромное пространство всей Солнечной системы, включая облако Оорта.
Нетрудно заключить по данным космохимии метеоритов, что образование органических соединений в ранней Солнечной системе было типичным и массовым явлением. Наиболее интенсивно оно проявилось в пределах будущего астероидного пояса, но, вероятно, также охватывало и другие зоны первичной туманности, в том числе орбитальную зону формирования нашей планеты.
Минеральные ассоциации в углистых хондритах не являются случайными, а органически связаны с последними этапами химической эволюции протопланетной туманности, которая охладилась до низких температур. Органические соединения формировались при температурах ниже 500° К за счет взаимодействия газовых компонентов. Типичные минеральные ассоциации углистых хондритов возникали в интервале температур 425 - 350° К. Согласно Э. Андерсу различные естественные термометры показывают следующие температуры образования:
Термометр 18О/16О между CaMg(CO3)2 и Н2О 18О/16О между серпентином и Н2О 13С/12С между CaMg(CO3)2 и полимером 3Fe + 4Н2О ↔ Fe3O4 + 4Н2О Оливин + Н2О ↔ серпентин Распространенность таллия (Т1) |
Температура К 360 ± 5 300 ± 15 357 ± 21 <400 350 425 |
Для первых четырех химических термометров температура формирования не зависит от величины давления, а у пятого и шестого эта зависимость имеет место.
В остывающей туманности солнечного состава сохранялись газовые виды Н2, N2, CO, СО2, Н2О между которыми устанавливались определенные химические равновесия. Зависимость величин отношений химических соединений углерода и азота от температуры солнечной туманности показано на рис. 20 (согласно Э. Андерсу и Р. Хаятсу 1981). В космических условиях в широком интервале температур наиболее стабильной формой нахождения углерода является СО, поскольку для образования СО2 недостает распространенности кислорода. Первые органические соединения возникли преимущественно при химических реакциях между водородом, СО и простейшими соединениями азота. В этом случае вероятные реакции (типа Фишера - Тропша) могли выражаться следующим образом:
nСО + (2n + 2) Н2 → СnН2n+2 + n Н2О
или более конкретно, как это показано на рис. 20
20 СО + 41 Н2 → С20Н42 + 20 Н2О,
Реакции этого типа значительно ускоряются в присутствии катализаторов, которыми могли быть магнетит и гидратированные силикаты, выделившиеся раньше в процессе химической эволюции солнечной туманности. По микроструктурным данным метеоритов представляется, что органические соединения были синтезированы преимущественно на поверхности минеральных зерен, впоследствии вошедших в состав углистых хондритов. Под микроскопом было обнаружено, что много органического вещества этих метеоритов находится в виде округленных флюоресцирующих частиц от 1 до 3 мкм в диаметре. Ядрышки магнетита или гидратированного силиката встречаются в центре этих частиц.
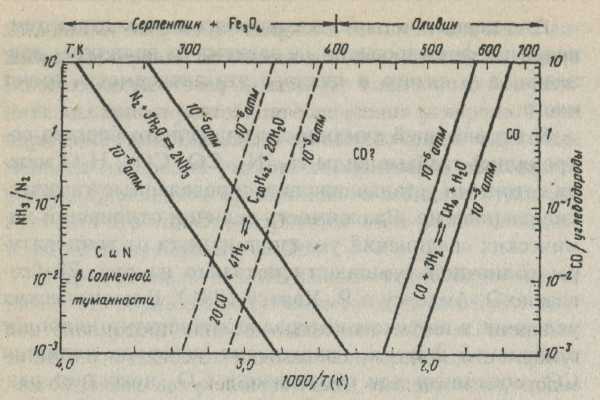
Рис. 20. Зависимость отношений химических соединений углерода и азота от температуры солнечной туманности. Сплошными линиями ограничены условия протекания соответствующих реакций, пунктирными - реакции типа Фишера - Тропша.
Отмеченные процессы синтеза органических веществ подтверждаются опытными данными. Эксперименты по моделированию реакций (типа Фишера - Тропша) в условиях близких к космическим показали, что когда СО, Н2, NH3 вступают в реакцию при температурах 400 - 770 К, в присутствии никеля, алюминия и глинистых минералов в качестве катализаторов, то среди продуктов реакций возникают многие органические вещества, включая аминокислоты.
В связи с обилием водорода в составе первичной туманности, который под влиянием солнечных лучей оказался отброшен в область формирования гигантских внешних планет, первоначально возникали продукты его взаимодействия с СО и азотом, согласно следующим реакциям:
2 Н2 + 2 СО ↔ СН4 + СО2
4 Н2 + СО2 ↔ СН4 + 2 Н2О
2 Н2:+ N2 ↔ 2 NH3-
Таким способом в отдельных зонах протопланетной туманности появлялись газовые смеси - сочетание водорода, метана, аммиака и молекул воды. В подобной газовой смеси могли происходить химические реакции синтеза с образованием органических соединений. Об этом косвенно свидетельствуют экспериментальные данные. Первые опыты по получению органических веществ в этой газовой смеси при пропускании через нее электрических разрядов были выполнены в 1953 г. по инициативе знаменитого американского химика Г. Юри его учеником С. Миллером. Позднее аналогичные результаты были получены и другими исследователями при воздействии на ту же газовую смесь ультрафиолетовых лучей и лучей от распада радиоактивных элементов. Реакции этого типа в газовой среде под действием ионизирующей радиации были названы реакциями Миллера - Юри. При этих реакциях возникали различные органические кислоты, такие как глутаминовая H2N-CH(C2H4COOH)-COOH и аспаргиновая H2N-CH(CH2COOH)-COOH. Однако роль солнечной радиации как источника ионизации, по всей вероятности была незначительной. Содержащая пыль протопланетная туманность была непрозрачной для ультрафиолетового света.
Однако в ранней Солнечной системе существовали мощные источники радиации, вызывающие фотохимические реакции. Это были рассеянные радиоактивные изотопы, находящиеся как в газовой, так и в твердой пылевой фазе первичной туманности. К ним принадлежали современные изотопы 235U, 238U, 40К, и изотопы вскоре вымершие (с периодами полураспада 1-80 млн. лет), которые показаны в таблице 17. Отсюда нетрудно заключить, что сама естественная радиоактивность, как наследство более древней эпохи синтеза нуклидов в виде α, β и γ излучений могла и должна была ионизировать окружающую среду, возбуждая многие химические реакции, в том числе синтез органических соединений. Таким образом, само вещество, законы сил, заложенных в атомах, включая свойства ядер и электронных оболочек, определили в исторической последовательности оптимальную обстановку для создания высокомолекулярных органических соединений. По-видимому, радиохимический синтез в древних космических системах органических веществ мог протекать при определенных дозах ионизирующей радиации. Радиоактивные излучения высокой интенсивности разрушают химические соединения. Поэтому следует думать, что при общем снижении радиационного фона в период распада вымерших и ныне существующих радиоактивных изотопов, был достигнут какой-то оптимум радиоактивного воздействия на исходные вещества, благоприятный для процессов синтеза органических соединений.
Частицы естественных катализаторов в солнечной туманности обладали первоначально также повышенной радиоактивностью, воздействуя на окружающую газовую среду. В целом синтез органических соединений в древних космических системах проходил как
под влиянием катализа, так и под действием радиоактивности.
Термодинамические условия формирования органических соединений в остывающей газовой туманности представлены на рис. 21 (по Р. Хаятсу и Э. Андерсу, 1981). На графике ограничены поля формирования материала углистых хондритовС1, С2, СЗ. Этот материал формировался при температуре ниже 400° К и был завершающим в химической эволюции солнечной туманности. Низкотемпературный материл туманности впоследствии участвовал в построении родоначальных метеоритных тел - астероидов и планет.
В настоящее время можно полагать, что синтез довольно сложных высокомолекулярных органических соединений, естественных предшественников живого вещества, был закономерным этапом в химической эволюции Солнечной системы в канун формирования планет. Возникшие в космических условиях органические вещества вошли в состав разных тел нашей системы, но лишь на Земле реализовались возможности прогрессивной эволюции, обеспечившие относительно быстрое возникновение саморегулирующих высокомолекулярных систем - непосредственных предков живых организмов. В родоначальных телах метеоритов и в кометах химическая эволюция оказалась замороженной.
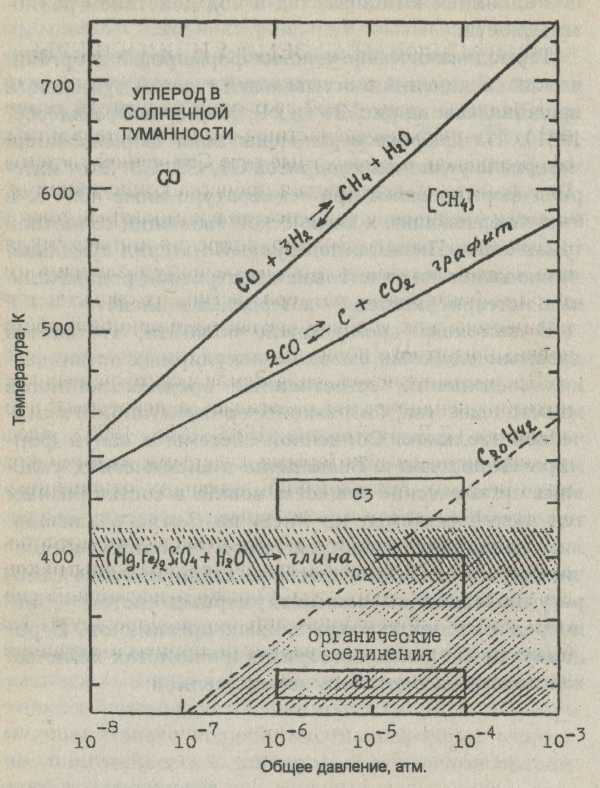
Рис. 21. Образование органических соединений в солнечной туманности по мере ее охлаждения по данным органической космохимии в зависимости от температуры и давления. Под глиной понимается сумма всех гидратированных силикатов.
ФОРМИРОВАНИЕ ЗЕМЛИ И БИОСФЕРЫ
Продукты химической эволюции солнечной туманности - минеральные частицы разного состава и газы сформировали все известные тела Солнечной системы. На каком-то этапе развития процесса конденсации началось объединение конденсатов в компактные тела - первичные планеты. Видимо, аккреция или аккумуляция материала происходила по-разному в зависимости от ряда факторов - размера частиц, их свойств, термодинамических условий среды, радиационной обстановки, магнитного поля.
Проблема происхождения Земли в свете данных космохимии неоднократно излагалась в некоторых публикациях (Г.В. Войткевич, 1983, 1988, 1996). Здесь мы ограничимся некоторыми главными итогами космохимических исследований, имеющих отношение к образованию Земли и биосферы.
Земля возникла путем аккреции вещества, представленного преимущественно высокотемпературными конденсатами солнечного газа. Однако относительно способа аккумуляции единого мнения не существует. Так было предложено два варианта процесса сгущения протопланетного материала.
1. Гомогенная аккумуляция - наиболее полно разработана О.Ю. Шмидтом и его сторонниками. Оболочечное строение Земля приобрела в дальнейшем при химической дифференциации, вызванной радиоактивным нагревом материала.
2. Гетерогенная аккумуляция определила с самого начала главные черты строения земного шара - образование в первичной Земле металлического ядра и мантии. При такой аккумуляции из металлических частиц сначала образовалось ядро. Затем на него осели более поздние конденсаты в виде силикатов, образовав мощную мантию первичной планеты.
Модели гетерогенной аккумуляции были предложены К. Таркяном, С. Кларком, А.П. Виноградовым, Г.В. Войткевичем, А.В. Макалкиным, Дж. Смитом, а также В.А. Рудником и Э.В. Соботовичем.
Согласно модели С. Кларка, К. Таркянаи Л. Гроссмана, образование Земли началось с накопления высокотемпературных конденсатов до железного этапа конденсации. На это первичное накопление осели металлические конденсаты. Затем последовало осаждение силикатных частиц, а завершилось формирование первичной планеты осаждением самых низкотемпературных конденсатов - гидратированных силикатов, воды и органических веществ. В общем последовательность аккумуляции повторяла последовательность конденсации в солнечной туманности (см. рис. 17).
В настоящее время мы имеем ряд аргументов космохимического и физического порядка в пользу гетерогенной аккумуляции (Г.В. Войткевич, 1988).
Образование первичной биосферы Земли, естественно, было связано с выделением на ее поверхности атмосферы, гидросферы, продуктов выветривания ювенильных пород и живого вещества.
Основные предпосылки появления жизни и биосферы на Земле возникли в конце остывания первичной газовой протопланетной туманности. На последних этапах остывания в результате радиохимических и каталитических реакций между биофильными элементами образовались многочисленные органические соединения, обусловившие появление ДНК и саморазвивающихся высокомолекулярных систем.
Самые поздние конденсаты солнечной туманности при объединении в компактные массы дали образование родоначальных тел углистых хондритов. Поэтому можно считать, что материал, завершивший построение первичной мантии нашей планеты, был аналогичным материалу углистых хондритов (С1).
Если допустить, что в период своего образования Земля получила в общей сложности ~ 1% материала типа углистых хондритов (С1), то нетрудно подсчитать, что она приобрела n Χ 1017 тонн органического вещества. Это огромное количество. Оно в 105 -106 раз превышает современную активную биомассу Земли. Огромное количество органического вещества земной коры в виде рассеянной органики, углей, горючих сланцев и нефтей возникло позже, в ходе фотосинтетической деятельности фотоавтотрофных организмов, используя углерод СО2 глубинного мантийного происхождения. В 1981 г. Дж. Брукс произвел расчеты, которые дали вероятное количество первичного органического вещества небиологического происхождения на Земле. 4,6 - 3,8 млрд. лет тому назад наша планета могла получить 0,2 Χ 108 тонн аминокислот, n Χ 107 т формальдегида и n Χ 1012 т органических полимеров за счет осаждения материала типа углистых хондритов.
Независимо от указанных количественных расчетов, можно полагать, что верхняя зона первичной мантии планеты, сложенная силикатами, гидросиликатами, оказалась обогащенной органическими веществами абиогенного происхождения, водой в разных формах и природными газами. При радиогенном нагреве произошла дегидратация, дегазация этой зоны в форме вулканических проявлений. Летучие продукты этих извержений при охлаждении образовали на поверхности планеты первичные океаны, первичную атмосферу, обогащенную СО2, Н2, N2. Одновременно происходил вынос в первичный океан органического вещества, растворенного в ювенильных водах, или адсорбированных на поверхности минеральных частиц.
Первичная газово-водная оболочка ранней Земли превратилась в подлинную биосферу лишь тогда, когда в ней появились живые организмы, использующие воду, газы и органические вещества для своего питания. В свете современных геохимических и космохимических данных несомненно, что жизнь на Земле очень древняя и ее начало связано с образованием самой Земли. Уже давно возникло убеждение в том, что жизнь на нашей планете существует столько времени, сколько существует и сама Земля. Не исключена возможность, что химическая эволюция протопланетной туманности завершилась образованием молекул ДНК. Однако реализация ее функций оказалась возможной лишь в пределах ранней Земли, в самых ранних водоемах. При весьма раннем возникновении живого вещества сформировалась ранняя биосфера как сочетание благоприятных условий для биокосных систем и с ними связанных систем биологических при умеренных температурах, позволяющих существование жидкой поды. Во всяком случае данные космохимии указывают, что в период своего образования наша планета получила достаточно полный набор сложных органических соединений, чтобы путем полимеризации аминокислот, сложных углеводородов и других соединений возникли саморегулирующиеся высокомолекулярные системы, характерные для живого вещества. Период химической эволюции в пределах Земли был в общем довольно коротким. Он начался еще в космических условиях и продолжался на Земле, когда радиоактивность материала была еще достаточно высокой. По существу, возникновение Земли, жизни и биосферы было единым процессом. Возникновение жизни и биосферы в основном можно представить себе как синхронное событие в ранней истории планеты.
