- •Анаболическая – предшественники биологически активных соединений (гормоны, нуклеотиды, гем, креатин, карнитин, фосфолипиды, нейромедиаторы и др.)
- •Энергетическая – источники энергии в экстремальных условиях (длительное голодание, избыточное потребление белков с пищей).
- •Пищевая ценность белков
- •Полноценные – белки, в которых содержатся все незаменимые и частично заменимые аминокислоты.
- •Неполноценные – белки, в которых нет хотя бы одной незаменимой аминокислоты.
- •Переваривание белков
- •Эндопептидазы расщепляют пептидные связи, удаленные от концов пептидной цепи (пепсин, трипсин, химотрипсин, эластаза)
- •Экзопептидазы действуют на пептидные связи, образованные n-концевыми (аминопептидаза) и с-концевыми (карбоксипептидазы а и в) остатками аминокислот
- •Переваривание белков в желудке:
- •Переваривание белков в кишечнике:
- •Трансаминирование аминокислот
- •Дезаминирование аминокислот
- •Трансаминирование аминокислоты с
- •Прямое окислительное дезаминирование глутамата:
Полноценные – белки, в которых содержатся все незаменимые и частично заменимые аминокислоты.
(Многие животные белки: белки мяса, яичный альбумин, казеин молока)
Неполноценные – белки, в которых нет хотя бы одной незаменимой аминокислоты.
(В основном, растительные белки, в которых редко встречаются: Мет, Лиз, Три, Тре)
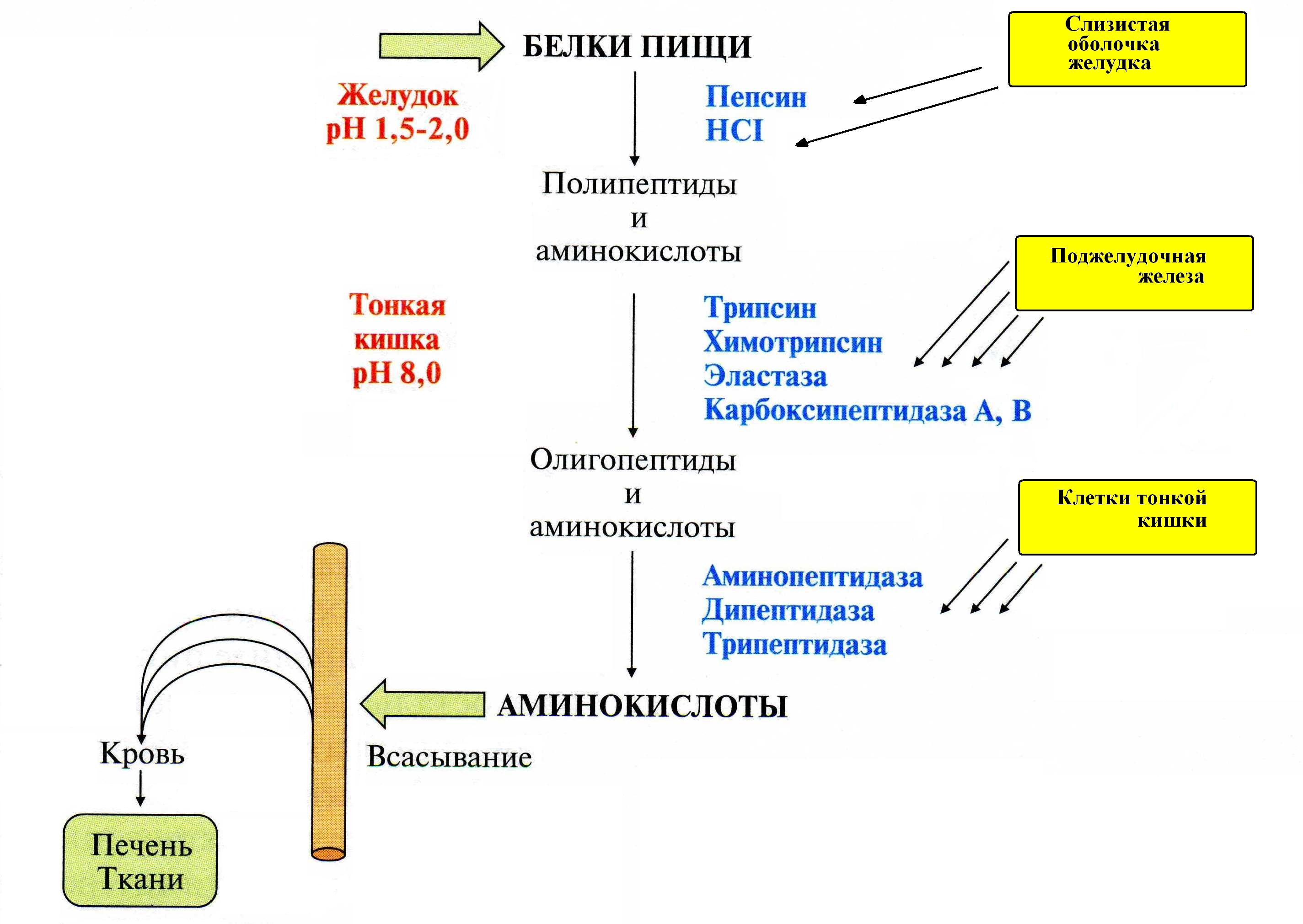
Переваривание белков
В пище очень мало свободных аминокислот, поэтому, они поступают в ЖКТ в составе белков.
В ходе переваривания белков в ЖКТ образуются свободные аминок-ты.
Переваривание белков начинается в полости желудка и продолжается в тонкой кишке.
Реакции расщепления пептидных связей катализируют ферменты пептидгидролазы (пептидазы).
Они синтезируются в клетках желудка, поджелудочной железы и тонкой кишки.
Пептидазы обладают относительной субстратной специфичностью, но преимущественно гидролизуют пептидные связи, образованные определенными аминокислотами.
Все пептидазы делятся на 2 группы в зависимости от места расположения в пептиде гидролизуемой связи:

Эндопептидазы расщепляют пептидные связи, удаленные от концов пептидной цепи (пепсин, трипсин, химотрипсин, эластаза)
Экзопептидазы действуют на пептидные связи, образованные n-концевыми (аминопептидаза) и с-концевыми (карбоксипептидазы а и в) остатками аминокислот
Пептидазы, которые действуют в желудке и полости кишечника синтезируются в секреторных клетках в неактивной форме в виде проферментов.
Проферменты выделяются к месту действия в просвет желудка или кишечника, где активируются путем частичного протеолиза.
Такой механизм активации протеолитических ферментов защищает секреторные клетки желудка и поджелудочной железы от самопереваривания.
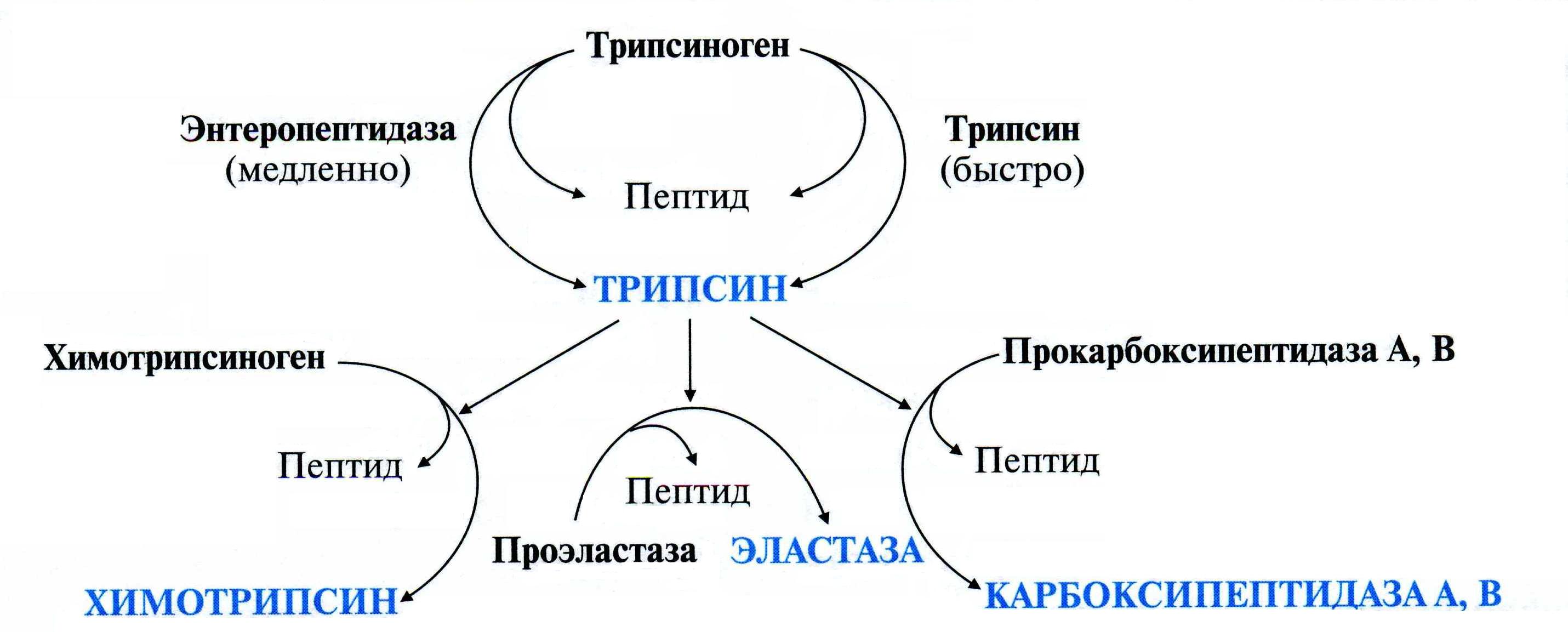
Частичный протеолиз:

Энтеропептидаза
Переваривание белков в желудке:
Происходит при участии фермента пепсина:
Профермент пепсиноген синтезируется желудочными железами и при поступлении пищи секретируется в полость желудка.
В желудочном соке пепсиноген превращается в активный фермент пепсин путем частичного протеолиза.
В пищевых белках пепсин гидролизует связи, образованные аминогруппой ароматических аминокислот Фен и Тир, а также Глу и Асп с любой другой аминокислотой
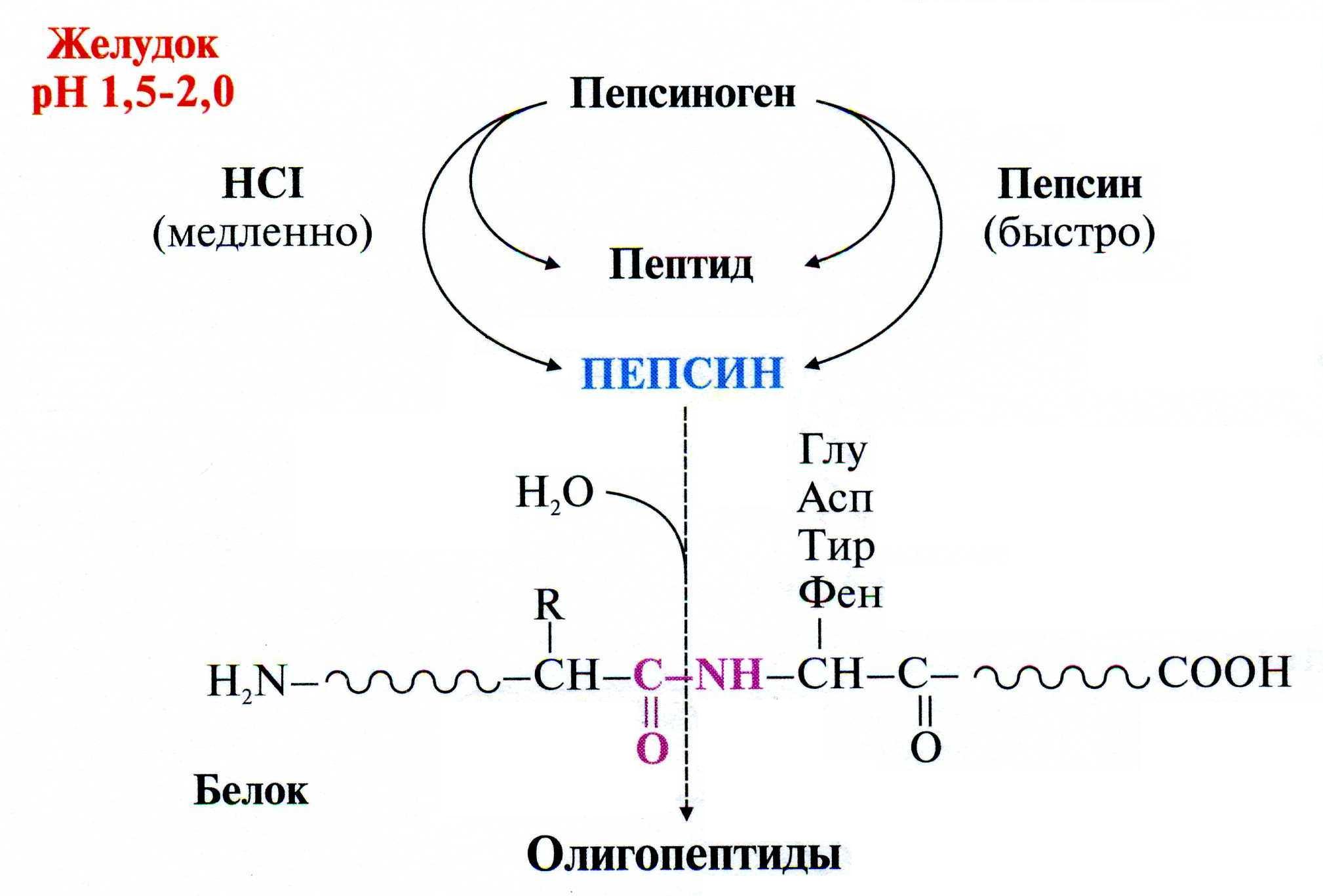
Олигопептиды, которые образовались в результате действия пепсина в желудке, поступают в тонкую кишку.
Переваривание белков в кишечнике:
! В тонкой кишке происходит бóльшая часть работы по перевариванию белков.
Содержимое желудка (химус) поступает в полость 12-перстной кишки.
В полости 12-перстной кишки на олигопептиды действует набор панкреатических пептидаз.
Ферменты – панкреатические пептидазы: трипсин, химотрипсин, эластаза, карбоксипептидазы А и В синтезируются в клетках поджелудочной железы в виде неактивных проферментов.
Основная панкреатическая пептидаза – трипсин.

Набор активных ферментов: трипсин, химотрипсин, эластаза, карбоксипептидазы А и В работают в полости 12-перстной кишки.
В результате совместного действия этого набора ферментов образуются ди- и трипептиды, аминокислоты и небольшое кол-во коротких пептидов (олигопептидов).
Завершающий этап переваривания – гидролиз небольших пептидов до свободных аминокислот происходит в пристеночном слое либо уже в клетках кишечника после их всасывания.
! Ферменты завершающего этапа: аминопептидаза, дипептидаза, трипептидаза синтезируются в клетках тонкой кишки сразу в активной форме.
Это связано с тем, что эти ферменты действуют только на короткие пептиды, не оказывая никакого влияния на белки и не опасны для белков кишечника.
Аминопептидаза отщепляет N-концевые остатки аминокислот от олигопептидов.
Ди- и трипептидазы, расщепляют ди- и трипептиды до свободных аминокислот.
Образовавшиеся свободные аминокислоты поступают в кровь воротной вены, затем в клетки печени и затем в другие ткани.
В тканях аминокислоты используются для синтеза белков и различных биологически активных в-в или вступают в реакции катаболизма.