
6. Хіміко-фізичні методи
До хіміко-фізичних методів очищення речовини відносяться методи, засновані на використанні гомогенних чи гетерогенних хімічних реакцій, що приводять до утворення мікродомішками таких стійких сполук чи простих речовин, що надалі можуть бути вилучені з основної речовини будь-яким придатним фізичним способом.
У технології одержання особливо чистих неорганічних речовин чисто хімічні методи самостійно не використовуються, а майже завжди сполучаються з тими чи іншими фізичними способами видалення нових хімічних форм мікродомішок з основної речовини чи її розчинів: фільтрування нерозчинних опадів і аерозолей, витяг з розчинів хелатів чи іонних асоціатів придатним сорбентом чи екстрагентом; ректифікація основного компонента із системи, що містить поділяючий агент і т.д.
Серед хіміко-фізичних методів очищення речовини найбільш відомі методи вибіркового окислювання чи відновлення мікродомішок (у тому числі методи термічної дисоціації домішкових сполук), гідридний метод, метод амальгамного обміну і виділення макрокомпонентів у газоподібному стані при взаємодії речовини з реагентом у рідкій фазі); осадження і співосадження мікродомішок з газоподібних середовищ і розчинів у виді практично нерозчинних твердих фаз; вибіркового галогенування; вибіркового комплексоутворення в розчинах. До числа хіміко-фізичних методів відноситься також метод хімічних транспортних реакцій.
Вибіркове комплексоутворення в розчинах
Серед хіміко-фізичних методів очищення речовини спосіб зв'язування мікродомішок у розчині в міцні комплексні сполуки, що вилучаються потім із середовища яким-небудь способом, одержав досить велике поширення.
Серед хелатоутворюючих реагентів найбільше застосування в комплексо-адсорбційному способі одержали діетилдитіокарбамат натрію і купферон.
Діетилдитіокарбамат натрію
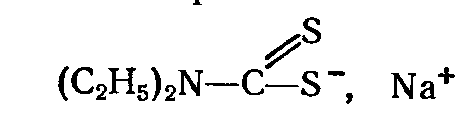
утворює з багатьма катіонами комплексні сполуки з чотиричленними циклами виду:
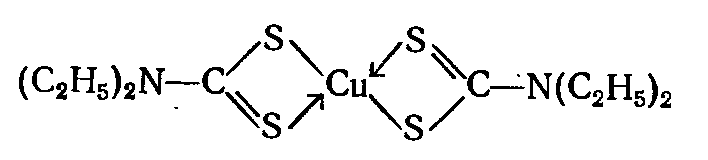
Діетилдитіокарбамат натрію використовується для очищення водних розчинів хлоридів літію, натрію, калію, магнію, кальцію і барію, броміду калію, сульфатів цинку і кадмію, молібдатц і вольфрамату амонію. Умови утворення і стійкість діетилдитіокарбаматів металів аналогічні сульфідам тих же металів. Залишковий вміст таких мікродомішок як Fe+, Hg, Cu2+, Bi, As, Ni і інших після видалення комплексних сполук з розчину не перевищує 5·10-7 – 1·10-5% стосовно сольової частини рідкої фази.
Інший хелатоутворюючий реагент, придатний для видалення багатьох мікродомішок з кислих (рН=2-5) водних розчинів солей лужних металів і деяких органічних кислот – купферон,
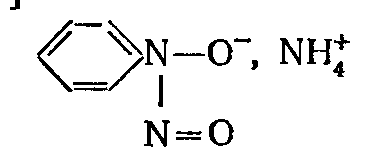
який утворює комплексні сполуки з п’ятичленними циклами:
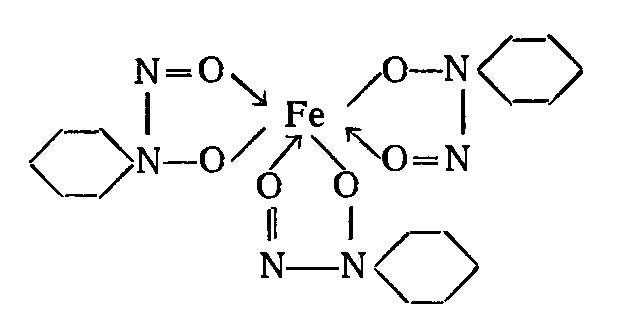
Купферон використовується для очищення водних розчинів йодидів і дигідроортофосфатів лужних металів і амонію від мікродомішок Fe3+, Cu2+, Pb і інших домішок до 1·10-6% і менше.
Навіть з концентрованих (400-600 г/л) водних розчинів винної кислоти купферон дозволяє витягти багато мікродомішок.
Для глибокого очищення речовин від великої групи мікро-домішок застосовується послідовне введення в розчин різних хелатоутворюючих реагентів, після чого суміш обробляється активним вугіллям.
Вибіркове комплексоутворення можливе і з застосуванням неорганічних лігандів. Водні розчини солей хрому (20-60 г/л Сг3+) за допомогою K4[Fe(CN)6] і активного вугілля марки ОУ можна очистити від домішки Fe3+ 5-10-4% і менше. Гірше віддаляються домішки міді, нікелю, олова і свинцю.
Спосіб вибіркового комплексоутворення в розчинах має необмежені можливості через велику розмаїтість груп, що координуються, які можна використовувати для зв'язування іонів мікродомішок, що підлягають видаленню з основної речовини. Лігандами в даному випадку можуть бути дуже численні неорганічні й органічні іони чи молекули. Однак найбільш перспективними є такі ліганди, що утворюють з іонами мікродомішок (в основному з іонами металів) гетероциклічні сполуки (хелати). Однією з найбільш чудових властивостей циклічних сполук є їхня надзвичайна стійкість («циклічний ефект»). Помічено, що комплексна сполука стає більш міцною зі збільшенням числа груп у ліганді, здатних до координації, однак при двох і більш приєднуючих лігандах може відбуватися взаємодія груп, які координуюють, що приводить до перекручування кутів зв'язку і зменшенню міцності комплексної сполуки.
Особливий практичний інтерес представляють комплексні сполуки, що легко і цілком сорбуються з розчинів на активних вугіллях і інших сорбентах.
Три фактори визначають кратність очищення розчинів основного компонента від мікродомішок комплексоадсорбційним способом: стійкість комплексної частинки (іона, молекули), ступінь її адсорбції і розчинність сорбенту в оброблюваному розчині.
