
Уфимский государственный нефтяной технический университет
Кафедра «Общая и аналитическая химия»
Дисциплина «Общая и неорганическая химия»
ОТЧЕТ
по лабораторной работе №10,11
На тему: «Химические свойства металлов iiia и iva – подгрупп
(Al, Sn, Pb)»
Выполнил
студент группы__________ ______________ Фамилия И.О.
(Подпись, дата)
Принял
доцент кафедры ОАХ ______________ Чалова О.Б.
(Подпись, дата)
Цель работы:
- Изучить свойства металлов IIIA и IVA- подгрупп;
- Изучить свойства характеристичных соединений металлов IIIA и IVA- подгрупп;
Краткая теория.
1. Положение элементов в периодической системе, свойства атомов
Электронные конфигурации атомов, валентные электроны
IIIA- подгруппа:
IVA- подгруппа:
Степени окисления: IIIA- подгруппа ……………..IVA- подгруппа …….
2. Свойства простых веществ – металлов:
- положение в «ряду стандартных окислительно-восстановительных (электродных) потенциалов металлов»
φ(Men+/Me) =
- активность металлов:
Составьте уравнения реакций:
- взаимодействие с кислородом:
а) Al б) Sn
в) Pb
- взаимодействие с галогенами (хлором):
а) Al б) Sn в) Pb
- взаимодействие с серой:
а) Al
- взаимодействие с водными растворами кислот, окисляющими H+ (HF, HCl, HBr, HI, разбавленной H2SO4, H3PO4, RCOOH и другими):
а) Al + HBr → б) Sn + RCOOH →
- Металлы IIIA – подгруппы не взаимодействует с водой, так как …………………………………, но легко вытесняют водород из водного раствора щелочи
Al + NaOH + H2O →
- взаимодействие с концентрированной H2SO4:
а) Sn + H2SO4(конц) → ………….+ S + H2O
- взаимодействие с разбавленной и концентрированной HNO3:
а) Pb + HNO3(разб) → ………….+ NО + H2O
б) Sn + HNO3(конц) → H2SnO3 + NO2 + H2O
3. Свойства оксидов и гидроксидов металлов IIIA и IVA- подгрупп:
- формулы оксидов металлов IIIA …………и IVA- подгрупп……………….
- формулы гидроксидов металлов IIIA ……………..и IVA- подгрупп……………
- растворимость, взаимодействие с водой оксидов и гидроксидов металлов IIIA и IVA- подгрупп
- диссоциация в водном растворе гидроксидов металлов IIIA и IVA- подгрупп (на примере гидроксида олова (II)):
[Sn(OH)4]2-
+ 2H+
![]() 2 H2O
+ Sn(OH)2
Sn2+
+ 2OH-
2 H2O
+ Sn(OH)2
Sn2+
+ 2OH-
Оксиды и гидроксиды металлов IIIA и IVA- подгрупп проявляют ………………………… свойства
- взаимодействие оксидов и гидроксидов металлов IIIA и IVA- подгрупп с кислотами и кислотными оксидами.
а) Al2О3 + H2SO4 →
б) Pb(OH)2 + H2SO4 →
- взаимодействие оксидов и гидроксидов металлов IIIA и IVA- подгрупп с основаниями при сплавлении происходит с образованием простых солей и воды
PbO + NaOH → Na2PbO2 + H2O
Pb(OH)2 + NaOH → Na2PbO2 + H2O
- взаимодействие оксидов и гидроксидов металлов IIIA и IVA- подгрупп с водными растворами щелочей происходит с образованием комплексных солей
Al2О3 + NaOH + H2O → Na[Al(OH)4]
Al(OH)3 + NaOH → Na[Al(OH)4]
Pb(OH)2 + NaOH →
4. Окислительно-восстановительные свойства соединений металлов IIIA и IVA-подгрупп
Соединения алюминия ……………….окислительно-восстановительных свойств, так как …………
Используя значения ОВП, приведенных на диаграммах Латимера, охарактеризовать окислительно-восстановительные свойства соединений олова.
Диаграммы Латимера:
а) для олова;
-0,118

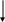 SnO2
SnO2
+0,154 -0,141
 Sn4+
Sn2+
Sn0
Sn4+
Sn2+
Sn0
 -0,96
-0,79
-0,96
-0,79
 [Sn(OH)6]2-
[Sn(OH)6]4-
[Sn(OH)6]2-
[Sn(OH)6]4-
Используя значения ОВП, приведенных на диаграммах Латимера, охарактеризовать окислительно-восстановительные свойства соединений свинца.
Диаграммы Латимера:
б) для свинца: -0,956

 PbS
PbS
1,685 -0,356


 PbSO4
PbSO4
1,456 - 0,126

 PbO2
Pb2+
Pb0
PbO2
Pb2+
Pb0
0,305 -0,538

 [Pb(ОН)6]2-
[Pb(OH)4]2-
[Pb(ОН)6]2-
[Pb(OH)4]2-
ВНИМАНИЕ! Все соединения свинца ядовиты! При работе с ними соблюдать особую осторожность! По окончании опытов с кислотами растворы слить в слив, а не растворившиеся металлы положить в специальную посуду!
Опыт 1. Взаимодействие «амальгамированного» алюминия с водой
В пробирку с 5 мл дистиллированной воды поместить обычную алюминиевую проволоку и оставить для сравнения до окончания опыта. В две пробирки налить по 3-5 мл раствора соли ртути(II) и опустить в каждую металлическую алюминиевую проволоку, выдержать в течение 5 минут. После чего проволочки протереть кусочком фильтровальной бумаги, и одну из них оставить на воздухе, а вторую поместить в пробирку с дистиллированной водой. Наблюдать за изменениями в пробирках и на поверхности проволоки, оставшейся на воздухе, в течение 5-10 минут.
- Отметить, происходят ли изменения в с обычной алюминиевой проволокой в воде
- в обычных условиях алюминий не взаимодействует с водой, потому что…………………
- отметить, как изменилась поверхность алюминиевой проволоки после обработки солью ртути………..
- составить уравнения реакций, протекающих в растворе соли ртути
Hg(NO3)2 + H2O →
- составить уравнения реакций, протекающих в растворе соли ртути на поверхности алюминиевой проволоки:
Al2O3 + HNO3 →
Al + Hg(NO3)2 →
- объяснить, может ли образоваться на поверхности «амальгамированного» алюминия защитная оксидная пленка……….
- отметить, что образуется на поверхности «амальгамированного» алюминия на воздухе…..
- составить уравнение реакции окисления алюминия на воздухе:
Al + O2 →
- отметить, какие изменения происходят в пробирке с «амальгамированной» алюминиевой проволокой в воде
- составить уравнение реакции между «амальгамированным» алюминием и водой:
Al + H2O →
- ответить, пассивирован ли «амальгамированный» алюминий.
Опыт 2. Взаимодействие «амфотерных» металлов (Al, Sn, Pb) с водным раствором щелочи
Налить в три пробирки по 1-2 мл концентрированного раствора щелочи - гидроксида натрия - и поместить в каждую из пробирок один из металлов (в первую - алюминиевую стружку, во вторую - гранулу олова, в третью - гранулу свинца). Пробирки осторожно нагреть на спиртовке.
- Отметить, как протекает реакция металлических Al, Sn и Pb с водным раствором щелочи
- растворы каких веществ называют щелочами, привести примеры………
- сравнить активность металлических Al, Sn и Pb по отношению к водному раствору щелочи
- ответить, чем покрыт каждый из металлов
- составить уравнения реакций растворения оксидных пленок металлов в растворе гидроксида натрия, учитывая, что образуются гидроксокомплексы:
Al2O3 + NaOH + H2O
SnO2 + NaOH + H2O
PbO + NaOH + H2O
- составить уравнения реакций металлов с раствором гидроксида натрия, учитывая, что образуются соответствующие гидроксокомплексы с координационным числом равным четырем:
1). Al + NaOH + H2O
2). Sn + NaOH + H2O
3). Pb + NaOH + H2O
- указать восстановители………………….. и окислитель……….
- ответить, какой газ выделяется…………….
- выписать (таблица) значения стандартных окислительно-восстановительных потенциалов электрохимических систем
Me +
4OH-
-
ne
![]() [Me(OH)4]n-4:
[Me(OH)4]n-4:
![]() …;
…;
![]() …;
…;
![]() …
.;
…
.;
- сравнить их значения с соответствующими потенциалами для процессов окисления в кислой среде:
![]() …
…
![]() …
…
![]() …
…
- ответить, в какой среде более выражены восстановительные свойства металлических Al, Sn и Pb…………………..
- рассчитать
потенциал «водородного электрода»
![]() =
=
при рН=14;
- рассчитать ЭДС реакций: ЭДС = φок . – φвос.
1).
2).
3).
- вывод.
Опыт 3. Взаимодействие металлов (Al, Sn, Pb) с концентрированной серной кислотой (показательный)
Налить в три пробирки по 1-2 мл концентрированного раствора серной кислоты и поместить в каждую из пробирок один из металлов (в первую - алюминиевую стружку, во вторую - гранулу олова, в третью - гранулу свинца). Подержать над отверстием пробирок фильтровальную бумагу, смоченную раствором соли свинца (II). Наблюдать за изменениями в пробирках в течение 2-3 минут. Пробирки осторожно нагреть на спиртовке.
- отметить, какие изменения происходят в пробирках при комнатной температуре…….
при нагревании……….
- ответить, какой элемент является окислителем в концентрированной серной кислоте….
- до каких продуктов может восстанавливаться концентрированная серная кислота
- ответить, что образуется при окислении металлического алюминия………….,
…………….. олова……………..………………, свинца……………………..
- составить уравнения первой реакции, учитывая, что первоначально выделяющийся газ – SO2:
Al + H2SO4(конц.) SO2 + … +
Sn + H2SO4(конц.) SO2 + … +
Pb + H2SO4(конц.) SO2 + … +
- составить уравнение второй реакции, учитывая, что образующийся белый осадок - S:
Al + H2SO4(конц.) S + ……...... +
Sn + H2SO4(конц.) S + ………. +
Pb + H2SO4(конц.) S + ………. +
- составить уравнение третьей реакции, учитывая, что выделяющийся газ с характерным запахом – H2S:
Al + H2SO4(конц.) H2S + … +
- составить уравнение реакции, протекающей на фильтровальной бумаге и доказывающей образование сероводорода:
H2S + Pb(NO3)2
- ответить, реакция металлов с концентрированной серной кислотой является селективной или нет……………………….
- ответить, в каких условиях алюминий «пассивируется» концентрированной серной кислотой……….
- вывод.
Опыт 4. Взаимодействие металлов (Al, Sn, Pb) с разбавленной азотной кислотой (показательный)
В три пробирки налить по 2-3 мл разбавленной азотной кислоты. Осторожно опустить в первую пробирку стружку алюминия, во вторую – гранулу олова, в третью – свинца. Если реакция идет слабо, слегка нагреть пробирки.
- отметить, какие изменения происходят в каждой из пробирок, с каким металлом реакция идет наиболее энергично;
- составить уравнения возможных реакций с разбавленной азотной кислотой, учитывая, что образуются соли нитраты металлов, вода и продукт восстановления азота (V)
Al + HNO3(разб.) → NO + ……….… + …………..
Al + HNO3(разб.) → NH4NO3 + ……………. +
- составить уравнения реакции олова с разбавленной азотной кислотой
Sn + HNO3(разб.) →
- составить уравнения реакции свинца с разбавленной азотной кислотой, учитывая, что образуются нитрат свинца (II), вода и оксид азота (II):
Pb + HNO3(разб.) →
- вывод
Опыт 5. Взаимодействие алюминия - А1- с концентрированной азотной кислотой (показательный)
В две пробирки налить по 1 мл концентрированной азотной кислоты и опустить в первую - алюминиевую проволоку, во вторую - гранулу или стружку алюминия. Наблюдать за изменениями в пробирках в течение 2 минут. Вынуть проволоку из раствора азотной кислоты и опустить в пробирку с раствором сульфата меди (II), наблюдать 2 минуты, после чего добавить 5-6 капель раствора хлорида натрия и наблюдать за изменениями. Пробирку с алюминиевой стружкой (или гранулой) в растворе азотной кислоты осторожно нагреть на спиртовке.
- Отметить, какие изменения происходят в каждой из пробирок при комнатной температуре……..
при нагревании………..
- ответить, почему при комнатной температуре реакция активного металла алюминия с концентрированной азотной кислотой не идет…..
- ответить, возможно, ли окисление алюминия ионами Cu2+
- составить уравнение реакции алюминия с сульфатом меди (II), рассчитать ЭДС реакции: ЭДС = φок . – φвос.
Al + CuSO4
- объяснить, почему после действия концентрированного раствора азотной кислоты, алюминий не взаимодействует с раствором сульфата меди (П)
- отметить, наблюдается ли выделение меди на алюминиевой проволоке из раствора сульфата меди (II) до и после добавления хлорида натрия
- объяснить, какова роль хлорида натрия в реакции алюминия с раствором сульфата меди (П)
- составить уравнение реакции алюминия с концентрированной азотной кислотой, протекающей при нагревании с образованием нитрата алюминия (III), воды и оксида азота (IV):
Al + HNO3(конц.) NO2 + … + …;
- вывод.
Опыт 6. Взаимодействие металлов (Sn, Pb) с концентрированной азотной кислотой (показательный)
В две пробирки налить по ~1 мл концентрированной азотной кислоты. Осторожно опустить в первую пробирку гранулу олова, во вторую - свинца. Наблюдать за изменениями в пробирках в течение ~2 минут. Пробирки нагреть.
- отметить, какие изменения происходят в каждой из пробирок при комнатной температуре………..
при нагревании………….
- ответить с каким металлом при комнатной температуре реакция идет наиболее энергично…………………..
- составить уравнение реакции олова с концентрированной азотной кислотой, протекающей при нагревании с образованием метаоловянной кислоты, воды и оксида азота (IV):
Sn + HNO3(конц.) NO2 + … +
- составить уравнение реакции свинца с концентрированной азотной кислотой, протекающей при нагревании с образованием нитрата свинца (II), воды и оксида азота (IV):
Pb + HNO3(конц.) NO2 + … + …
- вывод.
Опыт 7. Получение и свойства гидроксида алюминия
В две пробирки внести по 2 капли раствора соли сульфата алюминия и 2 н раствора гидроксида аммония до образования осадка. В первую пробирку к осадку гидроксида алюминия добавить избыток раствора соляной кислоты, во вторую пробирку – избыток раствора гидроксида натрия.
- Охарактеризовать внешний вид осадка гидроксида алюминия
- составить уравнение реакции образования гидроксида алюминия в молекулярной и ионной форме:
Al2(SO4)3 + NH4OH → …
- отметить, какие изменения происходят с осадком гидроксида алюминия при добавлении избытка соляной кислоты и избытка гидроксида натрия……………………….
- составить уравнение реакции взаимодействия гидроксида алюминия с соляной кислотой в молекулярной и ионной форме:
Al(OH)3 + HCl →
- составить уравнение реакции взаимодействия гидроксида алюминия с избытком гидроксида натрия:
Al(OH)3 + NaOH →
- ответить, какие кислотно-основные свойства проявляет гидроксид алюминия.
- составить уравнение диссоциации гидроксида алюминия
- равновесие диссоциации гидроксида алюминия при добавлении избытка кислоты смещается…………….. при добавлении избытка щелочи смещается…………….
- вывод
Опыт 8. Амфотерные свойства гидроксидов олова(II) и свинца(II)
Налить в две пробирки по две капли раствора SnCl2, в другие две - по две капли раствора Pb(NO3)2. Затем в каждую пробирку прибавить по несколько капель раствора аммиака до выпадения осадков. К выпавшим осадкам добавить в первую пробирку раствор HNO3 и во вторую - раствор NaOH.
- Охарактеризовать внешний вид осадка гидроксида олова(II) ………………, гидроксида свинца(II) …………………..
- составить уравнение реакции образования гидроксида олова(II) и гидроксида свинца(II) в молекулярной и ионной форме:
SnCl2 + NH4OH →
Pb(NO3)2 + NH4OH →
- отметить, какие изменения происходят с осадками гидроксидов при добавлении избытка соляной кислоты ………………и избытка гидроксида натрия………………………
- составить уравнение реакции взаимодействия гидроксида олова(II) и гидроксида свинца(II) с соляной кислотой в молекулярной и ионной форме:
Sn(OH)2 + HCl →
Pb(OH)2 + HCl →
- составить уравнение реакции взаимодействия гидроксида алюминия с избытком гидроксида натрия:
Sn(OH)2 + NaOH →
Pb(OH)2 + NaOH →
- ответить, какие кислотно-основные свойства проявляет гидроксид олова(II) и гидроксид свинца(II)……………………………..
Опыт 9. Окислительные свойства соединений свинца (IV)
В пробирку поместить одну ложечку порошка PbO2 и 10 капель концентрированного раствора NaOH. Пробирку нагреть на спиртовке. В горячий раствор внести 2 капли раствора Cr2(SO4)3 и снова нагреть пробирку. Отметить появление желтой окраски раствора, характерной для иона CrО42- . Написать уравнение реакции.
- отметить, какие изменения происходят в пробирке при нагревании………….
- составить уравнение реакции, учитывая, что образуется хромат натрия и тетрагидросоплюмбат(II) натрия
PbO2 + NaOH + Cr2(SO4)3 → Na2CrО4 + Na2[Pb(OH)4]
- как изменилась степень окисления свинца………………хрома…………………
- какие свойства проявляет оксид свинца (IV)
- Вывод
Опыт 10. Восстановительные свойства соединений олова (II)
К 1-2 каплям раствора хлорида олова SnCl2 прилить по каплям раствор щелочи до растворения первоначально образовавшегося осадка. К полученному раствору тетрагидроксостанната(II) натрия прилить 2-3 капли раствора соли висмута (Bi(NO3)3), перемешать.
- отметить, какие изменения происходят в пробирке ………….
- составить уравнение реакции, учитывая, что сначала образуется белый осадок Bi(OH)3, затем он чернеет, восстанавливаясь до металлического висмута; олово(II) при этом превращается в гексагидроксостаннат(IV) натрия
SnCl2 + NaOH + Bi(NO3)3 → Bi + Na2[Sn(OH)6] +…
- как изменилась степень окисления олова…………………висмута…………………
- какие свойства проявляет олово(II)
- вывод
