
Портрет уксусной кислоты
Под звуки музыки раскладывается календарь – листы с большими рисунками по следующему ниже тексту.
Из всех кислот
Она, конечно, прима,
Присутствует везде
И зримо, и незримо.
В животных и растениях есть она,
С ней техника и медицина навсегда.
Ее потомство – ацетаты –
Очень нужные «ребята».
Всем известный аспирин.
Он, как добрый господин,
Жар больного понижает
И здоровье возвращает.
Это – меди ацетат.
Он растеньям друг и брат,
Убивает их врагов.
От кислоты еще есть толк –
Нас одевает в ацетатный шелк.
А пельмени любит кто,
Знает уксус тот давно.
Есть еще вопрос кино:
Хорошо всем надо знать,
Что без пленки ацетатной нам кино не увидать.
Конечно, есть и другие применения,
И вам они известны, без сомнения.
Но главное, что сказано, друзья,
«Хлеб промышленности» уксусная кислота.
Ведущий. Итак, остался последний товар, причем такой, о котором, может быть, многие знают очень мало. Слово для представления своего товара имеет фирма «СПК», ее интерес – стеариновая и пальмитиновая кислоты.
Директор. Думаю, мало кому известны стеариновая и пальмитиновая кислоты. Так будьте внимательны! Среди высших предельных одноатомных карбоновых кислот имеются:
СН3(СН2)14СООН, или С15Н31СООН – пальмитиновая кислота,
СН3(СН2)16СООН, или С17Н35СООН – стеариновая кислота.
Эти кислоты в виде сложных зфиров входят в состав жиров, поэтому их называют высшими жирными кислотами.
Мишель Эжен Шеврель совместно с А.Браконно установил, что большинство жиров состоит из стеарина и олеина, выделил стеариновую и пальмитиновую кислоты.
Пальмитиновая кислота – наиболее распространенная в природе жирная кислота, входит в состав глицеридов большинства животных жиров и растительных масел (например, пальмовое масло содержит 39–47% пальмитиновой кислоты), а также в состав некоторых восков.
Отдел рекламы (демонстрирует кислоты).
Две вот эти кислоты,
Словно сестры-близнецы,
Вместе как они похожи,
И тверды, и белокожи.
Итак, это твердые вещества, белого цвета, нерастворимы в воде, умеренно растворимы в спирте, эфире, хлороформе и других органических растворителях. Температура плавления стеариновой кислоты +69,3 °С, температура кипения от 360 до 370 °С.
1-й специалист-химик. Химические свойства жирных кислот имеют свои особенности. Окраска водных растворов индикаторов не изменяется при добавлении порошков пальмитиновой и стеариновой кислот.
Эти кислоты растворяются в водных растворах едких щелочей и карбонатов, образуя соли:
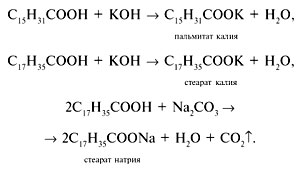
Есть вещества, которые являются спутниками человека всю жизнь. К таким веществам относится мыло. Вспомним с детства знакомые строки:
«Да здравствует мыло душистое
И полотенце пушистое!»
Натриевые и калиевые соли высших жирных кислот называют мылами. Они хорошо растворяются в воде, обладают моющим действием и составляют основу жидкого мыла (калиевые соли) и твердого мыла (натриевые соли). Водные растворы мыла имеют щелочную реакцию, т. к. соли подвергаются гидролизу.
Демонстрационный опыт. В стакане на 50 мл воды растворить 19 г ацетата натрия CH3COONa и добавить 0,5 мл спиртового раствора фенолфталеина. Раствор останется бесцветным. Затем нагреть на водяной бане. После закипания воды появляется малиновое окрашивание. Равновесие сдвигается вправо, среда раствора становится щелочной.
Уравнения реакций гидролиза:
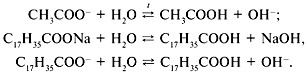
1-й специалист-химик. Соли жирных кислот, в состав которых входят Ca, Mg, а также тяжелые металлы, в воде нерастворимы. Поэтому моющая способность мыла утрачивается:
2С17Н35СООNa + CaCl2
![]()
(С17Н35СОО)2Ca
![]()
+ 2NaCl.
Cтеарат-ионы С17Н35СОО–, образующие пену в растворе, уводятся в осадок, в этом причина, почему мыло не вспенивается.
2-й специалист-химик. В промышленности карбоновые кислоты получают различными способами.
1-й способ состоит в каталитическом окислении парафинов. При этом через расплавленный парафин продувают воздух, содержащий добавки оксидов марганца:
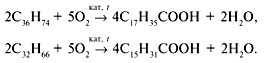
На производство мыла, олифы, смазок и других веществ недавно расходовалось до 400 000 т пищевых жиров. Между тем они с успехом могут быть заменены продуктами переработки нефти, угля, природных газов. В настоящее время эта задача успешно решается.
2-й способ – окисление спиртов:
![]()
3-й способ – окисление альдегидов:
![]()
Отдел рекламы (демонстрация выставки).
Мы дальше разговор ведем
И к применению перейдем.
Две вот эти кислоты –
Основа, знаете, свечи,
Что вечно вызывает удивление,
Меняя наше настроение.
Свечи несут нам освещение,
Еще нужны как украшение.
Смесь пальмитиновой и стеариновой кислот используют для изготовления стеариновых свечей. Жирные кислоты превращают в соли и используют для получения различных мыл. Жидкое мыло (калиевые соли) по сравнению с твердым (натриевые соли) лучше растворимо в воде и поэтому обладает более сильным моющим действием.
Мыла имеют недостаток: они плохо моют в жесткой воде. Кроме того, щелочной характер мыла вреден для некоторых тканей. В связи с этим широко развивается производство синтетических моющих средств. Как и мыло, моющие средства обладают хорошим моющим действием и не утрачивают его в жесткой воде.
Ведущий.
Вот двух кислот портрет,
Слушайте дальше ответ.
Пришла пора итоги подвести,
Как говорят,
Поставить точки все над i.
Фирма покупателей проводит небольшой конкурс, за участие в котором можно получить дополнительные очки.
1-й ученик. Я растворяю в 10 мл воды полтаблетки аспирина, раствор подогреваю в пробирке и добавляю 2–3 капли разбавленного раствора хлорида железа(III). Появляется фиолетовое окрашивание.
Каково строение аспирина? Почему появляется фиолетовое окрашивание?
2-й ученик (дает ответ). Аспирин – сложный эфир салициловой кислоты. При нагревании с водой происходит реакция гидролиза, в результате образуются две кислоты – салициловая и уксусная:
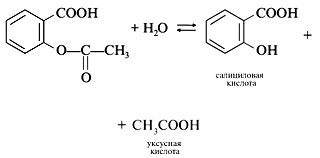
Салициловая кислота содержит две функциональные группы – OH и COOH. Фиолетовое окрашивание раствора обусловлено группой OH, вступающей с FeCl3 в характерную для фенолов реакцию.
Конкурс «Дальше, дальше»
1. Почему кислотные свойства карбоновых кислот гораздо выше, чем у спиртов?
2. Кто впервые из ацетилена получил уксусную кислоту?
3. Какое бытовое название бутановой кислоты?
4. В каком растении содержится муравьиная кислота?
5. Какой химический состав мыла?
6. Как называют продукт конденсации карбоновой кислоты с отщеплением молекулы воды?
7. Как называют безводную уксусную кислоту?
Подведение итогов
Во время урока участникам раздаются жетоны разного цвета. Красный жетон – очень хороший ответ. Желтый и синий жетоны – хороший ответ. Зеленый жетон – удовлетворительный ответ.
По количеству жетонов определяют итоги, выставляют оценки.
Т.Л.Гладченко,
учитель Икрянинской средней школы
(с. Икряное, Астраханская обл.)
![]()
Источник <http://him.1september.ru/articlef.php?ID=200600709>
Рекомендованная литература:
О. С. Габриелян и др. Химия 10 кл. М., Дрофа, 2002;
Л. С. Гузей, Р. П. Суровцева, Г. Г. Лысова. Химия 11 кл. Дрофа, 1999.
Г. Г. Лысова. Опорные конспекты и тесты по органической химии. М., ООО "Глик плюс", 1999.
===
Исп. литература для статьи «КАРБОНОВЫЕ КИСЛОТЫ»: Общая органическая химия, пер. с англ., т. 4, М., 1983, с. 11-137; The chemistry of carboxylic acids and esters, ed. by S. Patai, L, 1969; The chemistry of acid derivatives, ed. by S. Patai, pt. 1-2, N.Y., 1979. Д. В. Иоффе.
Лит.: Неницеску К. Д., Органическая химия, пер. с рум., т. 1-2, М., 1962-1963; Несмеянов А. Н., Несмеянов Н. А., Начала органической химии, кн. 1-2, М., 1969-70.
