Физические свойства
Кристаллические бесцветные вещества, плохо растворимые в холодной воде (лучше при нагревании), обладают высокими температурами плавления (бензойная кислота – 1220С, п-толуиловая – 1810С), возгоняются.
Химические свойства
Проявляют общие свойства карбоновых кислот, т.е.
кислотная диссоциация
-

C6H5COO- + H+
образование солей
|
+ NaOH |
|
+HOH |
образование сложных эфиров
|
+C2H5OH |
|
+HOH |
хлорангидридов, амидов
|
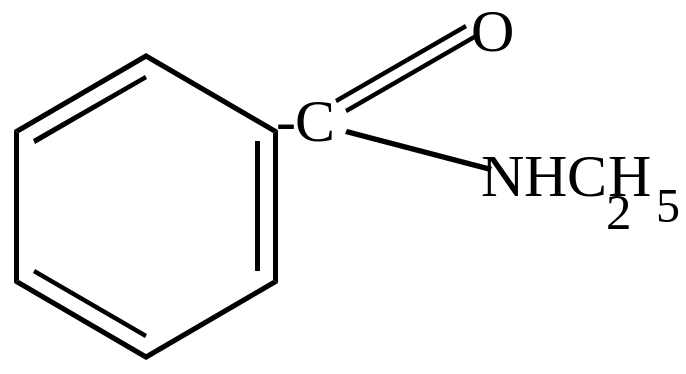
+NH2C2H5 |
|
Особенности свойств:
1. Кислоты, у которых группа –СООН связана непосредственно с ядром, обладают более сильными кислотными свойствами по сравнению с кислотами жирного ряда (за исключением муравьиной кислоты).
Формула |
Константа диссоциации |
Муравьиная кислота |
2,1.10-14 |
Бензойная кислота |
6,5.10-5 |
Уксусная кислота |
1,8.10-5 |
Это объясняется следующим: кислотные свойства обуславливаются тем, насколько сильно оттянута электронная пара от водорода, что зависит не только от явления взаимного влияния атомов в самой карбоксильной группе (показаны у муравьиной кислоты), но и от влияния радикала. Все углеводородные радикалы обладают электронодонорными свойствами и уменьшают полярность связи О-Н по сравнению с муравьиной кислотой, но у Ar донорные свойства выражены слабее, чем у Alk.
Различная сила кислотных свойств проявляется в реакциях вытеснения кислот из их солей.
CH3COONa
+ C6H5COOH
![]() C6H5COONa
+ CH3COOH
C6H5COONa
+ CH3COOH
ацетат натрия бензойная кислота растворимо в воде уксусная кислота
(нерастворима в воде)
При введении в ароматическое ядро электронодонорных групп константа диссоциации уменьшается, при введении электроноакцепторной группы – увеличивается.
Формула кислоты |
Константа диссоциации |
C6H5COOH |
6,5.10-5 |
o-CH3C6H4COOH |
6,95.10-3 |
o-NO2C6H4COOH |
1,2.10-3 |
2) Образование хлорангидридов может происходить не только при действии PCl5
|
+ PCl5 |
|
+ |
|
+ HCl |
но и другими путями:
а) при непосредственном действии хлора на ароматические альдегиды. Хлор при этом замещается Н в альдегидной группе, т.к. нет подвижного водорода в -положении.
|
+ Cl2 HCl + |
|
б) при гидролизе бензотрихлорида ограниченным количеством воды:
|
+ H2O 2 HCl + -HCl |
|
бензотрихлорид |
|
|
3) Благодаря плоскому жесткому строению бензольного кольца реакционноспособность карбоксильной группы зависит от пространственных факторов.
Например, реакция этерификации ароматических кислот при наличии двух заместителей в о-положении не идет вследствие пространственных затруднений.