
- •Оглавление
- •Введение
- •Правила работы с тестами
- •Аминокислот, пептидов и белков». Занятие 1. Введение в практикум. Аминокислоты, пептиды.
- •Методические указания к самоподготовке
- •Примеры тестов для контроля исходного уровня знаний:
- •1.1. … Является незаменимой аминокислотой для человека
- •1.2. Формула … соответствует глутаминовой кислоте в форме диполярного иона.
- •2.1. Из колонки 2 выберите боковые радикалы, соответствующие α-аминокислотам, указанным в колонке 1.
- •3.1. Какие из приведенных ниже высказываний согласуются с представлениями о строении и свойствах пептидной группы?
- •3.2. Выберите из приведенных ниже высказываний те, которые согласуются с представлениями о трансаминировании α аминокислот.
- •Работа 2. Нингидриновая реакция.
- •Работа 3. Реакция глицина с формальдегидом.
- •Работа 4. Реакция глицина с азотистой кислотой.
- •Работа 5. Амфотерные свойства α-аланина.
- •Работа 6. Биуретовая реакция.
- •Работа 7. Ксантопротеиновая реакция (Мульдера).
- •Работа 8. Реакция Фоля.
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний Задание 1. Выберите наиболее правильный ответ.
- •1.1. …Придают белкам основный характер.
- •1.2. Атомы остова полипептидной цепи располагаются в следующем порядке:
- •2.2. Структура белка – стабилизирующие связи.
- •Примеры ситуационных задач Задача 1.
- •Задача 2.
- •Самостоятельная работа студентов
- •Работа 1. Количественное определение белка сыворотки крови биуретовым методом.
- •Техника выполнения работы
- •Фотоэлектроколориметр
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи Задача 1.
- •Задача 2.
- •Занятие 3. Физико-химические свойства белков.
- •Методические указания к подготовке
- •Примеры тестов контроля исходного уровня знаний
- •1.1. Дан трипептид гли – ала – вал
- •1.2. В полипептидной цепи прерывает -спирализацию … .
- •2.2. Уровень организации белковой молекулы – ее структурный элемент.
- •3.1. Предложите наиболее оптимальный метод осаждения белка-фермента с целью дальнейшего использования его каталитической активности.
- •3.2. Выберите метод, которым можно очистить белки сыворотки крови от сернокислого аммония при разделении их высаливанием.
- •Ход работы
- •Работа 2. Осаждение белков при кипячении.
- •Ход работы
- •Работа 3. Осаждение белков солями тяжелых металлов.
- •Осаждение белков медным купоросом.
- •Осаждение белков уксуснокислым свинцом.
- •Работа 4. Осаждение белков органическими кислотами.
- •Ход работы
- •Задача 2.
- •Занятие 4. Методы выделения и очистки белков.
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •1.1. Молекулярная масса белков … .
- •2.2. Установите соответствие.
- •3.2. … Основаны на различии размера молекул.
- •Примеры ситуационных задач Задача 1.
- •Устройство прибора для электрофореза
- •Проведение электрофореза
- •Выключение прибора и выявление белковых фракций
- •Количественное определение белковых фракций
- •Денситометрический метод
- •Работа 2. Диск-электрофорез в полиакриламидном геле. Принцип метода
- •Ход работы
- •Работа 4. Очистка от низкомолекулярных примесей методом гельфильтрации на сефадексе (молселекте).
- •Ход работы
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •1.1. Гемоглобин связывается с углекислым газом …..
- •1.2. … По структуре является гликопротеином.
- •3.1. Во многих гликопротеинах углеводный компонент присоединяется к белку посредством гликозидной связи через… .
- •3.2. Протеогликановые комплексы (мукополисахариды) характеризуются … .
- •Работа 2. Выделение муцина слюны и определение в нем углеводного компонента.
- •Ход работы
- •Работа 3. Выделение казеиногена из молока.
- •Ход работы
- •Занятие 6. Коллоквиум по модулю «Строение и функции белков.
- •Методические указания к самоподготовке
- •Контрольные вопросы по модулю «Строение и функции аминокислот, пептидов и белков».
- •Модуль 2. Ферменты Занятие 7. Классификация, структура и свойства ферментов.
- •Методические указания к самоподготовке
- •Примеры тестов для контроля исходного уровня знаний
- •3.1. Фермент от неорганического катализатора отличает ....
- •3.2. Для количественного определения глюкозы в сыворотке крови применяют ...
- •Порядок выполнения работы
- •Качественная реакция на крахмал
- •Реакция Фелинга
- •Работа 3. Термолабильность ферментов.
- •Порядок выполнения работы
- •Работа 4. Влияние рН среды на активность амилазы слюны.
- •Порядок выполнения работ
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •1.2. Молярная активность (число оборотов) ферментов выражается в...
- •Задача 1.
- •Задача 2.
- •Ход работы
- •Практическое значение работы
- •Работа 4. Определение активности щелочной фосфатазы в сыворотке крови по гидролизу n-нитрофенилфосфата.
- •Принцип метода
- •Ход работы
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •3.1. Вещества-антиметаболиты являются...
- •3.2. Иммобилизованные ферменты используются...
- •Примеры ситуационных задач Задача 1.
- •Работа 6. Конкурентное торможение сукцинатдегидрогеназной активности. Принцип метода
- •Ход работы
- •Иммуноферментный анализ.
- •1. Прямой ифа
- •Модуль 3. Биологические мембраны. Регуляторные молекулы. Занятие 11. Биологические мембраны. Особенности цитоплазматических мембран у бактерий ( семинар).
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •1.1. Избирательная проницаемость мембран достигается путем активного транспорта. Активный транспорт отличается от пассивного тем, что… .
- •1.2. Маркером плазматической мембраны является фермент…
- •2.2. Липид – его характеристика
- •3.1. Из перечисленных ферментов антиоксидантной активностью обладают… .
- •3.2. Жирная кислота, в молекуле которой содержится 20 атомов углерода и 4 двойные связи -… .
- •Примеры ситуационных задач Задача 1.
- •Занятие 12. Регуляторные механизмы у эукариот и прокариот. Рецепторы (семинар).
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Занятие 13. Гормоны пептидной и белковой природы.
- •Методические указания к самоподготовке
- •Примеры ситуационных задач
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов к ситуационным задачам Задача 1.
- •Задача 2.
- •Занятие 14. Стероидные гормоны. Тканевые гормоны.
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач.
- •Работа 2. Качественное определение 17-кетостероидов в моче.
- •Эталоны ответов к тестовым заданиям.
- •Эталоны ответов к ситуационным задачам Задача 1.
- •Задача 2.
- •Занятие 15. Коллоквиум по модулю «Биомембраны. Регуляторные молекулы».
- •Методические указания к самоподготовке
- •Контрольные вопросы к коллоквиуму:
- •Модуль 4. Энергетический обмен. Занятие 16. Введение в обмен веществ. Биохимия питания.
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •3.1. Полноценные пищевые белки – это … .
- •3.2. Биологическая роль пектинов ...
- •Работа 4. Количественный анализ желудочного сока.
- •Техника выполнения работы
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи Задача 1.
- •100 Г белка – 16 г n
- •80 Г белка – х
- •Задача 2.
- •3500 Ккал – 100%
- •Занятие 17. Витамины и факторы роста бактерий. Биологическая роль в метаболизме.
- •Методические указания к самоподготовке
- •1.1. По химической природе витамины – это...
- •1.2. Витамин е является …
- •2.1. Витамин – химическая структура.
- •2.2. Сопоставьте химическое название витамина и название по проявлению недостаточности
- •3.1. Активирование витамина д заключается ...
- •3.2. Утверждения относительно витамина а являются верными:
- •Примеры ситуационных задач
- •Оформление работы
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи Задача 1.
- •Задача 2.
- •Занятие 18. Введение в биоэнергетику. Макроэргические соединения. Общие пути катаболизма.
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний Задание 1. Выберите один наиболее правильный ответ:
- •Примеры ситуационных задач Задача 1.
- •Принцип метода
- •Ход работы
- •Работа 2. Качественное определение активности сукцинатдегидрогеназы мышц.
- •Ход работы
- •Расчеты
- •Практическое значение работы
- •Работа 4. Восстановление цитохрома с.
- •Ход работы
- •Работа 5. Обнаружение активности цитохромоксидазы.
- •Задача 2.
- •Занятие 19. Тканевое дыхание и окислительное фосфорилирование (семинар).
- •Методические указания к самоподготовке
- •Примеры тестовых заданий Задание 1. Выберите один наиболее верный ответ:
- •1.1. Бурая жировая ткань ...
- •Задание 2. Установите соответствие.
- •2.1. Дайте определение перечисленным типам окисления:
- •3.2. Соединения, обладающие разобщающим действием: ...
- •Примеры ситуационных задач Задача 1.
- •Задача 2.
- •Занятие 20. Образование энергии в фотосинтезирующих организмах (семинар).
- •Методические указания к самоподготовке
- •Примеры тестов для контроля исходного уровня знаний
- •1.1. В состав фотосистемы I входят все компоненты, кроме:
- •1.2. Реакции световой фазы фотосинтеза протекают в:
- •2.1. Установите принадлежность кофакторов фотосинтеза:
- •2.2. Установите соответствие:
- •3.1. Переносчиками электронов в фс1 при нециклическом транспорте являются:
- •3.2. Процесс, который не относится к реакции световой фазы:
- •4.1. Компонентов акцепторной системы реакционного центра фс1:
- •4.2. Циклического потока электронов в фс1:
- •Примеры ситуационных задач Задача 1
- •Задача 2
- •Занятие 21. Коллоквиум по модулю «Энергетический обмен».
- •Контрольные вопросы к коллоквиуму:
- •Модуль 5. Обмен углеводов. Занятие 22. Структура и свойства моносахаридов, дисахаридов и полисахаридов.
- •Методические указания к самоподготовке
- •Примеры тестов для контроля исходного уровня знаний
- •Примеры вопросов контрольной работы:
- •Работа 3. Реакция Фелинга.
- •Работа 4. Взаимодействие моносахаридов с аммиачным раствором оксида серебра (проба Толленса).
- •Работа 5. Реакция Селиванова на фруктозу.
- •Работа 8. Отсутствие восстанавливающей способности у сахарозы.
- •Работа 9. Реакция Барфеда.
- •Работа 10. Качественная реакция на крахмал.
- •Работа 11. Кислотный гидролиз крахмала.
- •Эталоны ответов на тесты
- •Эталоны ответов на контрольные упражнения
- •Занятие 23. Пути поступления и расходования углеводов в организме. Метаболизм гликогена.
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •1.1. Все известные амилазы желудочно-кишечного тракта осуществляют расщепление:
- •1.2. Переносчиком гликозильных групп в реакции биосинтеза гликогена является ...
- •3.1. Уровень глюкозы в крови повышают ...
- •3.2. Моносахариды в кишечнике всасываются ...
- •Примеры ситуационных задач Задача 1.
- •Самостоятельная работа студентов
- •Глюкозооксидазным методом. Принцип метода
- •Ход определения
- •Эталоны ответов к тестам
- •Эталоны ответов к ситуационным задачам Задача 1.
- •Задача 2.
- •Занятие 24. Катаболизм глюкозы. Анаэробный и аэробный гликолиз. Спиртовое и молочнокислое брожение.
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний:
- •1.1. При окислительном декарбоксилировании пирувата в аэробных условиях образуется ... .
- •3.1. В процессе гликолиза необратимыми являются реакции образования:
- •3.2. При распаде углеводов у микроорганизмов обнаруживают ....
- •Порядок выполнения работы
- •Работа 2. Открытие продуктов дрожжевого сбраживания глюкозы.
- •Порядок выполнения работы
- •Ход определения
- •Работа 4. Обнаружение продуктов спиртового брожения. Ход работы
- •Эталоны ответов на тестовые задания
- •Эталоны ответов на ситуационные задачи Задача 1.
- •Задача 2.
- •Занятие 25. Глюконеогенез. Пентозофосфатный путь превращения глюкозы. Путь Энтнера-Дудорова у бактерий. Регуляция обмена углеводов (семинар).
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •1.1. Энергетические расходы в глюконеогенезе на одну молекулу глюкозы из двух молекул пировиноградной кислоты составляют ... Атф.
- •1.2. Пентозофосфатный путь окисления глюкозы ....
- •3.1. Общими метаболитами для пентозного цикла и гликолиза являются...
- •3.2. Установите правильную последовательность процесса глюконеогенеза из липидов:
- •Задача 2.
- •Занятие 26. Коллоквиум по модулю «Обмен углеводов».
- •Контрольные вопросы к коллоквиуму
- •Модуль 6. Структура, функции и обмен липидов. Занятие 27. Структура и свойства липидов.
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •1.1. Из приведенных высказываний относительно ненасыщенных жирных кислот, входящих в состав липидов, является верным…
- •1.2. Из приведенных высказываний относительно свойств липидов, является верным…
- •2.2. Жирная кислота-количество углеродных атомов в цепи:
- •3.1. … Образуются при омылении фосфолипидов .
- •3.2. …Встречаются в составе ганглиозидов.
- •Занятие 28. Переваривание и всасывание липидов. Обмен нейтрального жира.
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •1.1. Ферменты, участвующие в расщеплении жиров в желудочно-кишечном тракте относятся к классу….
- •1.2. Высшие жирные кислоты образуются из всех перечисленных соединений, кроме….
- •3.1. Особенно высокая активность фермента глицеролкиназа обнаруживается в….
- •3.2. Переваривание и всасывание липидов нарушается при дефиците ….
- •Работа 3. Количественное определение суммарных липидов в сыворотке крови. Принцип метода
- •Ход работы
- •Занятие 29. Обмен жирных кислот, окисление и синтез. Синтез кетоновых тел.
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •1.1. Окисление жирных кислот является источником энергии во всех тканях, кроме…
- •1.2. Транспорт жирной кислоты из цитозоля в митохондрии осуществляется с помощью… .
- •3.1. При бета-окислении жирных кислот с нечетным количеством углеродных атомов образуются… .
- •3.2. Катаболизм жирных кислот до со2 и н2о включает следующие стадии…. .
- •Ход работы
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов к ситуационным задачам Задача 1.
- •Занятие 30. Обмен стероидов. Метаболизм холестерина. Обмен фосфолипидов.
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •1.1. Донором метильных групп для синтеза фосфатидилхолина из фосфатидилэтаноламина является… .
- •1.2. Фосфатидная кислота образуется в результате… .
- •3.1. Биохимические функции лхат:
- •3.2. Липотропными факторами являются… .
- •Эталоны ответов к тестовым заданиям.
- •Эталоны ответов к ситуационным задачам. Задача 1.
- •Задача 2.
- •Занятие 31. Коллоквиум по модулю « Структура и функциии липидов».
- •Методические указания к самоподготовке
- •Контрольные вопросы
- •Модуль 7. Обмен аминокислот, белков и нуклеопротеинов. Занятие 32. Переваривание и всасывание белков. Протеолитические ферменты.
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Работа 2. Определение активности пепсина и уропепсина. Принцип метода
- •Ход определения активности уропепсина
- •Принцип метода
- •Ход определения
- •Эталоны ответов на тестовые задания
- •Эталоны ответов на ситуационные задачи Задача 1.
- •Задача 2.
- •Занятие 33. Общие пути метаболизма аминокислот: переаминирование, дезаминирование, декарбоксилирование.
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •1.1. В состав коферментов аминотрансфераз входит витамин....
- •1.2. Серотонин синтезируется из....
- •3.1. …. Являются производными этого соединения:
- •3.2. Функции гистамина:....
- •Принцип метода
- •Ход работы
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи Задача 1.
- •Задача 2.
- •Занятие 34. Конечные продукты азотистого обмена.
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний Задание 1. Выберите один наиболее верный ответ.
- •1.1. Предшественник мочевины в орнитиновом цикле … .
- •2.2. В ходе орнитинового цикла последовательно образуются … .
- •5. Орнитин, карбамоилфосфат, аргининосукцинат, аргинин, цитруллин
- •2.1. Реакция – фермент
- •2.2. При катаболизме указанных аминокислот образуются....
- •3.1. Источниками аммиака в организме являются ... .
- •3.2. В синтезе мочевины участвуют следующие ферменты ... .
- •Работа 2. Определение содержания мочевины в сыворотке крови ферментативным методом. Принцип метода
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи Задача 1.
- •Задача 2.
- •Занятие 35. Специфические пути метаболизма отдельных аминокислот.
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •1.1. Заболевание (синдром), при котором наблюдается моча черного цвета – ... .
- •1.2. В данной реакции образуется ....
- •3.1. При развитии фенилкетонурии в крови и моче накапливаются ... .
- •3.2. Метиленовая группа в молекуле метилен-н4-фолата может превращаться в ... .
- •Примеры ситуационных задач Задача 1.
- •Задача 2.
- •Самостоятельная работа студентов
- •Занятие 36. Метаболизм нуклеопротеинов и нуклеотидов.
- •Методические указания к самоподготовке
- •Примеры тестового контроля
- •1.1. Нуклеотиды расщепляются ферментами:
- •1.2. В биосинтезе пиримидиновых нуклеотидов используется фермент ... .
- •2.2. Выберите соединения, являющиеся донорами азота в синтезе пуриновых и пиримидиновых нуклеотидов:
- •3.1. Ксантиноксидаза катализирует реакции:
- •3.2. Выберите из перечисленных условий возможные причины подагры:
- •Работа 2. Определение содержания мочевой кислоты в сыворотке крови фосфорновольфрамовым методом. Принцип метода
- •Ход определения
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •1.1. Нуклеотиды соединяются между собой ... .
- •1.2. Синтез рнк-затравки катализирует фермент ... .
- •3.1. Компоненты и факторы необходимые для биосинтеза рнк ...
- •3.2. Закономерности, раскрывающие вторичную структуру днк – правила американского биохимика Чаргаффа ... .
- •Примеры ситуационных задач Задача 1.
- •Задача 2.
- •Самостоятельная работа студентов
- •Работа 1. Метод выделения плазмидной днк из дрожжей для последующего введения в клетки e.Coli.
- •Ход работы
- •Секвенирование - исследование последовательности нуклеотидов днк.
- •Полимеразная цепная реакция.
- •Клонирование - способ получения больших количеств идентичных молекул нуклеиновых кислот или их фрагментов
- •Занятие 38. Биосинтез белка и его регуляция. Особенности биосинтеза у микроорганизмов (семинар).
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •1.1. Энхансеры представляют собой участки днк размером 10-20 пар оснований, присоединение к которым регуляторных белков ... .
- •1.2. Реакцию
- •Катализирует фермент ...
- •2.2. Оператор – это участок молекулы прокариотической днк, отвечающий в транскрипции за:
- •3.1. … Используются в ходе трансляции как макроэрги
- •3.2. К посттрансляционной модификации белков не относится ...
- •Примеры ситуационных задач Задача 1.
- •Задача 2.
- •Эталоны ответов на тесты контроля исходого уровня знаний
- •Эталоны ответов к ситуационным задачам
- •Задача 2.
- •Занятие 39. Молекулярные механизмы генетической изменчивости. Мутации (семинар).
- •Методические указания к самоподготовке
- •13. Перечислите формы переноса генетического материала у бактерий.
- •Примеры тестов контроля исходного уровня знаний
- •1.1. Для проведения генно-инженерных процедур необходимо ... .
- •1.2. Частота мутаций на одну гамету за поколение составляет ... .
- •3.1. Для трансформации чаще всего используют:
- •3.2. Внедрение генов в компетентные клетки осуществляется при помощи:
- •Примеры ситуационных задач Задача 1.
- •Задача 2.
- •Эталоны ответов на тесты контроля исходого уровня знаний
- •Эталоны ответов к ситуационным задачам Задача 1.
- •Задача 2.
- •Занятие 40. Коллоквиум по модулю «Обмен аминокислот, белков и нуклеопротеинов».
- •Методические указания к самоподготовке
- •Контрольные вопросы к коллоквиуму
- •Модуль 8. Функциональная биохимия специализированных тканей и органов. Занятие 41. Водно-солевой обмен и его регуляция.
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний.
- •1.1. Влияние кальцитонина на минеральный обмен характеризуется…
- •1.2. Микроэлементами в организме человека являются… .
- •3.1. В регуляции водно-натриевого гомеостаза участвуют…
- •3.2. Стимулом для увеличения секреции ренина является…
- •Примеры ситуационных задач Задача 1.
- •Задача 2.
- •Самостоятельная работа студентов
- •Принцип метода
- •Ход работы
- •Эталоны ответов к тестовым заданиям.
- •Эталоны ответов к ситуационным задачам Задача 1.
- •Задача 2.
- •Занятие 42. Взаимосвязь обмена веществ и его регуляция.
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний.
- •1.1. Повышение концентрации глюкозы при пищеварении стимулирует…
- •1.2. Универсальным энергетическим субстратом для всех тканей является….
- •3.1. Обмен углеводов, липидов и аминокислот главным образом регулируют …
- •3.2. Уровень глюкозы крови контролируют гормоны поджелудочной железы… .
- •Техника определения
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи Задача 1
- •Задача 2.
- •Занятие 43. Механизмы обезвреживания токсических веществ.
- •Методические указания для самоподготовки
- •Примеры тестов контроля исходного уровня знаний.
- •1.1. В реакциях микросомального окисления участвует цитохром…
- •1.2. Сульфаниламидные препараты, инактивируются в результате реакции… .
- •2.1.Основными поставщиками протонов и электронов в реакции микросомального окисления являются:
- •3.1. В реакциях инактивации активных форм кислорода участвуют…
- •3.2. Для выяснения антитоксической функции печени применяют… .
- •Примеры ситуационных задач
- •Ход определения
- •Работа 3. Проба Квика-Пытеля. Принцип метода
- •Задача 2.
- •Занятие 44. Перекисное окисление липидов. Активные формы кислорода. Механизмы антиокислительной защиты.
- •Методические указания для самоподготовки
- •Примеры тестов контроля исходного уровня знаний
- •1.1. Супероксидрадикал генерируют все ферменты, кроме….
- •1.2. … Образуется при взаимодействии перекиси водорода с супероксидрадикалом.
- •3.1. Основные свойства радикалов кислорода...
- •3.2. Продуцируют природные радикалы кислорода… .
- •Эталоны ответов на ситуационные задачи Задача 1 .
- •Занятие 45. Биохимия крови
- •Методические указания для самоподготовки
- •Примеры тестов контроля исходного уровня знаний
- •3.1 К возникновению железодефицитных анемий чаще всего приводят…
- •3.2. Белки плазмы крови выполняют следующие функции…
- •Работа 2. Определение активности альфа-амилазы в сыворотке крови амилокластическим методом. Принцип метода
- •Ход работы
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Задача 2.
- •Занятие 46. Биохимия печени.
- •Методические указания для самоподготовки
- •Примеры тестов контроля исходного уровня знаний
- •1.1. Содержание в крови прямого билирубина и активность алт возрастает при….
- •1.2. Утверждение, относящееся к синтезу гема …
- •2.1. Гем распадается с образованием железа и желчных пигментов. Какова дальнейшая судьба этих соединений?
- •3.1. В основе детоксикации ядовитых веществ в печени лежат процессы…
- •3.2. Процессы… … происходят только в печени.
- •Примеры ситуационных задач Задача 1.
- •Задача 2.
- •Самостоятельная работа студентов.
- •Работа 1. Пробы на коллоидоустойчивость.
- •Ход работы
- •Работа 2. Количественное определение активности альдолазы в сыворотке крови (метод Брунса в модификации е.Н. Валуйской и в.И. Товарницкого).
- •Принцип метода
- •Ход работы
- •Работа 3. Определение активности альдолазы фруктозо-1-монофосфата.
- •Принцип метода
- •Ход работы
- •Работа 4. Количественное определение билирубина в сыворотке крови по методу Иендрашека. Принцип метода
- •Ход работы
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи Задача 1.
- •Задача 2.
- •Занятие 47. Система гемостаза
- •Методические указания для самоподготовки
- •Примеры тестов контроля исходного уровня знаний
- •Работа 2. Определение времени рекальцификации плазмы.
- •Ход работы
- •Эталоны ответов к тестовым заданиям
- •Эталоны тветов на ситуационные задачи
- •Задача 2.
- •Занятие 48. Основы иммунохимии (семинар).
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Эталоны тветов на ситуационные задачи
- •Занятие 49. Биохимия специализированных тканей и органов.
- •Методические указания для самоподготовки
- •Примеры тестов контроля исходного уровня знаний
- •1.1. Способностью связывать кальций обладает белок… .
- •1.2. … Процессы, обеспечивающие энергией интенсивно работающую мышцу.
- •3.1. Гидроксилирование аминокислот … … в коллагене нарушается при авитаминозе витамина «с».
- •3.2. Среди свободных аминокислот мозга преобладает… .
- •Работа 2. Количественное определение свободного оксипролина в моче.
- •Ход работы
- •Работа 3. Определение холинэстеразы в головном мозге.
- •Работа 4. Выделение гликогена из мышечной ткани.
- •Ход работы
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •2.1. Установите соответствие цифровых и буквенных положений.
- •Эталоны ответов на ситуационные задачи
- •Приложения
- •Рекомендуемая литература
- •Журналы по биохимии (библиотека бгму)
- •Некоторые биохимические показатели жидких сред организма
- •Экзаменационные вопросы
Работа 2. Нингидриновая реакция.
Принцип метода. Реакция основана на способности альфа-аминокислот при взаимодействии с нингидрином подвергаться дезаминированию. При этом отщепленная аминогруппа участвует в образовании мурексидного комплекса сине-фиолетового цвета.
Техника выполнения работы. В пробирку поместите 4 капли 1 % раствора глицина и 2 капли 0,1 % раствора нингидрина. Содержимое пробирки осторожно нагрейте до появления сине-красной окраски.
Химизм реакции:

Работа 3. Реакция глицина с формальдегидом.
В пробирку поместите 5 капель 1 % раствора глицина и добавьте 1 каплю индикатора метилового красного. Раствор окрашивается в желтый цвет (нейтральная среда). К полученной смеси добавьте равный объем формалина. Отметьте появление красной окраски (кислая среда). Данная реакция под названием "формольное титрование" используется для количественного определения карбоксильных групп в α-аминокислотах. Напишите реакцию взаимодействия глицина с формальдегидом.
Работа 4. Реакция глицина с азотистой кислотой.
В пробирку поместите 5 капель 1 % раствора глицина и равный объем 5 % раствора нитрита натрия. Добавьте 2 капли концентрированной уксусной кислоты и осторожно взболтайте смесь. Наблюдайте выделение газа. Реакция используется для количественного определения аминогрупп в аминокислотах. Напишите реакцию взаимодействия глицина с азотной кислотой.
Работа 5. Амфотерные свойства α-аланина.
1. В пробирку поместите 5 капель 1 % раствора альфа-аланина и добавьте по каплям 0,1 % раствор хлороводородной кислоты, подкрашенный индикатором конго в синий цвет, до появления розово-красной окраски.
2. В пробирку поместите 5 капель 1 % раствора α-аланина и по каплям добавьте 0,1 % раствор гидроксида натрия, подкрашенный фенолфталеином, до исчезновения окраски.
Работа 6. Биуретовая реакция.

Принцип метода. Реакция основана на способности пептидной группы белков и полипептидов образовывать с ионами меди в щелочной среде комплексные соединения фиолетового цвета.
Реакция позволяет обнаружить наличие пептидной группы -CO-NH- в исследуемом веществе и, следовательно, является универсальной реакцией для обнаружения веществ белковой природы. Свое название реакция получила от производного мочевины биурета, который дает в данных условиях то же окрашивание, что и белок. Окрашивание появляется за счет образования медной комплексной соли (см. реакцию).
Техника выполнения работы. В две пробирки поместите по 5 капель раствора яичного белка и желатины. В обе пробирки добавьте по 10 капель раствора едкого натра и по одной капле раствора сульфата меди. В обеих пробирках появляется красно- или сине-фиолетовое окрашивание.
Работа 7. Ксантопротеиновая реакция (Мульдера).
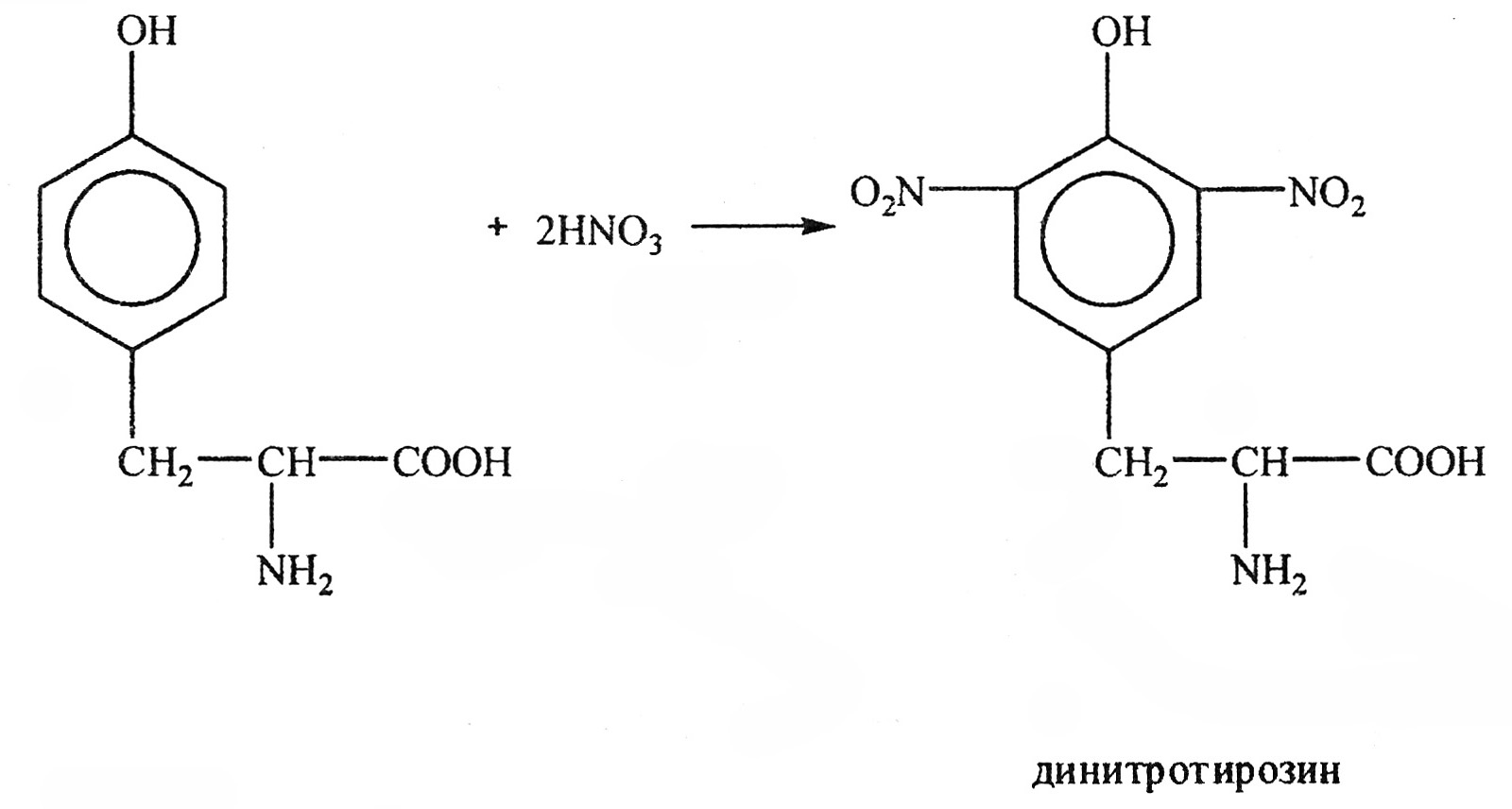
При подщелачивании возникает хиноидная структура, окрашенная в оранжевый цвет.

Реакция основана на способности циклических аминокислот фенилаланина,триптофана, гистидина и тирозина, содержащих бензольное кольцо, при взаимодействии с концентрированной азотной кислотой образовывать нитропроизводные желтого цвета. В щелочной среде нитропроизводные циклических аминокислот превращаются в соответствующие соли хиноидной структуры, окрашенные в оранжевый цвет. При взаимодействии азотной кислоты с тирозином реакция нитрования протекает по выше представленному уравнению.
В одну пробирку поместите 5 капель 1% раствора яичного белка , в другую- 1% раствора тирозина. В обе пробирки добавьте по 3 капли концентрированной азотной кислоты. Нагрейте до кипения (осторожно!). Отметьте появление желтого окрашивания. Содержимое пробирок охладите под краном, к охлажденному раствору прибавляйте по каплям 10 % раствора едкого натра до тех пор, пока не начнется переход окраски.
