
- •Краткая история развития теплотехники
- •Термодинамическая система
- •Параметры состояния
- •Уравнение состояния и термодинамический процесс
- •Теплота и работа
- •Внутренняя энергия
- •Первый закон термодинамики
- •Теплоемкость газа
- •Уравнение состояния идеального газа
- •Смесь идеальных газов
- •Основные положения второго закона термодинамики
- •Энтропия
- •Метод исследования тд процессов
- •Основные термодинамические процессы идеального газа
- •Политропный процесс
Энтропия
Одним из функций состояния термодинамической системы является энтропия. Энтропией называется величина определяемая выражением:
dS = dQ / T. [Дж/К]
или для удельной энтропии:
ds = dq / T. [Дж/(кг·К)]
Энтропия есть однозначная функция состояния тела, принимающая для каждого состояния вполне определенное значение. Она является экстенсивным (зависит от массы вещества) параметром состояния и в любом термодинамическом процессе полностью определяется начальным и конечным состоянием тела и не зависит от пути протекания процесса.
Энтропию можно определить как функцию основных параметров состояния:
S = f1(P,V) ; S = f2(P,T) ; S = f3(V,T) ;
или для удельной энтропии:
s = f1(P,υ) ; s = f2(P,T) ; s = f3(υ,T) ;
Так как энтропия не зависит от вида процесса и определяется начальными и конечными состояниями рабочего тела, то находят только ее изменение в данном процессе
Цикл и теоремы Карно
Циклом Карно называется круговой цикл, состоящий из 2-х изотермических и из 2-х адиабатных процессов. Обратимый цикл Карно в p,υ- и T,s- диаграммах показан на рис.3.1.
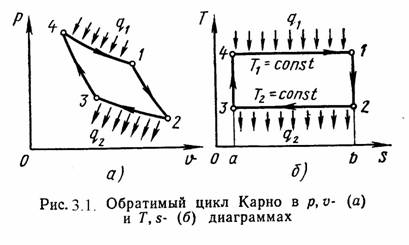
1-2 – обратимое адиабатное расширение при s1=Const. Температура уменьшается от Т1 до Т2. Работу получают за счет уменьшения внутренней энергии.
2-3 – изотермическое сжатие, отвод теплоты q2 к холодному источнику от рабочего тела.
3-4 – обратимое адиабатное сжатие при s2=Const. Температура повышается от Т3 до Т4.
4-1 – изотермическое расширение, подвод теплоты q1 к горячего источника к рабочему телу. В этом процессе вся подводимая теплота превращается в работу.
Основной характеристикой любого цикла является термический коэффициент полезного действия (т.к.п.д.).
ht = Lц / Q1 ,
или
ht = (Q1 – Q2) / Q1 .
Для обратимого цикла Карно т.к.п.д. определяется по формуле:
htк = (Т1 – Т2) / Т1 .
Отсюда следует 1-я теорема Карно:
"Термический к.п.д. обратимого цикла Карно не зависит от свойств рабочего тела и определяется только температурами источников".
Из сравнения произвольного обратимого цикла и цикла Карно вытекает 2-я теорема Карно:
"Обратимый цикл Карно является наивыгоднейшим циклом в заданном интервале температур".
Т.е. т.к.п.д. цикла Карно всегда больше т.к.п.д. произвольного цикла: htк > ht .
Метод исследования тд процессов
Как сказано ранее первый закон ТД устанавливает взаимосвязь между количеством теплоты, внутренней энергией и работой. При этом, количество теплоты подводимое к телу или отводимое от тела зависит от характера процесса.
К основным ТД процессам относятся: изохорный, изотермический, изобарный и адиабатный.
Для всех этих процессов устанавливается общий метод исследования, который заключается в следующем:
выводится уравнение процесса кривой Pυ и Ts – диаграммах;
устанавливается зависимость между основными параметрами рабочего тела в начале и конце процесса;
определяется изменение внутренней энергии по формуле, справедливой для всех процессов идеального газа:
при постоянной теплоемкости DU = m·сv·(t2 - t1);
вычисляется работа: L = P·(V2 – V1);
определяется количество теплоты, участвующее в процессе:
q = cx·(t2- t1);
определяется изменение энтальпии по формуле, справедливой для всех процессов идеального газа:
Di = (i2 – i1)
или при постоянной теплоемкости: Di = сp·(t2 – t1);
определяется изменение энтропии:
Ds = cv·ln(T2/T1) + R·ln(υ 2/υ 1) ;
Ds = cp·ln(T2/T1) - R·ln(P2/P1) ;
Ds = cv·ln(T2/T1) + cp·ln(υ 2/υ 1) .
Все процессы рассматриваются как обратимые.
