- •Введение
- •1. Углеводы
- •1.1. Строение углеводов
- •1.2. Химические свойства углеводов
- •1.3. Производные углеводов
- •2. Нуклеиновые кислоты
- •2.1. Повреждения структуры днк
- •3. Липиды и клеточные мембраны
- •3.1. Эфиры жирных кислот и глицерина
- •3.2. Липидные компоненты клеточных мембран
- •3.3. Клеточные мембраны
- •4. Аминокислоты, пептиды и белки
- •4.1. Аминокислоты
- •4.2. Пептиды и белки
- •5. Ферменты
- •5.1. Индуцированное соответствие
- •5.2. Эффект сближения реагирующих групп
- •5.3. Дестабилизация связей
- •5.4. Согласованный кислотно-основный катализ
- •5.5. Ингибирование ферментов
- •6. Метаболизм
- •7. Катаболические превращения
- •7.1. Гликолиз
- •7.2. Окислительное декарбоксилирование пирувата
- •7.3. Цикл Кребса
- •7.4. Катаболизм жирных кислот
- •7.5. Катаболические превращения аминокислот
- •8. Окислительное фосфорилирование
- •Nad(p)h fmn убихинон cyt b cyt c1 cyt c cyt aa3 o2
- •9. Фотосинтез
- •10. Основные анаболические процессы
- •10.1. Глюконеогенез
- •10.2.Биосинтез жирных кислот
- •10.3. Биосинтез терпеноидов
- •10.4. Биосинтез аминокислот
- •10.5. Биосинтез пептидов и белков
- •10.6. Образование азотистых оснований и нуклеиновых кислот
- •11. Нейрогуморальная регуляция
- •12. Метаболизм ксенобиотиков
- •13. Клетки и активный кислород
- •Заключение
- •Оглавление
5.1. Индуцированное соответствие
Взаимодействующая с активным центром фермента молекула суб-страта включается во внешнюю сферу белковой молекулы и меняет харак-тер отношений между полярными группами внешней сферы. В результате этого минимум энергии соответствует уже другому их расположению, и тогда проявляется легкость протекания внутренних перестроек гидрофоб-ного наполнения белковой глобулы. Эта конформационная перестройка завершается тем, что субстрат оказывается уже в окружении других функ-циональных групп, которые и обеспечивают каталитическое превращение. Часто после перестройки субстрат оказывается включенным во внутрен-нюю сферу белковой глобулы. В растворах ферментов это выражается в изменении многих физико-химических показателей: меняются оптическое вращение, скорость седиментации, вязкость, термическая стабильность.
После протекания реакции снова изменяется характер взаимодействия теперь уже продуктов превращения субстрата с окружающими его функ-циональными группами фермента и тогда новая перестройка приводит к отходу продуктов превращения от активного центра и восстановлению его строения в том состоянии, которое готово к присоединению новой моле-кулы субстрата. В соответствии с этим каждое состояние субстрата вызы-вает иное распределение окружающих его функциональных групп, что и отличает индуцируемое соответствие от модели «ключ-замок».
5.2. Эффект сближения реагирующих групп
Одна из главных особенностей ферментативного катализа заключа-ется в эффекте сближения реагирующих групп. В результате взаимодейст-вия субстрата с его окружением в активном центре реагирующие группы оказываются в наиболее благоприятном для протекания реакции положе-нии. Этот эффект наблюдается и в обычной органической химии. Так, на-пример, реакция гидролиза п‑бромфениловых эфиров карбоновых кислот катализируется карбоксилатными ионами:
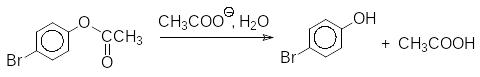
Если скорость гидролиза п-бромфенилацетата в присутствии эквива-лентного количества ацетата натрия принять за единицу, то соль моно-п-бромфенилового эфира глутаровой кислоты гидролизуется примерно в 1000 раз скорее, в 2,2105 раза скорее гидролизуется соль соответствую-щего моноэфира янтарной кислоты:
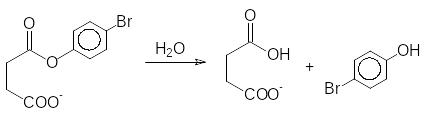
А для моно-п-бромфенилового эфира малеиновой кислоты скорость гидролиза возрастает в 107 раз. Интересно, что для солей моно-п-бром-фениловых эфиров некоторых 2,2-дизамещённых глутаровых кислот ско-рость гидролиза может увеличиваться в 31018 раз. Это связано с уменьше-нием степеней свободы при вращении молекул, что обеспечивает опти-мальное расположение катализирующей гидролиз анионной карбоксилат-ной группы около сложноэфирной группы.
Ещё один пример представлен реакцией гидролиза гликозидов сали-циловой кислоты и 4-гидроксибензойной кислоты. Скорость гидролиза первого соединения на 4 порядка выше, чем второго:
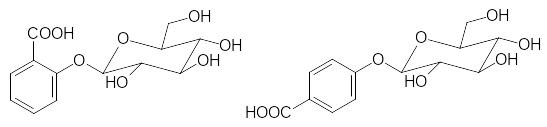
Здесь очевидна каталитическая роль кислотной группы, которая у производного салициловой кислоты находится непосредственно у аномер-ного (гликозидного) атома кислорода.
И последний пример: известно, что прямая реакция этерификации фенола карбоновыми кислотами идёт крайне медленно, но в то же время 2‑гидроксикоричная кислота циклизуется в лактон (кумарин) даже в щелочной среде: