- •Тюменская государственная архитектурно-строительная академия Кафедра «Строительные материалы» дорожно-строительные материалы
- •Введение.
- •Общие методические указания.
- •Раздел 1. Методические указания по разделам программы курса.
- •Глава 1. Начальные сведения о материалах.
- •Структура строительных материалов.
- •Свойства строительных материалов.
- •1.3. Вопросы для самоконтроля.
- •Глава 2. Материалы на основе минерального сырья.
- •2.1. Природные каменные материалы.
- •2.1.1. Вопросы для самоконтроля.
- •2.2. Керамические материалы.
- •2.2.1. Вопросы для самоконтроля.
- •2.3. Неорганические вяжущие вещества.
- •2.3.1. Вопросы для самоконтроля.
- •2.4. Растворы и бетоны на основе неорганических вяжущих веществ.
- •2.5. Расчет состава тяжелого цементного бетона.
- •Основные этапы расчета:
- •I этап: Расчет ориентировочного (начального) состава бетона
- •Значение коэффициента а1 и а2
- •Коэффициент раздвижки зерен в зависимости от расхода цемента и в/ц
- •2.5.1. Вопросы для самоконтроля.
- •Глава 3. Материалы на основе органических вяжущих.
- •3.1. Полимерные материалы.
- •3.1.1. Вопросы для самоконтроля.
- •3.2. Органические вяжущие вещества.
- •3.2.1. Вопросы для самоконтроля.
- •3.3. Дорожные бетоны на основе органических вяжущих материалов
- •3.3.1. Вопросы для самоконтроля.
- •3.4. Проектирование состава асфальтобетона.
- •Ориентировочный зерновой состав минеральной части
- •Глава 4. Материалы на основе древесины.
- •4.1. Вопросы для самоконтроля.
- •Глава 5. Металлические материалы.
- •5.1. Вопросы для самоконтроля.
- •Раздел 2. Контрольное задание № 1.
- •Глава 6. Примеры решения задач.
- •6.1. Основные свойства.
- •Задача.
- •Задача.
- •Задача.
- •Задача.
- •Задача.
- •6.2. Горные породы.
- •Задача:
- •Задача.
- •3. Задача.
- •6.3. Керамические материалы.
- •1.Задача.
- •2.Задача.
- •3.Задача.
- •6.4. Неорганические вяжущие.
- •Решение: После обжига масса сухого известняка
- •6.5. Цементные бетоны.
- •1. Задача.
- •Раздел 3. Контрольное задание № 2.
- •Глава 7. Примеры решения задач.
- •7.1. Материалы на основе древесины.
- •7.2. Органические вяжущие.
- •Вязкость разжиженного битума
- •На вязкость составленного дегтя.
- •7.3. Бетоны на основе органических вяжущих.
- •Технические требования к щебню (гост 8267-93).
- •Технические требования к песку (гост 8736-93).
- •Технические требования к минеральному порошку. (гост 16557-78)
- •Показатели прочности и морозостойкости щебня и гравия (гост 9128-97)
- •Показатели физико-механических свойств плотных и высокоплотных асфальтобетонов из горячих смесей (гост 9128-97)
- •Характеристика битумов нефтяных дорожных (гост 22245-90)
- •Литература.
Раздел 1. Методические указания по разделам программы курса.
Глава 1. Начальные сведения о материалах.
Структура строительных материалов.
Окружающий нас мир представляет собой различные формы, вечно движущейся и изменяющейся материи (от латинского слова «materrerum» – мать вещей). Веществом называется вид материи, обладающий при определенных условиях постоянными свойствами (плотностью, твердостью, цветом, точкой плавления и т.д.).
Вещества слагаются из одного или нескольких химических элементов. Каждый химический элемент состоит из одинаковых атомов – электрически нейтральных частиц, в центре которых находится атомное ядро. В ядре сосредоточена основная масса атома, и оно несет положительный электрический заряд. Ядро состоит из протонов, имеющих положительный заряд, и нейтронов, не несущих никакого заряда. Большую часть объема атома составляет пространство, в котором движутся электроны. Электроны связаны с ядром и удерживаются от свободного перемещения в пространстве силами притяжения между частицами с противоположными по знаку электронными зарядами (кулоновскими силами, или электростатическим притяжением).
В большинстве случаев вещества построены из молекул или ионов, которые образуются из атомов. Молекула представляет собой совокупность прочно связанных атомов. Атомы соединяются в молекулы за счет сил химических связей. Возникновение различных видов химической связи вызывается различием во взаимодействии электронов.
Различаются следующие типы связей: 1) ионная связь, 2) ковалентная связь, 3)металлическая связь.
Вещества с ионной связью образуются при соединении металла с неметаллическими элементами.
Ионная связь относится к электростатическим силам, существующим между частицами с зарядами противоположного знака (рис. 1). Типичным примером вещества с ионной связью является гипс – СаSО4.

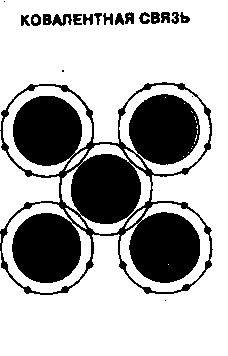
Ковалентная связь возникает в результате обобществления электронов двумя атомами (рис. 2). Энергия ковалентной связи очень велика. Такая связь характерна для высокомолекулярных углеводородов в полимерах, для атома кварца.
Рис. 2
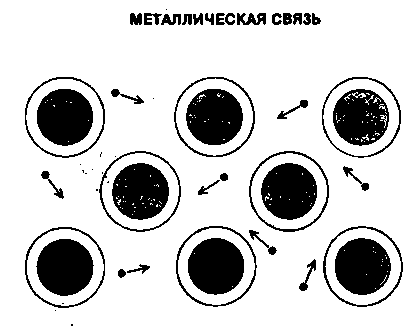
Металлическая связь характерна для твердых металлов. В металле каждый атом связан с несколькими соседними атомами. Связывающие их электроны могут относительно свободно перемещаться по всей трехмерной структуре металла (рис. 3). Эта связь обуславливает такие типично металлические свойства, как высокая электропроводность и блеск.
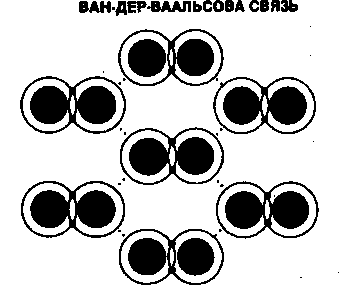
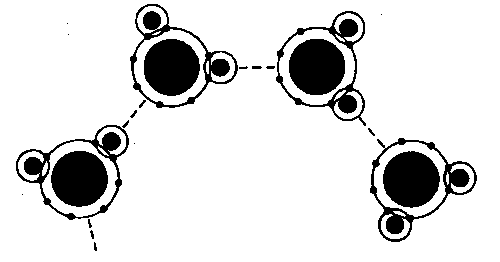
Существование вещества в жидкой и твердой формах объясняется силами притяжения, действующими между молекулами или ионами. Эти силы называются межмолекулярными силами. Все межмолекулярные силы имеют электростатическую природу. Различают ван-дер-ваальсовые силы (взаимодействие между нейтральными частицами) (рис. 4) и водородную связь (рис. 5). Водородная связь существует в тех веществах, где атом водорода присоединен к атомам кислорода, азота или фтора.
Рис. 4 |
ВОДОРОДНАЯ СВЯЗЬ
Рис. 5 |
Водородная связь более слабая, чем ионная и ковалентная, но сильнее вандерваальсовой. Тем не менее, водородная связь оказывает заметное влияние на свойства многих веществ.
В природе материалов в чистом виде все перечисленные разновидности связей встречаются редко, поскольку практически всегда налагаются два типа связей или более, хотя обычно и превалирует одна из них.
Всякий материал имеет структуру, под которой понимается определенное расположение, или конфигурация, составляющих его компонентов.
Структуру вещества (материала) можно рассматривать на трех уровнях:
1) на уровне субатомной структуры; ее анализируют, изучая размещение и плотность электронов, и их взаимодействие;
2) на уровне микроструктуры – исследуются организация атомов или молекул (например, расположение атомов в кристаллической решетке), а также большие группы атомов с хорошо выраженными особенностями. Эти группы образуют микроструктурные элементы;
3) на уровне макроструктуры – ее изучают, анализируя взаимное размещение микроструктурных элементов. Макроструктуру можно видеть невооруженным глазом.
Изучение субатомной структуры и микроструктуры возможно только с помощью физико-химических приборов высокого разрешения (электронные микроскопы, рентгеновские аппараты, спектрометры, синхрофазотроны и др).