2.4. Химические свойства алкенов
Химические свойства алкенов определяются наличием в их молекулах двойной связи.
2.4.1. Реакции электрофильного присоединения
Электронное облако π-связи подвергается атаке электрофильными реагентами. Поэтому многие реакции алкенов протекают по механизму электрофильного присоединения, обозначаемого символом АЕ (от англ. addition electrophilic). Реакции электрофильного присоединения — это ионные процессы, протекающие в несколько стадий. На первой стадии происходит взаимодействие электрофильной частицы с электронным облаком π-связи. Положительно заряженная электрофильная частица за счет электростатического притяжения образует с молекулой алкена π-комплекс. В качестве электрофильной частицы чаще всего выступает протон Н+, источником которого являются протонсодержащие кислоты HCI, HBr, H2SO4. Затем образуется ковалентная связь между протоном и одним из атомов углерода двойной связи. Этот атом углерода переходит в состояние sp3-гибридизации. Второй атом углерода двойной связи приобретает положительный заряд, и вся частица становится карбкатионом.
Карбкатион — это частица с положительным зарядом на атоме углерода. Положительно заряженный атом углерода в карбокатионе находится в sp3-гибридном состоянии. Он имеет вакантную р-орбиталь, и три его σ-связи располагаются в одной плоскости.

На второй стадии процесса карбкатион взаимодействует с анионом Х - и образует с ним σ-связь за счет пары электронов аниона.
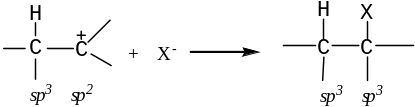
Характерной особенностью электронного облака π-связи является его подвижность. Под влиянием заместителей электронная плотность π-связи может смещаться к одному из атомов углерода. π-Связь тогда становится полярной, а на атомах углерода, соединенных двойной связью, возникают частичные заряды. Увеличение полярности в конечном счете может привести к гетеролитическому разрыву π-связи.

Большинство реакций присоединения к алкенам протекает по следующей общей схеме:

Ниже приведены некоторые реакции электрофильного присоединения к алкенам:

Правило Марковникова: при присоединении молекул типа НХ к несимметричным алкенам атом водорода присоединяется к более гидрогенизированному атому углерода двойной связи.
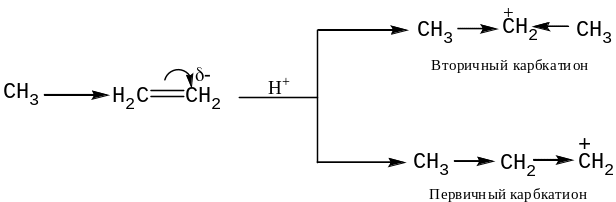
Такое направление реакции объясняется совокупностью двух факторов. В статическом, т. е. нереагирующем, состоянии в несимметричных алкенах под действием заместителей происходит смещение электронной плотности π-связи с возникновением частичных зарядов, определяющих место будущей атаки со стороны протона. В пропене местом атаки будет атом С-1 с частичным отрицательным зарядом, возникшим под действием +I-эффекта метильной группы.
![]()
В динамическом состоянии, т.е. в процессе реакции, из двух возможных карбкатионов будет получаться более устойчивый вторичный карбкатион. Он образуется за счет присоединения протона к более гидрогенизированному атому углерода. Во вторичном карбкатионе атом углерода, несущий положительный заряд, связан с двумя алкильными группами, в первичном — с одной. Поэтому во вторичном карбкатионе за счет +I-эффекта двух алкильных групп происходит более эффективное понижение положительного заряда.