
1. Вивчення кінетики реакції інверсії сахарози
Ціль роботи: вивчення кінетичних характеристик реакції першого (псевдопершого) порядку.
Цільові задачі: оволодіння методом розрахунку порядку реакції з використанням поляриметричного методу; освоєння методики роботи на поляриметрі; розрахунок кінетичних характеристик реакції (константи швидкості, енергії активації, часу напіврозпаду, часу інверсії сахарози на 10%).
Проведення досліду:
Включити водяну баню або термостат і довести температуру 60оС. Включити поляриметр і дати йому прогрітися не менше 10 хв.
Відміряти розчини глюкози і HCl (їх концентрації і об’єми вказуються викладачем). Злити обидва розчини в склянку з притертою пробкою. В момент змішування почати відлік часу.
Отриману реакційну суміш заповнити кювету поляриметра і виміряти кути обертання площину поляризації (αt) через 3, 6, 10, 20, 30, 40 хвилин від початку реакції.
Зразу ж після заповнення кювети суміш, що залишилася в склянці, помістити у водяну баню або термостат при 60оС на 30 хв. При цьому реакція проходить практично до кінця.
Вийняти склянку із сумішшю з термостату (водяної бані), охолодити до кімнатної температури, заповнити нею кювету і визначити кут обертання, що відповідає виникненню рівноваги (α).
Експериментальні дані показати викладачу. Обчислити необхідні для подальших обчислень величини. Всі експериментальні і розрахункові дані занести в таблиці.
Побудувати графік залежності ln(αt – α) від часу і продовжити його до перетину з віссю ординат (точка А).
Виміряти відрізок, що рівний ОА, рівний ln(α0 – α), і записати його значення в таблицю.
Концентрація HCl С = моль/л:
Температура досліду Т = оС
№
Час від початку досліду t, хв.
Кут обертання площини поляризації α, о
αtα
α0α
ln(αtα)
α0α
ln
αtα
k, хв1
1
0
2
3
3
6
4
10
5
20
6
30
7
40
8
kсер =
Обчислити величини
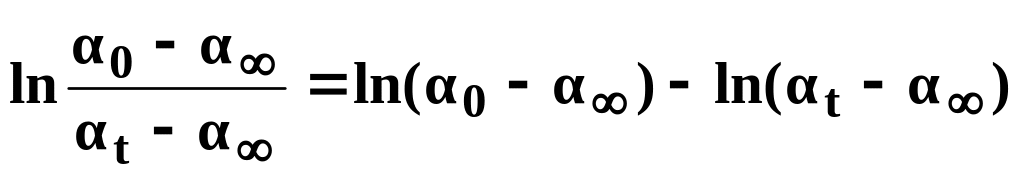 для кожного моменту часу; результати
занести в таблицю.
для кожного моменту часу; результати
занести в таблицю.Розрахувати для кожного інтервалу часу константу швидкості інверсії сахарози:
![]()
Після того, як будуть знайдені константи швидкості інверсії для кожного моменту часу, обчислити середнє значення kсер.
Розрахувати енергію активації реакції по рівнянню Арреніуса:
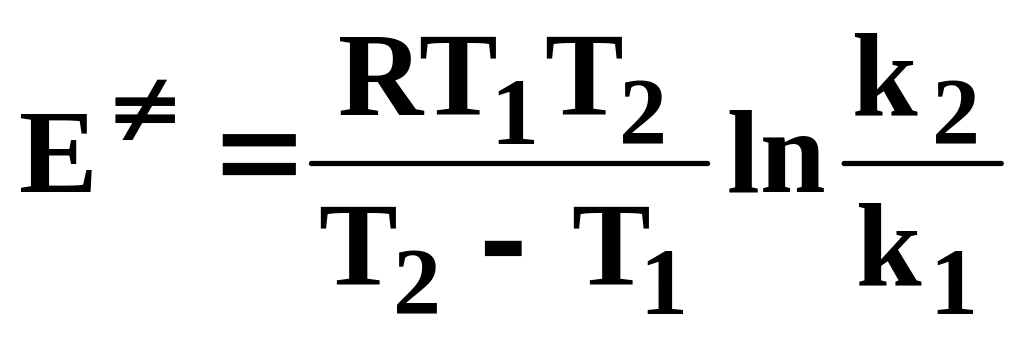
використовуючи вказані викладачем значення k2 і Т2 і приймаючи температуру досліду за Т1, а середнє значення константи швидкості – за k1.
Розглянути час напівреакції (t1/2) і час інверсії сахарози на 10% по рівнянню:
![]() ,
,
![]()
![]()
