
- •Химические элементы, присутствующие в некоторых объектах анализа
- •Примеры аналитических реакций
- •Виды химического анализа Классификация видов химического анализа:
- •V изменяется в ходе реакции
- •Физический смысл - отношение скоростей обратной и прямой реакций. Степень ионизации α – доля ионизованных молекул
- •- Предельный закон. 2. Расширенный закон.
- •3.Уравнение Дэвиса. 4. Эксперимент для электролитов. 5. Эксперимент для неэлектролитов (сахароза).
v1 = k1 при αA = αB = 1
V изменяется в ходе реакции
При динамическом равновесии k1 = k-1
Тогда: k1/k-1 = К0равн = (αC∙αD)/(αA∙αB)
В общем виде:
eA + fB = gC + hD
и тогда
K0равн = (αCg∙αDh)/(αAe∙αBf)
Физический смысл - отношение скоростей обратной и прямой реакций. Степень ионизации α – доля ионизованных молекул
D ↔ A+ + B-
αΑ+ = αB- = C∙α; αD = C∙(1 – α);
K0равн = (αA+∙αB-)/αD = C∙{α2/(1 – α)};
α
<< 1; K0равн
= α2∙C;
α
=
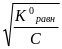
CKCl, M (18oC) |
α |
Kравн |
|
CAcH, M |
α |
Kравн |
2,0 |
0,71 |
3,5 |
0,2 |
0,0095 |
1,83∙10-5 |
|
1,0 |
0,76 |
2,3 |
0,1 |
0,0136 |
1,83∙10-5 |
|
0,5 |
0,79 |
1,5 |
0,01 |
0,0419 |
1,83∙10-5 |
|
0,1 |
0,86 |
0,54 |
0,005 |
0,0585 |
1,83∙10-5 |
Активность - кажущаяся концентрация заряженной частицы, в соответствии с которой та проявляет себя в химических реакциях (Льюис, 1907 г.):
α = γ∙[В]; γ <1
Зависимость α от I (Льюис, Рэндел, 1921 г.).
Ионная сила раствора - мера интенсивности электрического ноля, создаваемого ионами в растворе, характеристика числа заряженных частиц:
n
I = 0,5∙Σ(Cj∙Zj2)
j=1
Дебай, Хюккель (1923 г.):
Во всех разбавленных растворах сильных электролитов с одинаковой ионной силой катионы и анионы с равными численными значениями зарядов имеют одинаковые коэффициенты активности.
Предельный закон (частица - точечный заряд):
lgγ
= - 0,511∙Z2·![]() (I
≤ 0,01)
(I
≤ 0,01)
lgγ = -0,511∙Z2 · /(1 + ) (I = 0,1- 0,5)
Уравнение Дэвиса:
lg γ = -0,511∙Z2· /(1 + ) - 0,1·Z2∙I (I = 0,5-1,0)
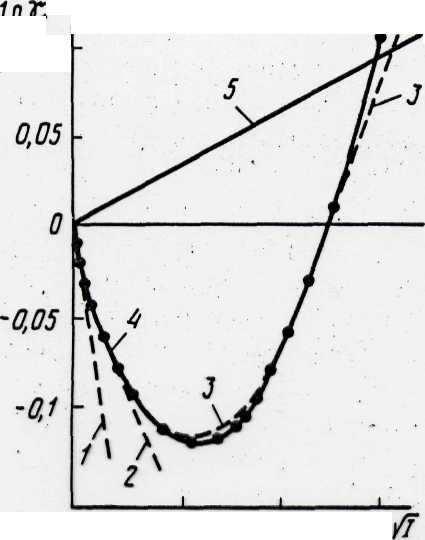
Графики зависимости величин γ от I.
- Предельный закон. 2. Расширенный закон.
3.Уравнение Дэвиса. 4. Эксперимент для электролитов. 5. Эксперимент для неэлектролитов (сахароза).
Эффективные диаметры и коэффициенты активноста ионов в водных растворах при 250
(по Киланду)
Ионы |
ri∙10-1 нм |
0,001 |
0,005 |
0,01 |
0,05 |
0,1 |
H3O+ |
9 |
0,967 |
0,933 |
0,914 |
0,86 |
0,83 |
Li+, C6H5COO- |
6 |
0,965 |
0,929 |
0,907 |
0,84 |
0,80 |
Na+, IO3- CH3COO- |
4-4,5 |
0,964 |
0,928 |
0,902 |
0,82 |
0,78 |
OH-, F-, ClO4-, MnO4- |
3,5 |
0,964 |
0,926 |
0,900 |
0,81 |
0,76 |
K+, Cl-, I-, NO3-, HCOO- |
3 |
0,964 |
0,925 |
0,899 |
0,80 |
0,76 |
Rb+, Cs+, Ag+, NH4+ |
2,5 |
0,964 |
0,924 |
0,898 |
0,80 |
0,75 |
Mg2+, Be2+ |
8 |
0,872 |
0,755 |
0,69 |
0,52 |
0,45 |
Ca2+, Cu2+, Zn2+ |
6 |
0,870 |
0,749 |
0,675 |
0,48 |
0,40 |
Sr2+, Ba2+, Cd2+, Hg2+ |
5 |
0,868 |
0,744 |
0,67 |
0,46 |
0,38 |
Pb2+, CO32- |
4,5 |
0,868 |
0,742 |
0,665 |
0,46 |
0,37 |
Hg22+, SO42-, CrO42- |
4 |
0,867 |
0,740 |
0,660 |
0,44 |
0,36 |
Al3+, Fe3+, Cr3+ |
9 |
0,738 |
0,54 |
0,44 |
0,24 |
0,18 |
PO43+, [Fe(CN)6]3- |
4 |
0,725 |
0,50 |
0,40 |
0,16 |
0,095 |
Th4+, Zr4+ |
11 |
0,588 |
0,35 |
0,255 |
0,10 |
0,065 |
[Fe(CN)6]4- |
5 |
0,57 |
0,31 |
0,20 |
0,048 |
0,021 |
