
ХИМИЯ НЕФТИ И ГАЗА
.pdf
vk.com/club152685050 | vk.com/id446425943
44
 CH4 + C5H12
CH4 + C5H12
C6H14 |
+ H2 |
C2H6 |
+ C4H10 |
|
 2 C3H8
2 C3H8
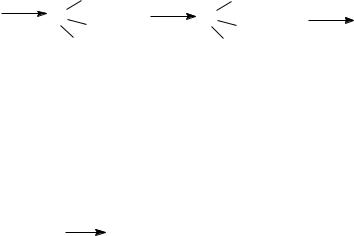
В ходе каталитического риформинга нафтенов протекают реакции изомеризации, дегидрирования, гидрокрекинга:
|
CH3 |
|
|
|
+ 3 H2 |
дегидрирование |
|
CH |
|
CH3 |
|
3 |
|
|
|
|
C2H5 + |
|
изомеризация |
|
+ H2 |
CH3 |
|
|
+ CH4 |
|
|
|
|
гидрокрекинг |
|
|
C3H8 + C4H10 |
|
|
В ходе каталитического риформинга аренов протекают реакции |
|||
изомеризации, диспропорционирования: |
|
|
|
CH |
CH3 |
|
|
3 |
|
|
|
2 |
+ |
|
|
|
|
|
|
|
|
CH3 |
CH3 |
|
CH3 |
|
|
|
H3C |
|
CH3 |
В условиях каталитического риформинга происходит изомеризация и ароматизация бензиновых фракций, что повышает эксплуатационные характеристики топлив.
Контрольные вопросы
1Явление катализа. Механизм действия катализаторов.
2Основные технические характеристики катализаторов.
3Особенности и механизм каталитического крекинга.
4Каталитический риформинг: сырье, основные реакции.
5Особенности и основные процессы гидрокрекинга.
6Применение процессов каталитического крекинга, риформинга, гидрокрекинга.
Список рекомендуемой литературы
1Сыркин А.М., Мовсумзаде Э.М. Основы химии нефти и газа.-Уфа:
Изд-во УГНТУ, 2002.- C.99-101.
2Химия нефти и газа: учеб.пособие для вузов /под ред.Проскурякова А.Е.
иДрабкина Е.Е.- СПб.: Химия, 1996.-С.240-268.
3Пузин Ю.И. Химия нефти и газа: электронный учебно-методический комплекс. – Уфа: УГНТУ, 2009.- Гл.6.3.2.

vk.com/club152685050 | vk.com/id446425943
45
С.С. Злотский, Н.Н. Михайлова
Лекция 13. Окисление углеводородов. Основные кислородсодержащие продукты нефтехимии
Ключевые слова: окисление углеводородов, цепные реакции, спирты, карбоксильные соединения, кислоты, гидропероксиды, катализаторы, ингибиторы, депарафинизация.
Окисление углеводородов до углекислого газа и воды (сжигание, горение) широко используется для получения тепла и совершения работы:
CnH2n+2 + (3n+1)/2O2  nCO2 + (n+1)H2O + Q
nCO2 + (n+1)H2O + Q
При этом углеводороды теряются безвозвратно, поскольку в настоящее время проблема регенерации углекислого газа в промышленном масштабе не решена.
Неполное, контролируемое селективное окисление углеводородов различного строения до ценных и полезных в практическом значении продуктов и мономеров является важнейшей составной частью нефтехимии. В этих реакциях широко используются различные окислители – молекулярный кислород и озон, перекиси, минеральные кислоты, окислы и соли металлов переменной валентности и др. Часто в ходе окислительных превращений имеет место разрушение (деструкция) углеводородного скелета и образуется несколько молекул с меньшим числом атомов углерода. Окисление насыщенных и алкилароматических углеводородов в жидкой фазе протекает по механизму цепной, свободно-радикальной реакции с промежуточным образованием гидропероксидов, быстрый распад которых приводит к молекулярным продуктам и новым радикалам, продолжающим цепное окисление.
Получение синтетических жирных кислот (СЖК) является одним из первых промышленных нефтехимических процессов окисления. Сырье представляет собой смесь твердых парафинов С20 – С40, полученных депарафинизацией масляных фракций. Окислителем выступает кислород воздуха, процесс осуществляется при 110 – 1500С, в качестве катализатора используются окислы и соли металлов переменной валентности в высшем состоянии окисления:
R1 |
|
CH |
|
CH |
|
R2 |
O2 |
R1COOH + R2COOH |
|
|
|
|
|||||
2 |
2 |
|
|
|
||||
Реакция протекает с разрывом углерод-углеродных связей и образуется смесь кислот С4-С20, которую после выделения из реакционной массы подвергают дистилляции и, как правило, разделяют на фракции по числу
атомов углерода в молекуле: С2-С7, С7-С9, С10-С16, С17-С20.
Применение СЖК находят в производстве поверхностно-активных веществ, фотореагентов, ингибиторов коррозии, пластификаторов и др.
Гордость отечественной нефтехимии – разработанный в СССР в середине XX века метод жидкофазного окисления изопропилбензола (кумола) до фенола

vk.com/club152685050 | vk.com/id446425943
46
и ацетона:
|
|
CH3 |
|
|
|
|
CH3 |
|
C CH3 |
OH |
|
|
|
CH |
O2 |
CH3 |
|
|||
CH3 |
OOH |
+ |
O |
|||
|
CH3 |
|||||
|
|
|
|
|
Ключевой стадией является кислотно-катализируемое разрушение гидроперекиси кумола при 50-600С.
В определенных условиях конденсация фенола с ацетоном приводит к ценному соединению – 2,2-бис(4'-оксифенил)-пропану:
|
|
|
CH3 |
|
2 |
OH + (CH3)2CO |
HO |
C |
OH |
|
|
|
CH3 |
|
Важнейшими продуктами нефтехимии являются простейшие α-окиси – окись этилена и окись пропилена. Их получают при 200 – 3000С реакцией соответствующего олефина с кислородом воздуха в присутствии различных катализаторов (чаще всего серебро, осажденное на инертных носителях – силикагель, Al2O3 и др.):
R |
|
CH |
|
CH |
+ O |
R |
|
CH |
|
CH |
R=H,CH |
|
|
|
|
||||||||
2 |
2 |
2 |
3 |
||||||||
|
|
|
|
|
|
|
|
O |
|
||
Целевые α-окиси используются для получения гликолей и полигликолей, алканоаминов, простых, сложных эфиров и др.
Окисление метильных групп в орто- и пара-ксилолах приводит к фталевым кислотам:
|
|
|
|
|
CH3 |
COOH |
H3C |
CH3 |
O2 |
HOC |
COH; |
CH3 O2 |
COOH |
|
||||||
|
|
|
O  O
O
На основе терефталевой кислоты производится широкая гамма синтетических волокон, эфиры орто-фталевой кислоты применяются в качестве пластификаторов.
В число основных кислородсодержащих продуктов нефтехимии входят этанол, пропанолы и бутанолы. Общим методом получения этанола, вторпропанола и втор-бутанола является кислотнокатализируемая гидратация этилена, пропилена и бутилена соответственно:
|
|
|
|
CH2 + H2O |
H+ |
|
|
|
CH |
|
CH3 |
R=H;CH3;C2H5 |
R |
|
CH |
|
R |
|
|
||||||
|
|
|
|
|
||||||||
|
|
|
||||||||||
|
|
|
|
|
|
|
|
OH |
|
|
|
|
Окислительное дегидрирование вторичных спиртов приводит к кетонам:
|
|
|
|
|
|
O2 |
|
|
|
|
RCH2 |
CH |
|
CH3 |
RCH2CCH3 |
R=H,CH3 |
|||||
|
|
|
|
|
|
|
|
|
||
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
||||
|
|
|
|
|
|
|
|
|||
Современный метод получения высших жирных спиртов (ВЖС) основан на реакции этилена с алюминийорганическими реагентами. Триэтилалюминий реагирует с молекулами этилена с образованием высших алюминийорганических соединений, которые окисляются кислородом до алкоголятов алюминия:
vk.com/club152685050 | vk.com/id446425943
47
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
(C2H4)xOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
(C2H4)x H |
O2 |
|
(OC2H4)x H |
H SO |
4 |
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
Al(C2H5)3+nC2H4 |
Al |
|
|
|
|
|
|
|
|
|
Al |
|
|
|
|
|
|
|
|
2 |
Al2(SO4)3 |
+H |
|
|
(C2H4)yOH |
||
(C2H4)y |
|
|
|
H |
|
(OC2H4)y |
|
|
H |
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
x,y,z=2,4,6... |
|
(C2H4)z |
|
H |
|
|
|
(OC2H4)z |
|
H |
|
|
|
|
H |
|
(C2H4)zOH |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Сернокислый гидролиз последних приводит к требуемой смеси ВЖС с четным числом атомов углерода.
Ряд кислородсодержащих соединений (спирты, альдегиды, кетоны, кислоты и др.) образуются при каталитическом газофазном взаимодействии олефинов со смесью монооксида углерода и водорода (синтез-газ). Из этилена образуется пропионовый альдегид, из пропилена - масляные альдегиды нормального и изостроения:
R |
|
CH |
|
CH2+ CO+ H2 |
R |
|
CH2 |
|
CH2 |
|
CHO + R |
|
|
CH |
|
CH3 R=H,CH3 |
|
|
|
|
|
|
|
|
|||||||||
|
|
|||||||||||||||
|
||||||||||||||||
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
CHO |
|||
В целом ассортимент кислородсодержащих продуктов современного нефтехимического синтеза включает сотни различных соединений, упомянем аллиловый спирт, глицерин, эпихлоргидрин, циклогексанол, циклогексанон, монохлоруксусную кислоту и др.
Контрольные вопросы
1 Основные стадии процесса получения фенола и ацетона.
2Основные стадии получения низших кетонов.
3Реакции, сопровождающие окисление высших парафинов до СЖК.
4Различие между жидкофазным и газофазным окислением.
5Реакция олефинов с синтез-газом.
Список рекомендуемой литературы
1Леффлер Уильям Л. Переработка нефти.–2-е изд., перераб.: пер. с англ.- М.: ЗАО «Олимп-Бизнес», 2004. – С.196-199.
2Имашев У.Б. Промышленная органическая химия на предприятиях Республики Башкортостан: учеб. пособие. –Уфа: Изд-во УГНТУ, 2000.–
С.44-68.

vk.com/club152685050 | vk.com/id446425943
48
Л.З.Рольник
Лекция 14. Методы очистки нефти, газа и нефтепродуктов
Ключевые слова: перегонка, очистка, нефть, дистиллаты, нефтепродукты, газы, крекинг, катализатор, температура, гидрогенизация, гидрообессеривание, сероводород, меркаптаны, сульфиды, дисульфиды, тиофен, бензтиофен, дибензтиофен.
В результате прямой перегонки и крекинга нефти получаются различные дистиллаты. Однако эти дистиллаты не являются готовыми товарными нефтепродуктами, так как содержат различные примеси. Поэтому все нефтепродукты должны подвергаться очистке, чтобы соответствовать техническим требованиям.
Для очистки различных нефтепродуктов и газов применяют следующие методы: химические (очистка серной кислотой, щелочью); физико-химические (адсорбция глинами); каталитические (под давлением и при повышенных температурах).
Химические методы
а) Очистка серной кислотой
Применяется для удаления непредельных углеводородов, а также сернистых, азотистых и смолистых веществ.
Непредельные соединения взаимодействуют с серной кислотой с образованием алкилсульфатов:
CnH2n+1CH = CH2 + H2SO4 |
CnH2n+1 |
|
CH |
|
O |
|
SO2OH |
|
|
|
|||||
|
|
||||||
|
|
|
CH3 |
||||
Сероводород с серной кислотой вступает в окислительно- |
|||||||
восстановительную реакцию: |
|
|
|
|
|
|
|
H2S + H2SO4 |
S + SO2 |
+ 2H2O |
|||||
Накопление серы нежелательно, поэтому сероводород удаляют промывкой щелочью до сернокислотной очистки. Полнота удаления смолистых и сернистых соединений зависит от условий очистки (концентрации кислоты, температуры и др.).
К недостаткам метода относится протекание различных побочных реакций с образованием полимеров.
б) Очистка щелочью
Применяется для удаления всех кислых соединений: нафтеновых и жирных кислот, фенолов, сероводорода, меркаптанов и др.
Для щелочной |
очистки |
применяют водные растворы NaOH |
||
(концентрация 3-20%): |
|
|
|
|
C H |
COOH + |
NaOH |
|
CnH2n+1 COONa + H2O |
|
||||
n 2n+1 |
|
|
|
|
Реакция обратима. Для смещения равновесия вправо необходимо увеличить концентрацию NaOH. Однако при этом образуется стойкая эмульсия «кислое масло-щелочь».

vk.com/club152685050 | vk.com/id446425943
49
Основная задача очистки газов - удаление сероводорода. Сероводород реагирует со щелочью с образованием кислых и средних солей:
H2S |
+ |
NaOH |
NaHS |
+ H2O |
H2S |
+ |
2NaOH |
Na2S |
+ 2H2O |
Меркаптаны взаимодействуют со щелочами с образованием меркаптидов:
CnH2n+1SH + NaOH |
|
Cn H2n+1SNa + H2O |
|
К недостаткам этого метода относятся:
1)меркаптиды легко гидролизуются;
2)меркаптаны нерастворимы в воде, что затрудняет их контакт со щелочью.
Физико – химические методы
К ним относится адсорбционная очистка глинами.
Некоторые пористые твердые вещества обладают большим запасом потенциальной поверхностной энергии (уголь, силикагель, глины).
Нефть, ее фракции – это смесь органических веществ, обладающих различной полярностью. Очищаемый продукт адсорбируется глиной, при этом наиболее полярные компоненты оседают на поверхности адсорбента, образуется адсорбционный комплекс, который подлежит удалению. Адсорбционная очистка глинами широко применяется в производстве нефтяных масел и для удаления смолистых веществ.
Целью очистки нефтяных масел глинами является удаление остатков смолистых веществ и полициклических углеводородов, а также нейтрализация масла после сернокислотной очистки.
Адсорбционная очистка масел ведется либо путем фильтрования через глину, либо контактным способом при нагревании масла до 300-3500С в смеси с тонко размолотой глиной. При этом смолы и полициклические углеводороды конденсируются в асфальтены.
Каталитические методы
Основная задача – обессеривание топлив и масел путем превращения сернистых соединений в углеводороды и сероводород (температура 400-4500С,
паровая фаза, катализатор – Al2O3 ∙ 3H2O с примесью SiO2).
При этом сернистые соединения распадаются с выделением H2S:
CnH2n+1SH |
C H |
|
|
|
n 2n |
C H |
SC H |
2CnH2n |
n 2n+1 |
n 2n+1 |
|
C H S-SC H |
2СnH2n |
|
n 2n+1 |
n 2n+1 |
|
+H2S
+H2S
+2H2S
Недостаток метода – уплотнение непредельных углеводородов, образование полимеров, дезактивация катализатора.
Наиболее прогрессивный метод гидрообессеривание, то есть каталитическая очистка под давлением водорода (гидрогенизация). В данном процессе происходит полное деструктивное гидрирование всех сернистых соединений, продукты не содержат непредельных соединений. Гидрообессеривание различных серусодержащих веществ протекает следующим образом:

vk.com/club152685050 | vk.com/id446425943
50
меркаптаны:
C H |
SH |
+ H |
C H |
|
+ |
H S; |
|
|
n 2n+1 |
|
2 |
|
|
||||
|
|
|
|
n 2n+2 |
|
2 |
|
|
сульфиды: |
|
|
|
|
|
|
|
|
C H SC H |
|
+ |
2H2 |
CnH2n+2 |
+ |
CmH2m+2 |
+ H2S; |
|
n 2n+1 m 2n+1 |
|
|
|
|
|
|
|
|
дисульфиды: |
|
|
|
|
|
|
|
|
CnH2n+1S-SCmH2m+1 |
|
+ 3H |
C H |
+ |
C H |
+ 2H S; |
||
|
|
|
2 |
n 2n+2 |
|
m |
2m+2 |
2 |
тиофан:
 + 2H2
+ 2H2  C4H10 + H2S; S
C4H10 + H2S; S
тиофен:
 + 3H2
+ 3H2  C4H10 + H2S; S
C4H10 + H2S; S
бензтиофен:
С2H5
+ H2 |
+ H2S; |
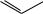
 S
S
дибензтиофен:
+ H2 |
+ H2S. |
S
Гидроочистка позволяет в значительной мере решить также проблему использования водорода, получающегося в больших количествах при каталитическом риформинге.
Контрольные вопросы
1 Классификация методов очистки нефти, газа и нефтепродуктов. 2 Химические методы очистки.
3Физико-химические методы очистки.
4Каталитические методы очистки. Гидрогенизация и гидрообессери-
вание.
Список рекомендуемой литературы
1 Сыркин А.М., Мовсумзаде Э.М. Основы химии нефти и газа. - Уфа:
Изд-во УГНТУ, 2002.- C.89-99.
2Рябов В.Д. Химия нефти и газа.- М.: ИД «ФОРУМ», 2009.- C.251-270.
3Виржичинская С.В., Дигуров Н.Г., Сиюшин С.А. Химия и технология нефти и газа: учеб. пособие.- М.: ИД «ФОРУМ», 2009.- C.246-252.
vk.com/club152685050 | vk.com/id446425943
51
Контрольные вопросы
для подготовки к экзамену по дисциплине «Химия нефти и газа» для студентов специальностей СТ, ГТ, МТ, БСТ, БМТ, ГБ, ГР, ГГ
Вопросы к модулю 1 «Состав и общие свойства нефтей и газов»
1Характеристика нефти. Гипотезы происхождения.
2Физические свойства нефти. Плотность и удельный вес.
3Молекулярная масса.
4Вязкость. Виды вязкости.
5Температуры застывания, помутнения, кристаллизации.
6 Показатель преломления. Молекулярная и удельная рефракции.
7 Электрические свойства нефтей. Пожароопасность нефтей и газов. Температуры вспышки, воспламенения, самовоспламенения.
8Октановое и цетановое числа.
9Элементный состав нефти. Основные классы соединений, содержащиеся в нефтях.
10Методы выделения и исследования состава нефти и газа. Экстракция сорбция, их виды. Кристаллизация.
11Дистилляционные методы разделения нефтей. Перегонка, ректификация.
12Методы выделения и исследования состава нефти и газа. Хроматография.
Вопросы к модулю 2 «Углеводороды нефти и газа»
13 Алканы нефти и газа. Номенклатура. Физические и химические свойства. Парафины и церезины.
14Нафтеновые углеводороды нефти. Номенклатура. Физические и химические свойства.
15Ареновые углеводороды нефти. Номенклатура. Физические и химические свойства.
16Алкены. Номенклатура, физические и химические свойства.
17Алкадиены. Физические и химические свойства.
18Алкины. Номенклатура. Физические и химические свойства.
Вопросы к модулю 3 «Гетероатомные и неуглеводородные соединения нефти
и газа»
19 |
Кислородсодержащие |
соединения |
нефти. |
Нефтяные кислоты. |
Номенклатура, физические и химические свойства. |
|
|||
20 Фенолы нефти. Номенклатура, физические и химические свойства. |
||||
21 |
Сернистые соединения нефти, физические и химические свойства. |
|||
22 |
Азотистые соединения нефти. Азотистые основания, нейтральные соединения. |
|||
23 |
Смолы. Асфальтены. |
Неорганические |
компоненты |
нефти. Классификация |
смолисто-асфальтеновых веществ нефти.
