
- •Кафедра хирургии и акушерства методические указания по теме: «Биологические объекты, использующиеся в биотехнологии»
- •Введение
- •Информационный материал
- •1. Общие сведения о биологических объектах
- •2. Вирусы и вироиды
- •3. Бактерии
- •4. Грибы
- •5. Простейшие
- •6. Водоросли
- •7. Растения
- •8. Животные
- •9. Требования, предъявляемые к биологическим объектам
- •10. Методы биотехнологии
- •12. Стадии биотехнологического процесса
- •Задания для аудиторной и самостоятельной работы
- •Вопросы для самоподготовки и контроля знаний студентов
- •Литература
- •Содержание
- •95492, Г. Симферополь, пгт. Аграрное, учебный корпус
10. Методы биотехнологии
Биотехнологии присущи свои специфические методы – это крупномасштабное глубинное культивирование биообъектов в периодическом, полунепрерывном или непрерывном режиме; выращивание клеток растительных и животных тканей в особых условиях. Биотехнологические методы культивирования биообъектов выполняются в специальном оборудовании, например, в ферментерах выращивают бактерии и грибы при получении антибиотиков, ферментов, органических кислот, некоторых витаминов, в подобных же ферментерах выращивают некоторые клетки человека (бласты) для получения белка – интерферона. Растительные клетки чаще выращивают в стационарных условиях на среде с уплотненной (например, агаризованной) подложкой в стеклянных или полиэтиленовых емкостях, хотя некоторые виды растительных клеток можно культивировать в специальных ферментерах. В стеклянных роллерах культивируют и большинство животных клеток или, например, в куриных эмбрионах.
Другие методы, используемые в биотехнологии, являются общими, например, с методами в микробиологии, биохимии, биоинженерии, органической химии и других науках.
Тем не менее, следует особо выделить методы клеточной и генной инженерии, когда в экспериментальных условиях удается создавать клетки с заведомо известными свойствами.
Однако даже в случае реализации генно-инженерных разработок измененная наследственная информация на уровне молекул инкорпорируется затем в клетках, с которыми и приходится иметь дело в биотехнологическом процессе. Из этого можно вывести представление об уровнях биотехнологии: клеточном и молекулярном. Тот и другой определяются биообъектами. В первом случае дело имеют с клетками, например, актиномицетов при получении антибиотиков, микромицетов при получении лимонной кислоты, животных при изготовлении вирусных вакцин, человека при изготовлении интерферона. Во втором случае дело имеют с молекулами, например, с нуклеиновыми кислотами в так называемой «рекомбинантной ДНК-биотехнологии» (рДНК-биотехнология), базирующейся на генной инженерии, или на использовании отдельных ферментов (ферментных систем), например, протеаз в моющих средствах, липаз для модификации вкуса молочных продуктов и т. д. Однако необходимо помнить, что в начальной или конечной стадии молекулярный уровень трансформируется в клеточный. Так, ферменты продуцируются клетками, а при генно-инженерных разработках реципиентом новой генетической информации становится также клетка.
Особенность методов, используемых в биотехнологии, заключается в том, что они должны выполняться, как правило, в асептических условиях, то есть при исключении возможности попадания в среду культивирования биообъекта болезнетворных (патогенных) и неболезнетворных (сапрофитных) микроорганизмов. Патогенные виды представляют непосредственную опасность для занятых в производстве людей и для потребителей конечных продуктов; сапрофитные виды могут выступать конкурентами за питательные субстраты, антагонистами, продуцентами токсических веществ, включая пирогены.
12. Стадии биотехнологического процесса
Большое разнообразие биотехнологических процессов, нашедших промышленное применение, приводит к необходимости рассмотреть общие, наиболее важные проблемы, возникающие при создании любого биотехнологического производства. Процессы промышленной биотехнологии разделяют на 2 большие группы: производство биомассы и получение продуктов метаболизма. Однако такая классификация не отражает наиболее существенных с технологической точки зрения аспектов промышленных биотехнологических процессов. В этом плане необходимо рассматривать стадии биотехнологического производства, их сходство и различие в зависимости от конечной цели биотехнологического процесса. В общем виде система биотехнологического производства продуктов микробного синтеза представлена на рис. 3.
Существует 5 стадий биотехнологического производства.
Две начальные стадии включают подготовку сырья и биологически действующего начала. В процессах инженерной энзимологии они обычно состоят из приготовления раствора субстрата с заданными свойствами (рН, температура, концентрация) и подготовки партии ферментного препарата данного типа, ферментного или иммобилизованного. При осуществлении микробиологического синтеза необходимы стадии приготовления питательной среды и поддержания чистой культуры, которая могла бы постоянно или по мере необходимости использоваться в процессе. Поддержание чистой культуры штамма-продуцента – главная задача любого микробиологического производства, поскольку высокоактивный, не претерпевший нежелательных изменений штамм может служить гарантией получения целевого продукта с заданными свойствами.
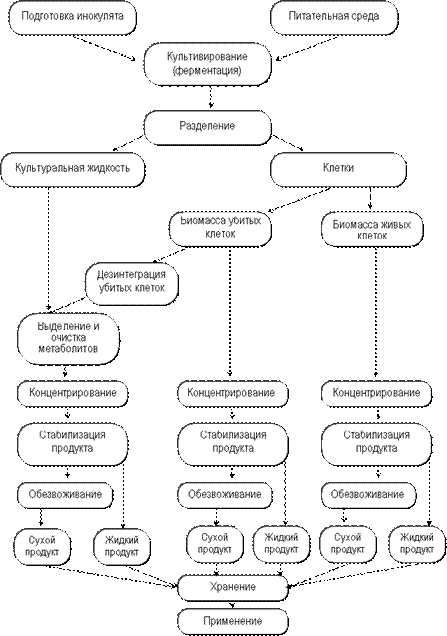
Рис. 3. Схема биотехнологического производства
Третья стадия – стадия ферментации, на которой происходит образование целевого продукта. На этой стадии идет микробиологическое превращение компонентов питательной среды сначала в биомассу, затем, если это необходимо, в целевой метаболит.
На четвертом этапе из культуральной жидкости выделяют и очищают целевые продукты. Для промышленных микробиологических процессов характерно, как правило, образование очень разбавленных растворов и суспензий, содержащих, помимо целевого, большое количество других веществ. При этом приходится разделять смеси веществ очень близкой природы, находящихся в растворе в сравнимых концентрациях, весьма лабильных, легко подвергающихся термической деструкции.
Заключительная стадия биотехнологического производства – приготовление товарных форм продуктов. Общим свойством большинства продуктов микробиологического синтеза является их недостаточная стойкость к хранению, поскольку они склонны к разложению и в таком виде представляют прекрасную среду для развития посторонней микрофлоры. Это заставляет технологов принимать специальные меры для повышения сохранности препаратов промышленной биотехнологии. Кроме того, препараты для медицинских целей требуют специальных решений на стадии расфасовки, так должны быть стерильными.
