
ФИЗИЧЕСКОЙ ХИМИИ
.pdfvk.com/club152685050 | vk.com/id446425943
43
Таблица 4
Нормальные окислительно-восстановительные потенциалы (Ео) по отношению к нормальному водородному электроду
|
E |
o |
|
|
0,000, B |
|
|
|
2H |
|
/ H |
|
|||
|
|
|
|
|
2 |
|
|
Окислитель |
+ne |
|
|
|
Восстановитель |
Ео, вольт |
|
Fe3+ |
+3e |
|
|
|
|
Fe |
-0,036 |
|
|
|
|
|
|
|
|
Cr3+ |
+3e |
|
|
|
|
Cr |
-0,71 |
Cr2O72-+14H+ |
+6e |
|
|
|
|
2Cr3+ + 7H2O |
+0,36 |
MnO4‾ +2H2О |
+3e |
|
|
|
|
MnО2 +4OН- |
+0,57 |
BrO3‾ + 3H2O |
+6e |
|
|
|
|
Br‾- + 6OH- |
+0,60 |
Fe3+ |
+e |
|
|
|
|
Fe2+ |
+0,77 |
BrO3‾ + 6H+ |
+6e |
|
|
|
|
Br‾ + 3H2O |
+1,44 |
MnO4‾ +8H+ |
+5e |
|
|
|
|
Mn2+ +4H2O |
+1,52 |
Co3+ |
+e |
|
|
|
|
Co2+ |
+1,84 |
Ce4+ |
+e |
|
|
|
|
Ce3+ |
+1,45 |
vk.com/club152685050 | vk.com/id446425943
44
Таблица 5
Численные значения коэффициента Стьюдента (для расчета границ доверительного интервала при доверительной
вероятности Р, объеме выборки n, числе степеней свободы f = n -1
n |
f |
Значение t при доверительной вероятности |
|||||
0,80 |
0,90 |
0,95 |
0,99 |
0,999 |
|||
|
|
||||||
2 |
1 |
3,08 |
6,31 |
11,07 |
63,7 |
636,62 |
|
3 |
2 |
1,89 |
2,92 |
4,30 |
9,92 |
31,60 |
|
4 |
3 |
1,64 |
2,35 |
3,18 |
5,84 |
12,94 |
|
5 |
4 |
1,53 |
2,13 |
2,78 |
4,60 |
8,61 |
|
6 |
5 |
1,48 |
2,02 |
2,57 |
4,03 |
6,86 |
|
7 |
6 |
1,44 |
1,94 |
2,45 |
3,71 |
5,96 |
|
8 |
7 |
1,42 |
1,90 |
2,36 |
3,50 |
5,41 |
|
9 |
8 |
1,40 |
1,86 |
2,31 |
3,36 |
5,04 |
|
10 |
9 |
1,38 |
1,83 |
2,26 |
3,25 |
4,78 |
|
11 |
10 |
1,37 |
1,81 |
2,23 |
3,17 |
4,59 |
|
12 |
11 |
1,36 |
1,80 |
2,20 |
3,11 |
4,49 |
|
13 |
12 |
1,36 |
1,78 |
2,18 |
3,06 |
4,32 |
|
14 |
13 |
1,35 |
1,77 |
2,16 |
3,01 |
4,22 |
|
15 |
14 |
1,35 |
1,76 |
2,14 |
2,98 |
4,14 |
|
16 |
15 |
1,34 |
1,75 |
2,12 |
2,95 |
4,07 |
|
17 |
16 |
1,34 |
1,75 |
2,11 |
2,92 |
4,02 |
|
18 |
17 |
1,33 |
1,74 |
2,10 |
2,90 |
3,97 |
|
19 |
18 |
1,33 |
1,73 |
2,09 |
2,88 |
3,92 |
|
20 |
19 |
1,33 |
1,73 |
2,09 |
2,86 |
3,88 |
|
21 |
20 |
1,33 |
1,73 |
2,09 |
2,85 |
3,85 |
|
22 |
21 |
1,32 |
1,72 |
2,08 |
2,83 |
3,82 |
|
23 |
22 |
1,32 |
1,72 |
2,07 |
2,82 |
3,79 |
|
24 |
23 |
1,32 |
1,71 |
2,07 |
2,81 |
3,77 |
|
25 |
24 |
1,32 |
1,71 |
2,06 |
2,80 |
3,75 |
|
26 |
25 |
1,32 |
1,71 |
2,06 |
2,79 |
3,73 |
|
27 |
26 |
1,32 |
1,71 |
2,06 |
2,78 |
3,71 |
|
28 |
27 |
1,31 |
1,70 |
2,05 |
2,77 |
3,70 |
|
29 |
28 |
1,31 |
1,70 |
2,05 |
2,76 |
3,67 |
|
30 |
29 |
1,31 |
1,70 |
2,05 |
2,76 |
3,66 |
|
31 |
30 |
1,31 |
1,70 |
2,04 |
2,75 |
3,65 |
|
41 |
40 |
1,30 |
1,68 |
2,02 |
2,70 |
3,55 |
|
61 |
60 |
1,30 |
1,67 |
2,00 |
2,66 |
3,46 |
|
121 |
120 |
1,29 |
1,66 |
1,98 |
2,62 |
3,37 |
|
|
|
1,28 |
1,64 |
1,96 |
2,58 |
3,29 |
|
|
|
|
|
|
|
|
|
vk.com/club152685050 | vk.com/id446425943
МЕТОДИЧЕСКАЯ РАЗРАБОТКА ПО АНАЛИТИЧЕСКИМ МЕТОДАМ ПОЛЯРОГРАФИИ И ВОЛЬТАМПЕРОМЕТРИИ ДЛЯ СТУДЕНТОВ, КОТОРЫЕ ЕЩЕ НЕ ПРОХОДИЛИ КУРС ФИЗИЧЕСКОЙ ХИМИИ.
Возникновение метода вольтамперометрии.
Аналитические методы вольтамперометрии и полярографии относятся к электрохимическим методам анализа. Полярография была открыта чехом Гейровским в конце 20-х годов, когда он изучал влияние напряжения, приложенного к ртутной капле,
погруженной в водный раствор, на величину поверхностного натяжения, (так называемый
«электрокапиллярный эффект», который мы здесь не проходим). Он заметил, что величина тока через каплю зависит от состава раствора. Доработав эту идею, он создал метод, который основан на измерении зависимости тока от напряжения на ртутно-
капельном электроде. Получающиеся зависимости, так называемые вольтамперные кривые или вольтамперограммы, зависят от состава раствора и позволяют проводить одновременно качественный и количественный анализ содержащихся в растворе микропримесей. Метод пощел «на-ура». В 1936 году за него была присуждена Нобелевская премия, высшая награда ученых.
Принцип метода.
Почему и каким образом вольтамперная характеристика ртутно-капельного электрода,
погруженного в раствор, зависит от концентрации растворенных веществ?
Протекание электрического тока в водном растворе связано с движением ионов,
образованных в результате электролитической диссоциации. Протекание тока через ртуть,
другие металлические и углеродные материалы – с движением электронов. Поэтому на границе электрод/раствор должен существовать какой-то процесс, обеспечивающий переход потока ионов в поток электронов, иначе ток не пойдет. Такой процесс представляет собой электрохимическую реакцию. Количество прореагировавшего вещества определяется законом Фарадея, то есть пропорционально прошедшему через электрод заряду:
М = Мэкв * Q/zF, |
(1) |
vk.com/club152685050 | vk.com/id446425943
Где М – масса прореагировавшего вещества, Мэкв – эквивалентная масса прореагировавшего вещества, Q - прошедший через электрод заряд, z- количество
электронов, участвующих в превращении одной молекулы или одного иона, F- число Фарадея, задающее коэффициент пропорциональности. Число Фарадея равно 96400
кулон/моль и представляет собою число Авогадро, умноженное на заряд электрона.
Если отнести уравнение (1) к единице времени, масса превратится в массовую скорость реакции (поток вещества) J, а заряд – в ток i, которые обычно относят к единице поверхности электрода (плотность тока):
J = Мэкв * i/zF, |
(2) |
Что нужно, чтобы измерить вольтамперограмму?
Для того, чтобы измерить вольтамперограмму, нужен спицальный прибор – полярограф или вольтамперометрический анализатор, или потенциостат, о которых пойдет речь ниже в разделе «Экспериментальные методы в вольтамперометрии». Кроме того, нужна электрохимическая ячейка, состоящая из корпуса, электродной системы и заполненная раствором фонового электролита, то есть раствором, в который добавлены соли, основания, кислоты, или другие добавки, создающие электропроводность и нужные параметры среды для успешного проведения анализа.
Почему ртуть?
Выбор ртутного электрода в первых вариантах полярографии не случаен. На ртутном электроде в водном растворе, содержащем электрохимически неактивные соли,
скажем, фторид натрия, в широком диапазоне напряжений не протекает никаких реакций,
связанных с протеканием тока через электрод. Поэтому, если мы прикладываем какое-то напряжение к ртутно-капельному электроду, ток остается нулевым, ведь никаких реакций на электроде нет. Такой электрод называется поляризуемым, от слова «поляризация», что в данном случае означает отклонение потенциала (напряжения) на электроде от равновесного значения. Возможность изменять напряжение позволяет измерить вольтамперограмму.
В качестве противоположного примера приводят обычно платиновый электрод в водном растворе. За счет высоких каталитических свойств платины при приложении отрицательных напряжений на платине выделяется водород с соответствующим протеканием тока (восстановление воды), а при приложении положительных потенциалов
– кислород (окисление воды) с соответствующим протеканием тока в одном и другом
vk.com/club152685050 | vk.com/id446425943
направлении. Поэтому невозможно произвольно менять напряжение на платиновом электроде в водном растворе, не создавая значительного тока. Такой электрод называется
«неполяризуемым». Для него нельзя произвольно изменять напряжение и измерить аналитическую вольтамперограмму
Капающий электрод позволяет все время обновлять поверхность датчика. Есть и некоторые другие достоинства ртутного электрода, связанные с химическими свойствами ртути. К сожалению все это несколько портится тем, что ртуть ядовита.
Как зависит вольтамперограмма от состава раствора. Форма полярографической
кривой.
Рассмотрим поведение ртутно-капельного электрода в водном растворе, где электропроводность создается электрохимически неактивным электролитом (фоном),
скажем, сульфатом калия. Пусть мы проводим изменение напряжения линейно во времени от нуля до сильно отрицательного значения, которое составляет в полярографии приблизительно -1,5. В. Если вещества и ионы в растворе отсутствуют, то вольтамперограмма такого электрода в растворе будет выглядеть, как это показано на рис.1, кривая 1. Ток почти нулевой, небольшое отклонение от нуля связано с тем, что при наложении напряжения поверхность электрода заряжается, как конденсатор,
концентрируя небольшое количество зарядов на своей поверхности.
Пусть теперь в раствор ввели соль меди, скажем, сульфат и равномерно размешали его по всему объему. Тогда на электроде появляется возможность протекания реакции
Cu+2 + 2e = Cu |
(3) |
Пусть в начале на электроде задано напряжение, которое недостаточно для разряда ионов меди. Снова проводим изменение напряжения линейно во времени от нуля до сильно отрицательного значения. В. В начальный момент времени распределение концентрации ионов меди в растворе не зависит от расстояния от поверхности электрода, обозначим его С0, (объемная концентрация). Пока напряжение изменяется в области, где реакция отсутствует, ток остается практически нулевым.
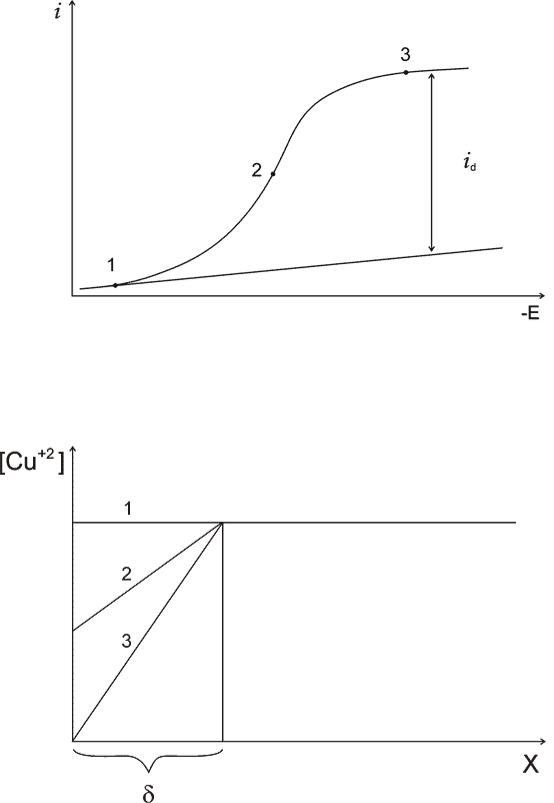
vk.com/club152685050 | vk.com/id446425943
Рис.1. Различные участки полярографической волны: область, где реакция практически отсутствует (1), область зависимости скорости реакции от потенциала (2) и диффузионная область (3).
Рис. 2. Распределение концентрации ионов меди около поверхности электрода,
соответствующее участкам 1, 2 и 3 вольтамперограммы, показанной на рис. 1.
По мере того, как мы подаем на электрод все более отрицательное
(восстановительное) напряжение, приближающееся к стандартному потенциалу восстановления меди, давление «электронного газа» увеличивается и он начинает
vk.com/club152685050 | vk.com/id446425943
заполнять имеющиеся полости, в данном случае, восстанавливать ионы меди по реакции
(3). Посмотрим, как это повлияет на вольтамперограмму. На вольтамперограмме возникнет дополнительный ток по сравнению со случаем, когда ионов меди нет. Его появление связано с тем, что электрод начнет поглощать ионы меди, находящиеся непосредственно на его поверхности, отдавая им электроны (электрон «прыгает» в
жидкости на 5-7 Ǻ). Диффузия ионов из объема будет компенсировать это поглощение. Из курса физической химии следует, что в начале кривой ток экспоненциально растет в зависимости от напряжения (уравнение Тафеля, которое мы не проходим в данном курсе).
В электрохимии выбирают гидродинамические условия таким образом, что у электрода устанавливается некоторое расстояние , в пределах которого концентрация линейно зависит от расстояния, то есть устанавливается стационарная диффузия. Это достигается либо путем задания постоянной скорости перемешивания, либо течения жидкости мимо электрода, либо путем использования электрода из капающей ртути, так что поверхность ртути все время движется определенным образом. Поэтому начальной части вольтамперной кривой соответствует распределение ионов в меди в растворе,
показанное на рис. 2. кривой 2. Следует обратить внимание, что концентрация ионов ртути вблизи поверхности электрода меньше, чем в объеме раствора, но не падает до нуля,
так как при таком напряжении разряд ионов меди на поверхности протекает не мгновенно,
а с некоторой задержкой. Величина этой задержки зависит от того, насколько велико отрицательное напряжение. Чем отрицательнее напряжение, тем меньше задержка. Для того, чтобы оценить величину тока при каком-то значении потенциала заметим, что диффузия ионов меди из раствора компенсирует разряд ионов меди, так что вблизи электрода устанавливается стационарное распределение ионов меди. Значит, скорость разряда ионов меди, связанная с величиной тока уравнением (2), компенсируется диффузией ионов меди к электроду, что описывается законом Фика:
Jдифф. = -D ∂C∕∂x = -D (С0- C)/ |
(4) |
Когда отрицательное напряжение увеличивается (по абсолютной величине) до такой степени, что концентрация меди на поверхности уменьшится до нуля, градиент концентрации ∂C∕∂x становится равен просто С0/ и дальнейшее увеличение (по абсолютной величине) отрицательного напряжения не приведет к увеличению тока. Все будет определяться диффузией. В стационарном состоянии J= Jдифф, поэтому из уравнений
(2) и (4) следует:
i = zF D С0/ |
(5) |
vk.com/club152685050 | vk.com/id446425943
Таким образом, вначале, когда отрицательное напряжение увеличивается ток растет экспоненциально, а затем выходит на предельное значение. Возникает характерная s-
образная кривая, получившая название «полярографической волны». В общем случае применяются не только ртутные электроды, но и электроды из различных углеродных материалов: пропитанного разными веществами (импрегнированного) графита,
стеклоуглерода, углеситалла, пирографита, золота, реже меди или амальгамированного серебра. В общем случаеметод называется вольтамперометрией, но за вольтамперометрией на ртутном электроде закрепился старый термин «полярография».
Какие существуют способы усиления сигнала в полярографии?
В 30-е годы метод полярографии триумфально шел по Европе и США, а в 50-е его стали забрасывать. Это было связано с тем, что предел обнаружения в описано выше
(классической) полярографии составляет примерно 10-5 моль/л, а точность 10-20%, хотя полярографисты любят утверждать, что у них точность 1%, что является чистым вымыслом. Для сравнения, точность 2% достигается при хорошем дозировании раствора пипеткой.) Таким образом, чувствительность метода была недостаточна для экологического и санитарного применения, где требуется определять микрограммы на литр раствора или на килограмм массы вещества, а точность недостаточна для технологического и арбитражного контроля, скажем, для идентификации образца разлитой нефти или расшифровки состава образца стали.
Однако в 80-е годы наблюдается новая волна подъема интереса к вольтамперометрии. В СССР и странах СЭВ существовал даже план обеспечить себя средствами анализа микроэлементов на этих принципах. Это было связано с тем, что появились новые методы усиления сигнала в вольтамперометрии, которые уменьшили предел обнаружения в методе до микрограммов на литр и даже до десятых долей микрограмма на литр. (Для сравнения, микрограмм весит карандашная галочка на бумаге).
Эти методы усиления: переменнотоковая полярография, инверсионная вольтамперометрия и каталитическая вольтамперометрия. Появление этих методов сделало вольтамперометрию приемлемой для большинства экологических и санитарных целей, где требуется высокая чувствительность метода, а требования к точности не очень высокая. Действительно, когда измеряется концентрация свинца в супе, человека волнует не то, что там 10 или 12 микрограммов на литр, а 10 микрограммов или 10 миллиграммов,
потому что при систематическом употреблении 10 миллиграммов смертельны, 10
микрограммов – нет.

vk.com/club152685050 | vk.com/id446425943
В чем сущность метода переменнотоковой вольтамперометрии?
Переменнотоковая вольтамперометрия заключается в том, что на медленную развертку напряжения на индикаторном (ртутном или другом) электроде накладывается переменная компонента, а ток фиксируется не весь, а только его переменная составляющая. Форма переменнотоковой составляющей напряжения может быть различная. Наиболее популярны гармоническая (синусоидальная) модуляция или модуляция прямоугольными ступеньками (меандр), реже встречается треугольник.
Почему при переходе к переменнотоковой вольтамперометрии полярографические волны превращаются в пики?
Пусть в постояннотоковой вольтамперометрии вольтамперограмма, то есть зависимость
тока i от напряжения E имеет какой-то вид: |
|
i = F(E) |
(6) |
Пусть модуляция напряжения задается законом: |
|
E= E(t) + Asin( t + ) |
(7) |
Тогда, при малой амплитуде А ток будет изменяться по следующему закону (учтено, что малое приращение тока определяется производной от тока по напряжению в точке E(t),
которую здесь обозначим ∂ F ∕∂ E:
i = F(E) = F[E(t) + Asin( t + )] = F [E(t)] + ∂ F ∕∂ E * Asin( t + 1 ) |
(8) |
|
Если теперь мы выберем только переменнотоковую компоненту тока, получим: |
|
|
iас = ∂ F ∕∂ E * Asin( t + 1 ) |
(9) |
|
Как видно, амплитуда переменного тока определяется |
производной от |
тока по |
напряжению. Для полярографической волны зависимость такой производной от
напряжения имеет вид пика (рис.3), максимум которого по оси напряжений совпадает с точкой перегиба полярографической волны. Таким образом, при переходе к переменнотоковой полярографии полярографические волны превращаются в пики (рис.3).

vk.com/club152685050 | vk.com/id446425943
Рис. 3. Соотношение постояннотоковой (DC) и переменнотоковой (AC)
вольтамперограмм. Максимум переменнотоковой полярограммы соответствует точке перегиба постояннотоковой .
По некотором причинам, которые проходят в курсе физической химии, это позволяет увеличить чувствительность в 100-1000 раз по сравнению с постояннотоковой вольтамперометрией. Это позволило достичь чувствительности порядка 1 мкг/л раствора при определении многих тяжелых металлов и порядка 1 мг/л при определении некоторых органических соединений, что снова вызвало подъем интереса к методу вольтамперометрии.
В чем сущность метода инверсионной вольтамперометрии? Из каких стадий он
состоит?
Еще более высокие чувствительности были достигнуты при появлении инверсионных, или накопительных, методов анализа в вольтамперометрии. Метод инверсионной вольтамперометрии (ИВА) заключается в том, что определяемое вещество первоначально в какой-то форме накапливают на поверхности электрода, а затем проводят развертку напряжения, сопровождающуюся появлением измеряемого сигнала. Опишем,
например, как используется этот прием при определении меди, свинца, кадмия и цинка методом ИВА (самый распространенный вид анализа в этой области, тем более, что перечисленные элементы можно определять одновременно).
Первоначально на электрод подается сильное отрицательное напряжение (скажем, -
1400 мВ, и все перечисленные металлы начинают выделяться в свободном виде на
