
ЭКСПЛУАТАЦИЯ КОМПРЕССОРНЫХ СТАНЦИЙ МАГИСТРАЛЬНЫХ ГАЗОПРОВОДОВ
.pdfvk.com/club152685050 | vk.com/id446425943
скорость распространения пламени достигает сотни метров в секунду. Например, температура самовоспламенения метановоздушной смеси находится на уровне 700 °С, а метан является основным компонентом природного газа. Его содержание в газовых месторождениях колеблется в диапазоне 92-98%.
При взрыве газовоздушной смеси, находящейся под давлением 0,1 МПа, развивается давление около 0,80 МПа. Газовоздушная смесь взрывается, если в ней содержится 5-15 % метана; 2-10 % пропана; 2-9 % бутана и т.д. При повышении давления газовоздушной смеси пределы взрываемости сужаются. Следует отметить, что примесь кислорода в газе увеличивает опасность взрыва.
Пределы и интервал взрываемости газов в смеси с воздухом при температуре 20 °С и давлении 0,1 МПа приведены в табл. 1.4.
Таблица 1.4
Пределы и интервал взрываемости газов в смеси с воздухом при температуре 20 °С и давлении 0,1 МПа
Газ |
Пределы взрываемости, % |
Интервал |
|
|
по объему |
взрываемости, % по |
|
|
|
|
объему |
|
нижний |
верхний |
|
Ацетилен |
2,3 |
82,0 |
79,7 |
Бутан |
1,5 |
8,5 |
7,0 |
Бутилен |
1,7 |
9,0 |
7,3 |
Водород |
4,0 |
75,0 |
71,0 |
Метан |
5,0 |
15,0 |
10,0 |
Нефтепромысл. газ |
4,0 |
14,0 |
10,0 |
Оксид углерода |
12,5 |
75,0 |
62,5 |
Природный газ |
5,0 |
15,0 |
10,0 |
Пропан |
2,0 |
9,5 |
7,5 |
Пропилен |
2,2 |
9,7 |
7,5 |
Этан |
3,0 |
14,0 |
11,0 |
Этилен |
3,0 |
33,3 |
30,3 |
1.2. Законы идеальных газов. Области их применения
Идеальными газами принято считать газы, подчиняющиеся уравнению Клапейрона ( Pv RT ). Одновременно под идеальными подразумеваются газы, в которых отсутствуют силы межмолекулярного взаимодействия, а объем самих молекул равен нулю. В настоящее время можно утверждать, что ни один из реальных газов не подчиняется этим газовым законам. Тем не менее эти специфические газовые законы достаточно широко используются в технических расчетах. Эти законы просты и достаточно хорошо характеризуют поведение реальных газов при невысоких давлениях и не очень низких температурах, вдали от областей насыщения и критических точек вещества. Наибольшее практическое распространение получили законы Бойля-Мариотта, Гей-Люссака, Авогадро и на их основе полученное уравнение Клапейрона-Менделеева.
Закон Бойля-Мариотга утверждает, что при постоянной температуре ( t = const) произведение
абсолютного давления и удельного объема идеального газа сохраняет постоянную величину ( Pv = const), т.е. произведение абсолютного давления и удельного объема зависит только от температуры.
Откуда при t = const имеем: |
|
|
|
P v |
2 |
P v . |
(1.27) |
2 |
1 1 |
|
Закон Гей-Люссака утверждает, что при постоянном давлении ( P = const) объем идеального газа

vk.com/club152685050 | vk.com/id446425943
изменяется прямо пропорционально повышению температуры:
|
|
|
v v (1 t) , |
|
|
(1.28) |
||
|
|
|
0 |
|
|
|
|
|
где v - удельный объем газа при температуре t °С и давлении |
P;v |
0 |
- удельный объем газа при |
|||||
|
|
|
|
|
|
|
|
|
температуре |
t |
0 |
= 0 °С и том же давлении |
P ; |
- температурный коэффициент объемного |
|||
|
|
|
|
|
|
|
|
|
расширения идеальных газов при 0 °С, сохраняющий одно и то же значение при всех давлениях и одинаковый для всех идеальных газов:
|
1 |
К-1 . |
(1.29) |
|
|
||||
273,16 |
||||
|
|
|
Таким образом, содержание закона Гей-Люссака сводится к следующему утверждению: объемное
расширение идеальных газов при изменении температуры и при P = const имеет линейный характер, а температурный коэффициент объемного расширения является универсальной постоянной идеальных газов.
Сопоставление законов Бойля-Мариотта и Гей-Люссака приводит к уравнению состояния идеальных газов:
Pv RT
,
(1.30)
где v - удельный объем газа; P - абсолютное давление газа; идеального газа; T - абсолютная температура идеального газа:
R - удельная газовая постоянная
T
P R
t 1/
t
273,2
.
(1.31)
Физический смысл удельной газовой постоянной R - это удельная работа в процессе P = const при изменении температуры на один градус.
Закон Авогадро утверждает, что объем одного моля идеального газа v не зависит от природы газа и вполне определяется давлением и температурой вещества ( P,T ). На этом основании
утверждается, что объемы молей разных газов, взятых при одинаковых давлениях и температурах, равны между собой. Если v - удельный объем газа, а - мольная масса, то объем моля (мольный
объем) равен v v . При равных давлениях и температурах для разных газов имеем:
v v RT / P
f (P,T ) const
.
(1.32)
|
объем газа |
|
зависит в общем случае только |
Так как удельный мольный |
v |
||
температуры, то произведение |
R в уравнении (1.32) - есть величина одинаковая |
||
поэтому называется универсальной газовой постоянной:
от давления и для всех газов и
|
|
R 8314 , Дж/кмоль·К. |
|
|
|
||||
R |
(1.33) |
|
|
||||||
Из уравнения (1.33) следует, что удельные газовые постоянные отдельных газов |
R |
определяются |
|||||||
через их мольные массы. Например, для азота ( N2 ) удельная газовая постоянная будет |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
R |
R |
|
|
|
||||
|
|
|
|
= 8314/28 = 297 Дж/(кг·К). |
(1.34) |
|
|
||
|
|
|
|
|
|
||||
|
|
|
N |
|
|
|
|||
|
|
|
2 |
|
|
|
|
||

vk.com/club152685050 | vk.com/id446425943
Для
G
кг газа с учетом того, что
Gv V
, уравнение Клапейрона записывается в виде:
|
|
PV G RT GRT , |
(1.35) |
||
где |
|
- количество вещества в молях G G / . Для 1 кмоля газа: |
|
||
G |
|
||||
|
|
|
|
||
|
|
Pv RT |
R |
T . |
(1.36) |
Последнее уравнение, полученное русским ученым Д.И. Менделеевым, часто называют уравнением Клапейрона-Менделеева.
Значение мольного объема идеальных газов в нормальных физических условиях ( 101,1 кПа) составит:
t
= 0 °С и P =
v |
RT |
|
P |
||
|
8314 273,16 |
|
101,1 10 |
3 |
|
|
= 22,4 м
3
/кмоль.
(1.37)
Уравнение состояния реальных газов часто записывают на основе уравнения Клапейрона с
введением в него поправки |
z , учитывающей отклонение реального газа от идеального |
|||
|
|
Pv zRT , |
(1.38) |
|
где |
z |
- коэффициент |
сжимаемости, определяемый |
по специальным номограммам или из |
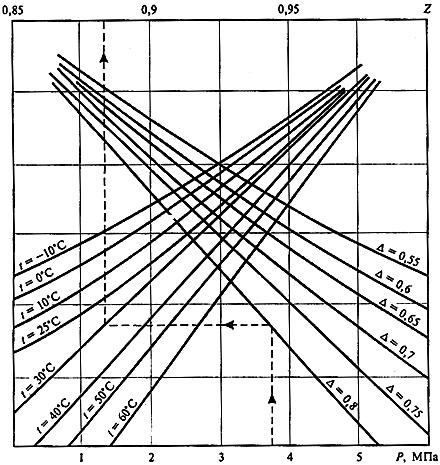
соответствующих таблиц. На рис. 1.1 приведена номограмма для определения численных значений
величины |
z |
природного газа в зависимости от давления |
P , относительной плотности газа по |
воздуху и его температуры t . В научной литературе коэффициент сжимаемости |
z |
обычно |
|
определяется в зависимости от так называемых приведенных параметров (давление и температура) газа:
P /
Pкр
;
PT
/ Tкр
,
(1.39)
где |
, |
P |
и |
P |
- соответственно приведенное, абсолютное и критическое давление газа; |
кр |
Tкр - соответственно приведенная, абсолютная и критическая температура газа.
,
T
и
vk.com/club152685050 | vk.com/id446425943
Рис. 1.1. Номограмма расчёта z в зависимости от
P
, , t
Критическим давлением называется такое давление, при котором и выше которого никаким повышением температуры жидкость уже не может быть превращена в пар.
Критической температурой называется такая температура, при которой и выше которой ни при каком повышении давления нельзя сконденсировать пар.
Численные значения критических параметров для некоторых газов приведены в табл. 1.5.
Таблица 1.5
Критические параметры некоторых веществ
Вещество |
Критическая |
Критическое давление |
|
|
|
температура t кр , °С |
Pкр , МПа |
Азот, N 2 |
|
- 149,9 |
3,34 |
|
|
|
|
Кислород, О |
2 |
-118,4 |
0,51 |
|
|
||
Метан, СН 4 |
|
-82,6 |
4,60 |
|
|
|
|
Этан, С 2 Н 6 |
|
32,3 |
4,80 |
|
|
|
|

vk.com/club152685050 | vk.com/id446425943
Пропан, С |
3 |
Н |
8 |
96,7 |
|
|
4,20 |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
Аммиак, NH |
|
132,3 |
|
|
1,13 |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
Пентан, С |
5 |
Н |
12 |
197,2 |
|
|
0,33 |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|||||||
Вода, Н |
2 |
O |
|
|
374,15 |
|
|
2,21 |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Воздух |
|
|
|
|
|
-140,7 |
|
|
0,38 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
Пример 1.3. Определить количество метана как идеального газа в резервуаре объемом 50 м |
при |
|||||||||||||
|
||||||||||||||
следующих условиях: температура газа в резервуаре |
t |
= 20 °С, манометрическое (избыточное) |
||||||||||||
давление в резервуаре - 5,1 МПа, абсолютное давление в помещении |
P |
= 99,08 кПа. |
|
|
||||||||||
Решение. Абсолютная температура газа в резервуаре
T T |
t |
0 |
|
Абсолютное давление газа в резервуаре
= 273,16 + 20 = 293,16 К.
P P |
P |
m |
0 |
Удельная газовая постоянная метана
= 5,1 + 99,08 · 10
3
= 5,2 МПа.
R
Плотность метана в баллоне
R
/
= 8314/16,04 = 518,36 Дж/(кг К).
|
P |
|
RT |
||
|
1 v
5,2 10 |
6 |
|
|
518,36 273,16 |
|
= 34,22 кг/м
3
Количество метана в резервуаре
G ·V
34,22 · 50 =1711 кг.
1.3.Технологические характеристики природных газов и их компонентов
Вприродных газах чисто газовых месторождений страны основным компонентом смеси является метан СН 4 , содержание которого в смеси составляет от 92 до 98% по объему. Остальные 2-8%
приходится на "производные" метана - гомологи метана и азота. Как отмечалось выше, кроме чисто газовых месторождений, имеются так называемые газоконденсатные месторождения. Конденсат состоит из легких бензиновых фракций и сжиженных углеводородных газов, обладающих способностью к выпадению из смеси.
Кроме двух названных типов газовых месторождений, различают еще понятие нефтепромысловых газов, сопутствующих месторождениям нефти. Содержание метана в таких газах колеблется от 30 до 90% по объему. Этот газ выделяется из нефти, поднимаемой на поверхность, в специальных
ловушках-трапах. Обычно в 1 тонне добываемой нефти содержится 200-400 м 3 газа при нормальных физических условиях.
Теплофизические свойства метана, содержащегося в большом количестве в природных газах,
vk.com/club152685050 | vk.com/id446425943
перекачиваемых по газопроводам, практически полностью и определяют свойства природных газов.
Метан СН |
4 |
- наиболее легкий из углеводородов, плотность его при нормальных физических |
||
|
|
|
|
|
условиях составляет 0,717 кг/м |
3 |
. Отношение его плотности к плотности воздуха равно 0,554. |
||
|
||||
Метан - это бесцветный газ, не имеющий запаха. Он нетоксичен, но при большой концентрации в воздухе вызывает удушье. При давлении 0,1 МПа и температуре - 162°С он сжижается.
Вслед за метаном в гомологическом ряду идет этан С |
2 |
Н |
6 |
. По плотности этот газ близок к |
|
|
|
воздуху; при давлении 0,1 МПа и температуре 20 °С он может рассматриваться как идеальный газ. В природных газах чисто газовых месторождений содержатся лишь доли процента этана. Увеличение содержания этана в составе природного газа повышает его теплоту сгорания. В соответствии с этим этан является ценным компонентом газообразования топлива.
Следующий насыщенный углеводород - пропан С 3 H 6 . Пропан в 1,5 раза тяжелее воздуха.
Различие в составе пропана и этана сводится к наличию в молекуле пропана одной группы СН
2
.
Каждый последующий углеводород данного гомологического ряда отличается от предыдущего на
одну группу СН
2
, называемую группой гомологической разности. Пропан содержится в сравнительно
незначительном количестве в природных газах чисто газовых месторождений. Значительно больше его содержится в природных газах газоконденсатных месторождений.
Пропан легко сжижается. Температура сжижения его при атмосферном давлении равна -43 °С. При снижении давления сжиженный пропан легко испаряется, что позволяет хранить и транспортировать его в сжиженном виде при небольшом давлении, а перед использованием регазифицировать и сжигать в газообразном состоянии.
Бутан С 4 Н
10
- газ, имеющий два изомера - н. бутан и изобутан. Оба изомера при давлении 0,1
МПа легко переходят в жидкое состояние. При этом давлении н. бутан становится жидкостью при температуре - 0,5°С, а изобутан при температуре - 10,5°С. Следовательно, бутан, как и пропан, легко сжижаются и составляют основу сжиженных углеводородных газов. Парциальные давления этана, пропана и бутана очень малы, и в газовой смеси они могут рассматриваться как идеальные газы.
Кроме углеводородов, в состав природных газов входят негорючие газы, к которым относятся азот, диоксид углерода, или углекислый газ, и кислород.
Азот N
2
является двухатомным бесцветным газом, не имеющим запаха и вкуса. Азот практически
не реагирует с кислородом, поэтому его рассматривают как инертный газ. В большинстве природных газов его содержание составляет 0,5-3%.
Диоксид углерода СО
2
является бесцветным тяжелым газом со слегка кисловатым запахом и
вкусом. Этот газ не способен к горению. При высоком содержании углекислого газа в воздухе (5-10% по объему) этот газ вызывает удушье. Содержание диоксида углерода в природном газе обычно не превышает 1% по объему.
При давлении 0,1 МПа диоксид углерода, минуя жидкое состояние, переходит в твердое состояние при температуре - 78 °С. Твердый диоксид углерода называют сухим льдом и используют для хранения пищевых продуктов.
Кислород О 2 является бесцветным газом |
без |
запаха и вкуса. Плотность кислорода |
при |
|
нормальных физических условиях равна 1,34 |
кг/м |
3 |
. В процессе горения кислород играет |
роль |
|
||||
окислителя. Примесь кислорода в газообразном топливе допускается не более 1 % по объему как по соображениям взрывобезопасности, так и в целях предохранения оборудования от коррозии.
vk.com/club152685050 | vk.com/id446425943
1.4. Термодинамическое обеспечение решения энерготехнологических задач трубопроводного транспорта природных газов
В теплотехнических расчетах процессов трубопроводного транспорта газа и определении показателей работы газоперекачивающих агрегатов используется большой набор
термодинамических величин: плотность газа, изобарная (
Ср
) и изохорная (
Сv
) теплоемкости,
коэффициент Джоуля-Томсона
Dh
коэффициент Джоуля-Гей-Люссака
Du
и ряд показателей
термодинамических процессов, таких как адиабатический, изоэнтальпийный, изотермический и др.
Теплотехнические характеристики природных газов обычно определяют с использованием уравнения состояния и дифференциальных соотношений термодинамики, связывая соответствующие параметры процесса с независимыми переменными уравнения состояния.
Определение характеристик природных газов всегда можно полностью осуществить, если исходные параметры позволяют определить удельную работу в рассматриваемом процессе.
Действительно, из уравнения первого начала термодинамики для адиабатического процесса ( g
= 0) следует: |
|
g dh |
(1.40) |
при
или
g 0, |
dh |
|
|
h |
h |
1,2 |
1 |
2 |
(1.41)
(1.42)
Для реального газа его энтальпия ( h ) определяется как функция двух переменных - температуры
( t ) и давления ( P ), |
h h(t, P) ; для идеальных газов - как функция только одной температуры ( t ), |
h h(t) . |
|
В связи с этим для реального газа, когда энтальпия h h(t, P) , удельная работа в интегральной форме будет определяться соотношением:
|
|
|
h C |
Pm |
(t |
2 |
t ) (C |
P |
D )(P |
P ) , (1.43) |
|
|
|
|
|
|
|
1 |
h |
2 |
1 |
|
|||
где t |
и t |
2 |
- начальная и конечная температуры процесса соответственно; P |
и P - начальное и |
||||||||
1 |
|
|
|
|
|
|
|
|
|
1 |
2 |
|
конечное давление газа в процессе, соответственно; Dh - коэффициент Джоуля-Томсона или характеристика дроссельного процесса, показывающая изменение температуры газа при изменении
его давления в изоэнтальпийном (дроссельном) процессе (
h
= const).
Для идеальных газов эта величина равна нулю и, следовательно, удельная работа по уравнению (1.43) для идеальных газов будет определяться только первым слагаемым правой части:
h CPm (t2 t1) . |
(1.44) |
Численные значения коэффициента Джоуля-Томсона для метана приведены в табл. 1.6.
Таблица 1.6
Значение коэффициента Джоуля-Томсона ( Dh ) для метана в зависимости от
vk.com/club152685050 | vk.com/id446425943
температуры и давления
Давление, |
|
Значение Dh |
(°С/МПа) при температуре t , °С |
||||
|
|
|
|
|
|
|
|
МПа |
-25 |
|
0 |
25 |
50 |
75 |
100 |
|
|
|
|
|
|
|
|
0,10 |
5,6 |
|
4,8 |
4,1 |
3,5 |
3,0 |
2,6 |
|
|
|
|
|
|
|
|
0,52 |
5,5 |
|
4,7 |
4,0 |
3,4 |
3,0 |
2,6 |
|
|
|
|
|
|
|
|
2,50 |
5,0 |
|
4,3 |
3,6 |
3,1 |
2,6 |
2,3 |
|
|
|
|
|
|
|
|
5,15 |
4,5 |
|
3,8 |
3,3 |
2,8 |
2,4 |
2,1 |
|
|
|
|
|
|
|
|
10,3 |
3,6 |
|
3,2 |
2,7 |
2,5 |
2,1 |
1,9 |
|
|
|
|
|
|
|
|
Положительное значение коэффициента Джоуля-Томсона характеризует дросселирование большинства природных газов при обычных температурах и давлениях. Поэтому при движении газа через разные сопротивления (регулирующие клапаны, фильтры и т.п.), особенно при резком падении давления, снижается и его температура, что вызывает обмерзание трубопроводов, запорных, регулирующих и измерительных устройств. Это явление и называют эффектом дросселирования.
Следует отметить, что при некоторых условиях дросселирование сопровождается и нагреванием газа. Коэффициент Джоуля-Томсона в этом случае принимает отрицательное значение.
При решении ряда технологических задач, в частности при построении приведенных характеристик центробежных нагнетателей, в расчетах процессов сжатия необходимо располагать
скорее не первичными термодинамическими величинами С p ,Cv , Dh , Du , а их комплексами
С p Dh , Cv Du , Pv и др.
Использование указанных комплексов не только упрощает проведение расчетов, но и позволяет в каждом конкретном случае выбрать правильный подход к их осреднению в данном процессе, избежать дополнительной ошибки при построении комплекса по осредненным величинам, например
C |
pm |
D |
|
hm |
Комплекс
и т.д.
C |
p |
D |
h |
|
|
для реальных газов зависит главным образом от температуры. Для природных
газов с содержанием метана в диапазоне 90-100% можно пользоваться следующим эмпирическим уравнением для его определения:
|
|
|
|
|
|
C p Dh (C p Dh )СН4 (1,37 0,37 rСН4 ) , (1.45) |
|
где |
r |
|
- мольное содержание метана в газе, доли единицы. |
||||
|
СН |
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
Имея значение |
C |
p |
D |
h для реальных газов, несложно определить, например, работу сжатия газа |
|||
|
|
||||||
в нагнетателе по уравнению (1.43), имея данные о перепаде температур и давлений газа по нагнетателю.
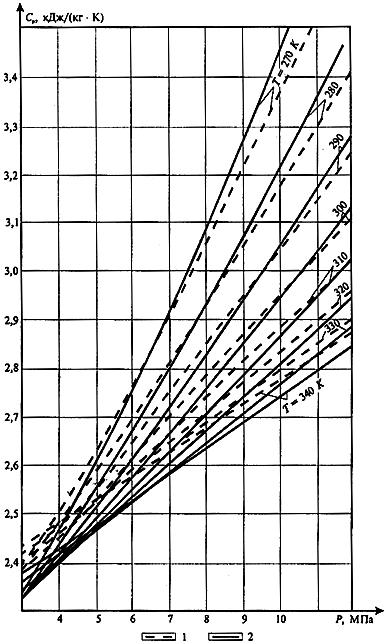
На рис. 1.2-1.5 приведены основные термодинамические величины и комплексы, обычно используемые при проведении теплотехнических расчетов, связанных с транспортом природного газа по газопроводу. Именно поэтому диапазон изменения давлений и температур для них выбран применительно к условиям, характерным для режимов работы магистральных газопроводов.
Диаграммы на рис. 1.2-1.5 построены для двух составов природного газа. Первый состав, отраженный на диаграммах штриховой линией, состоит из метана - 98,6%, пропана - 0,2%, бутана -
vk.com/club152685050 | vk.com/id446425943
0,15%, н. бутана - 0,05%, азота - 1%. Газ второго состава, отраженный на диаграммах сплошной линией, содержит метана - 94,36%, этана - 2,2%, пропана -1,2%, н.бутана - 0,5%, н.пентана - 0,2%, азота - 0,7%, кислорода - 0,5%, диоксида углерода - 0,4%.
Рис. 1.2. Зависимость изобарной теплоемкости |
С |
р |
от давления P и температуры |
|
природных газов первого (1) и второго (2) составов
T
для
vk.com/club152685050 | vk.com/id446425943
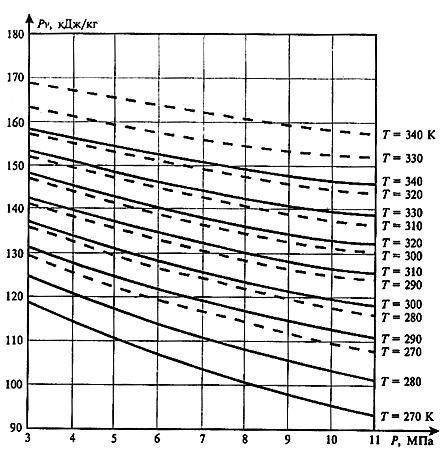
Рис. 1.3. Зависимость потенциальной функции |
Pv |
от давления |
P |
и температуры |
газов первого (пунктир) и второго (сплошная линия) составов
T
для природных
Данные по промежуточным составам газов можно получить обработкой соответствующих величин по простейшим интерполяционным зависимостям.
Все основные термодинамические характеристики природных газов при различных значениях температур и давлений, характерных для режимов работы магистральных газопроводов, приведены
в табл. 1.7 и 1.8, в
сжимаемости газа, |
|
которых |
P |
- давление (МПа), k |
- показатель |
||||
|
|||||||
- плотность газа (кг/м |
3 |
), |
h |
- энтальпия (кДж/кг), |
|||
|
|||||||
адиабаты, z - коэффициент
Pv - потенциальная функция,
равная zRT (кДж/кг), |
C |
р |
- изобарная теплоемкость кДж/(кг°С), |
|
|
||||
D |
- коэффициент Джоуля-Томсона (°С/МПа). |
|||
h |
|
|
|
|
С D |
h |
р |
- комплекс (кДж/кг·МПа),
