
II cеместр 2002/03 учебного года. Контрольная работа n1. Вариант 1.
1. Напишите уравнения следующих химических превращений:
(NH4)2CO3, изб. to CH3COOH лед.
B



 eSO4 Be(OH)2 BeCl2 X1 X2
. . .
eSO4 Be(OH)2 BeCl2 X1 X2
. . .


 H2O .
. .
H2O .
. .
K
 KO3 Y
KO3 Y
Xi -вещества, содержащие Be, Yi -вещество, содержащее K. (8 баллов)
2. Изобразите схематически на графике в координатах (DгидратацииНо298 M+(газ) - порядковый номер М), как изменяются значения DгидратацииНо298 ионов щелочных металлов (М=Li - Cs). Объясните эту закономерность. (3 балла)
3. При температуре 357 К равновесное давление р(О2) над надпероксидом калия составляет 0.2 атм. Используя данные таблицы, определите энергию кристаллической решетки пероксида калия. Считайте, что DrН0 и DrS0 не зависят от температуры.
Вещество |
DfН0, кДж/моль |
S0, Дж /моль*К |
Вещество |
DfН0, кДж/моль |
S0,Дж /моль*К |
C газ C алмаз C графит CO газ COCl2 газ CO2 газ Н газ Н+ газ Н+ р-р Н2 газ H2O газ H2Oж. |
712.5 1.8 0 -110.5 -220.3 -393.51 218.0 1536.2 0 0 -241.8 -285.8 |
158.0 2.4 5.7 197.6 283.9 213.8 114.6 108.8 0 132.1 188.7 70.1 |
O газ O2 газ O2- газ O22- газ OH- р-р K газ K крист. K+ газ K+ р-р KNO3 крист. KО2 крист. K2О2 крист. |
246.8 0 834.6 702.1 -230.2 89.2 0 514.7 -252.2 -446.7 -285.3 - |
160.9 205.0 - - -10.9 - 64.7 - 101.0 116.0 46.9 113.0 |
(7 баллов)
4. На рис.1 приведена схема фазовой диаграммы двухкомпонентной системы KF - CaF2.
1) Рассчитайте состав соединения, образующегося в системе.
2) Сколько фаз и какие находятся в равновесии в т.т. 1, 2?
3) На рис.2 приведены сечения кубической элементарной ячейки соединения. Определите соотношение катионов и анионов в химической формуле этого соединения. Какое из трех соединений, представленных на диаграмме, имеет данную структуру? Определите координационные числа и полиэдры анионов и катионов в этой структуре.
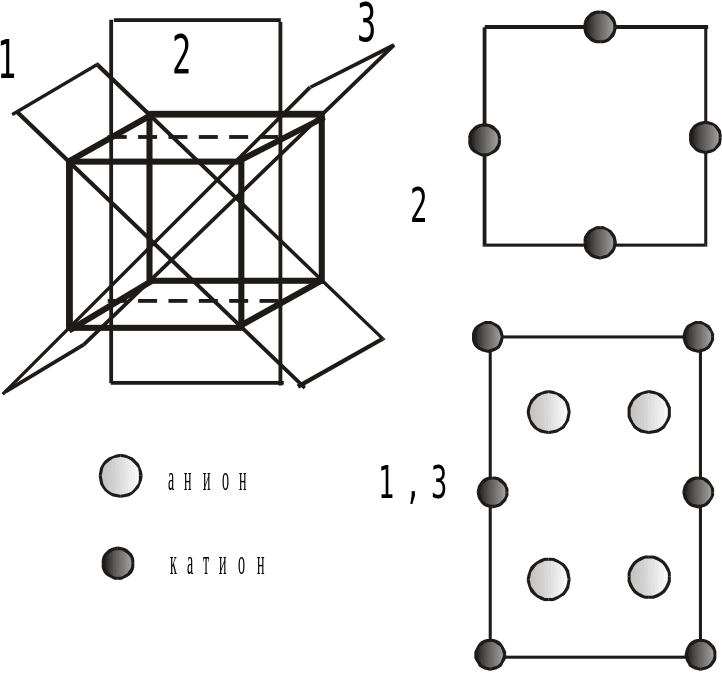
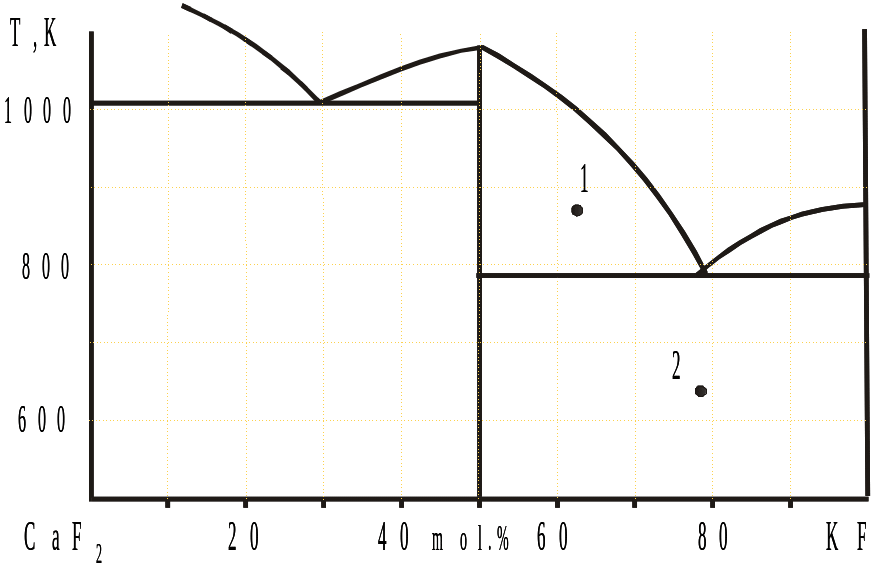 Рис.1 Рис.2 (7
баллов)
Рис.1 Рис.2 (7
баллов)
II cеместр 2002/03 учебного года. Контрольная работа n1. Вариант 2.
1. Напишите уравнения следующих химических превращений: H2O
N




 a2SO4
Na2S X1 X2 X3 Na2O2 .
. .
a2SO4
Na2S X1 X2 X3 Na2O2 .
. .

 AlCl3,p-p
AlCl3,p-p
. . . MgCl2 MgCO3

Mg
Xi -вещества, содержащие Na. (8 баллов)
2. Изобразите схематически на графике в координатах (DатомизацииНо298M(тв.) - порядковый номер М), как изменяются величины D атомизацииНо298 щелочных металлов (М=Li - Cs)? Объясните эту закономерность. (3 балла)
3. Энергия кристаллической решетки ВаО равна 3127 кДж/моль. Используя данные таблицы, определите, при какой температуре пероксид бария будет разлагаться, если равновесное давление кислорода р(О2) над ним составляет 0.2 атм?. Считайте, что DrН0 и DrS0 не зависят от температуры.
Вещество |
DfН0, кДж/моль |
S0, Дж /моль*К |
Вещество |
DfН0, кДж/моль |
S0, Дж /моль*К |
C газ C алмаз C графит CO газ COCl2 газ CO2 газ Н+ газ Н+ р-р Н2 газ H2O газ H2Oж. |
712.5 1.828 0 -110.5 -220.3 -393.51 1536.2 0 0 -241.8 -285.8 |
158.0 2.4 5.7 197.6 283.9 213.8 108.8 0 132.1 188.7 70.1 |
O газ O2 газ O22- газ O2- газ OH- р-р Ba газ Ba2+ газ Ba2+ р-р BaCO3 крист. BaO2 крист. BaО крист. |
246.8 0 702.1 834.6 -230.2 174.6 1790.6 -538.0 -1291.1 -629.7 - |
160.9 205.0 - - -10.9 170.1 - 9.6 112.0 98.8 70.3 |
(7 баллов)
4. На рис.1 приведена схема фазовой диаграммы двухкомпонентной системы TlCl-PbCl2.
1) Рассчитайте состав соединения, образующегося в системе.
2) Сколько фаз и какие находятся в равновесии в т.т. 1, 2?
3) На рис.2 приведены сечения кубической элементарной ячейки соединения. Определите соотношение катионов и анионов в химической формуле этого соединения. Какое из трех соединений, представленных на диаграмме, имеет данную структуру? Определите координационные числа и полиэдры анионов и катионов в этой структуре.
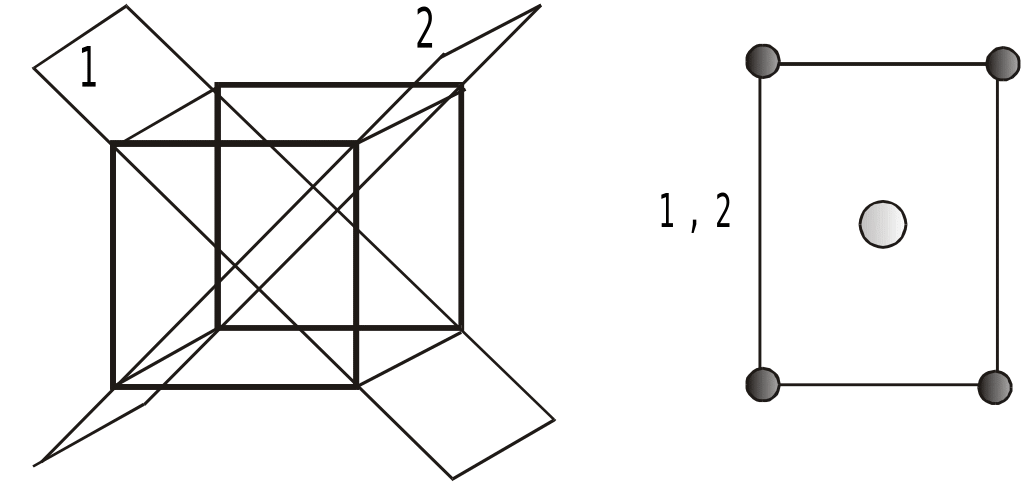
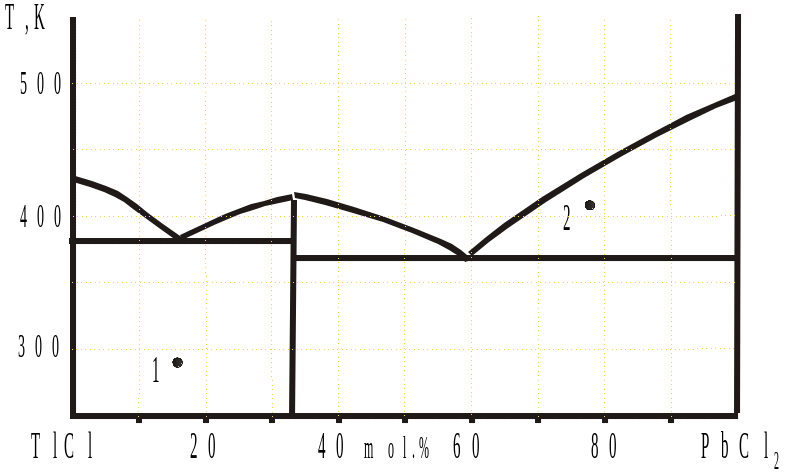 Рис.1 Рис.2 (7
баллов)
Рис.1 Рис.2 (7
баллов)
II cеместр 2002/03 учебного года. Контрольная работа N1. Вариант 3.
1. Напишите уравнения следующих химических превращений:
to H2SO4,p-p
B



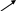 a(NO3)2 X1 X2 Ba
BaO2 . . .
a(NO3)2 X1 X2 Ba
BaO2 . . .


 to
to
K
 Cl KOH K2CO3 Y .
. .
Cl KOH K2CO3 Y .
. .
Xi -вещества, содержащие Ba, Y -вещество, содержащее K. (8 баллов)
2. Изобразите схематически на графике (DионизацииНо298 M(газ.) - порядковый номер М), как изменяются величины DионизацииНо298 щелочных металлов (М= Li - Cs). Объясните эту закономерность. (3 балла)
3. При температуре 514 К равновесное давление р(H2O) над гидроксидом магния составляет 0.5 атм. Используя данные таблицы, определите энергию кристаллической решетки оксида магния. Считайте, что DrН0 и DrS0 не зависят от температуры.
Вещество |
DfН0, кДж/моль |
S0, Дж /моль*К |
Вещество |
DfН0, кДж/моль |
S0 Дж /моль*К |
C газ C алмаз C графит CO газ COCl2 газ CO2 газ Н газ Н+ газ Н+ р-р Н2 газ H2O газ
|
712.5 1.828 0 -110.5 -220.3 -393.51 218.0 1536.2 0 0 -241.8
|
158.0 2.4 5.7 197.6 283.9 213.8 114.6 108.8 0 132.1 188.7 |
H2O ж. O газ O2 газ O2- газ OH- р-р Mg газ Mg крист. Mg2+ газ Mg2+ р-р MgCO3 крист. Mg(OH)2 крист. MgО крист. |
-285.8 246.8 0 834.6 -230.2 146.4 0 2373.0 - -1113.1 -924.9 - |
70.1 160.9 205.0 - -10.9 148.5 32.7 - -138.0 26.9 63.1 26.9 |
(7 баллов)
4. На рис.1 приведена схема фазовой диаграммы двухкомпонентной системы Li2O - WO3.
1) Рассчитайте состав соединения, образующегося в системе.
2) Сколько фаз и какие находятся в равновесии в т.т. 1, 2?
3) На рис.2 приведены сечения кубической элементарной ячейки соединения. Определите соотношение катионов и анионов в химической формуле этого соединения. Какое из трех соединений, представленных на диаграмме, имеет данную структуру? Определите координационные числа и полиэдры анионов и катионов в этой структуре.
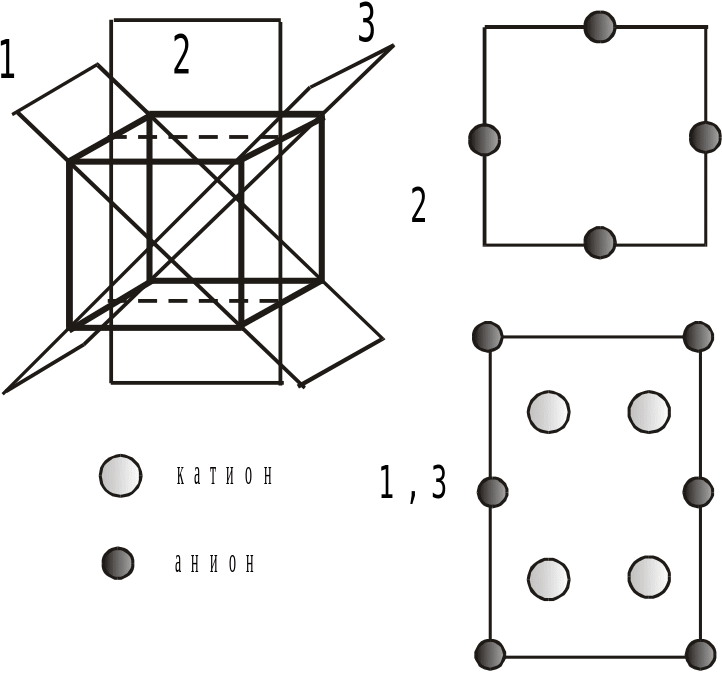
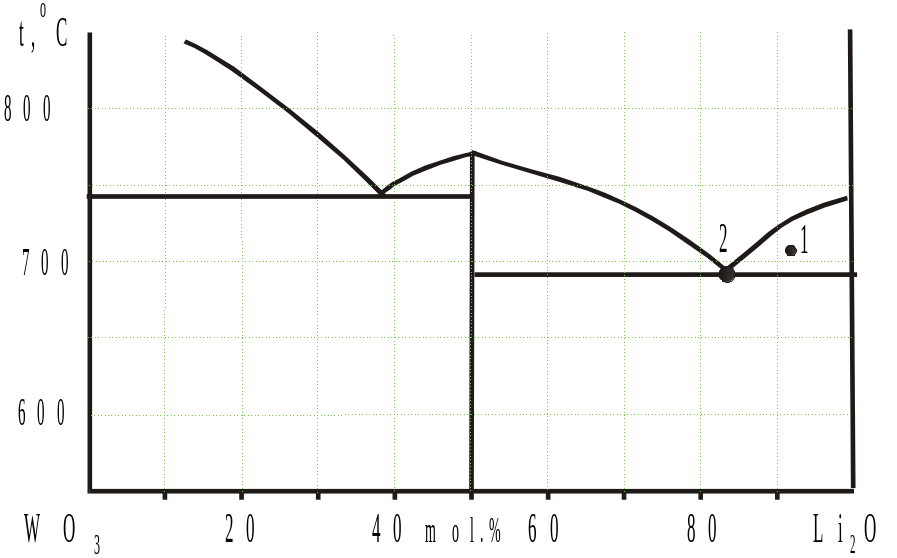
Рис.1.
Рис.2 (7 баллов)
II cеместр 2002/03 учебного года. Контрольная работа N1. Вариант 4.
Напишите уравнения следующих химических превращений:
X
 2 LiH
2 LiH
to
L

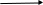 i2SO4 X1 Li2CO3 X2 LiOH
i2SO4 X1 Li2CO3 X2 LiOH
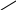

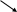
B aCl2 Y1
Y2 Ba(NO3)2
aCl2 Y1
Y2 Ba(NO3)2
Xi -вещества, содержащие Li, Yi -вещества, содержащие Ba. (8 баллов)
2. Изобразите схематически на графике в координатах (Ео(M+(р-р)/M(тв.) - порядковый номер М), как изменяются величины Ео M+(р-р)/M(тв.) для щелочных металлов (М= Li - Cs). Объясните эту закономерность. (3 балла)
3. При температуре 1242 К равновесное давление р(СO2) над карбонатом стронция составляет 0.1 атм. Используя данные таблицы, определите энергию кристаллической решетки оксида стронция. Считайте, что DrН0 и DrS0 не зависят от температуры.
Вещество |
DfН0, кДж/моль |
S0, Дж /мольК |
Вещество |
DfН0, кДж/моль |
S0 Дж /мольК |
C газ C алмаз C графит CO газ COCl2 газ CO2 газ Н газ Н+ газ Н+ р-р Н2 газ H2O газ
|
712.5 1.828 0 -110.5 -220.3 -393.5 218.0 1536.2 0 0 -241.8
|
158.0 2.4 5.7 197.6 283.9 213.8 114.6 108.8 0 132.1 188.7 |
H2O ж. O газ O2 газ O2- газ OH- р-р Sr газ Sr крист. Sr2+ газ Sr2+ р-р SrCO3 крист. SrО2 крист. SrО крист. |
-285.8 246.8 0 834.6 -230.2 164.0 0 1790.6 -545.5 -1220.1 -651.7 - |
70.1 160.9 205.0 - -10.9 135.1 53.1 - -26.3 97.1 43.1 54.4 |
(7 баллов)
4. На рис.1 приведена схема фазовой диаграммы двухкомпонентной системы ZnS – In2S3
