
- •Российский университет дружбы народов
- •К практическим занятиям по биохимии
- •Авторский коллектив:
- •Предисловие как пользоваться этим учебным пособием?
- •Список сокращений и условных обозначений
- •Техника безопасности при работе в биохимической лаборатории
- •1. Общие требования безопасности
- •Классификация химических реактивов в биохимической лаборатории
- •2. Требования безопасности перед началом работ
- •3. Требования безопасности во время работы
- •4. Требование безопасности в аварийных ситуациях
- •5.Требование безопасности по окончании работы
- •Раздел 1: Аминокислоты и простые белки Введение
- •1.1 Проверка знаний по органической химии
- •1.2. Цветные реакции на белки и аминокислоты. Реакции осаждения и денатурации белков а. Цветные реакции на белки и аминокислоты
- •Б. Реакции осаждения и денатурации белков
- •1.3. Количественное определение белка биуретовым методом. Построение калибровочных кривых
- •1 .4. Диализ белков. Бумажная хроматография аминокислот
- •А. Диализ
- •1.5. Коллоквиум I по теме «Аминокислоты и простые белки»
- •Раздел 2: Сложные белки, нуклеиновые кислоты и ферменты Введение
- •2.1 Действие амилазы на крахмал. Влияние температуры на активность амилазы а. Действие амилазы на крахмал
- •Б. Изучение влияния температуры на скорость ферментативной реакции
- •2.2. Количественное определение активности щелочной фосфатазы в сыворотке крови с п-нитрофенилфосфатом
- •2.3. Коллоквиум II по теме: «Сложные белки, нуклеиновые кислоты и ферменты» Вопросы, для самостоятельной подготовки
- •Варианты письменной части коллоквиума
- •Варианты заданий на компьютерном тестировании
- •Правильные ответы
- •Раздел 3: Витамины, липиды, гормоны Введение
- •3.1. Количественное определение витаминов с и р.
- •3.3. Влияние гормонов на содержание глюкозы в крови
- •3.4. Коллоквиум III по теме «Витамины, липиды, гормоны»
- •Раздел 4: Метаболизм. Биоэнергетика клеток. Химия и обмен углеводов Введение
- •4.1. Специфичность действия ферментов распада углеводов: амилазы и сахаразы
- •4.2. Количественное определение глюкозы. Построение «сахарных кривых»
- •4.3. Определение активности сукцинатдегидрогеназы в мышцах. Количественное определение пирувата в моче
- •4.4 Коллоквиум IV по теме: «Метаболизм. Биоэнергетика клеток. Химия и обмен углеводов»
- •Правильные ответы
- •Раздел 5: Обмен липидов и его регуляция Введение
- •5.1. Кинетика действия липазы.
- •5.2. Количественное определение фосфатидилхолинов (лецитинов) по фосфору
- •I. Приготовление рабочего раствора сыворотки.
- •II. Определение концентрации фосфатидолхолинов по содержанию фосфора.
- •5.3. Количественное определение холестерина в сыворотке крови
- •5.4. Количественное определение малонового диальдегида
- •5.5. Коллоквиум по теме «Обмен липидов»
- •Раздел 6: Переваривание белков и обмен аминокислот
- •6.1. Количественный анализ желудочного сока. Определение свободной, связанной, общей соляной кислоты и общей кислотности желудочного сока.
- •6.2. Количественное определение аспартатаминотрансферазы и аланинаминотрансферазы в сыворотке крови
- •6.3. Доказательство проявления активности аланин-аминотрансферазы (АлАт) методом бумажной хроматографии
- •6.4. Экспресс-метод определения повышенного содержания фенилаланина в плазме крови
- •6.5. Количественное определение мочевины в моче ферментативным уреазным/фенол-гипохлоритным методом
- •6.6. Количественное определение креатинина в моче
- •6.7. Коллоквиум по теме: «Обмен простых белков» Вопросы, для самостоятельной подготовки
- •Варианты письменной части коллоквиума
- •Правильные ответы
- •Раздел 7: Обмен хромопротеинов и нуклеопротеинов. Биохимия крови и мочи. Биосинтез нуклеиновых кислот и белков. Введение
- •7.1. Определение общего билирубина в сыворотке крови
- •7.2. Количественное определение мочевой кислоты в моче
- •7.3. А. Определение активности -амилазы в моче
- •7.3. Б. Составные части мочи в норме и при патологии
- •7.4. Определение активности холинэстеразы в сыворотке крови
- •7.5. Определение активности лактатдегидрогеназы в сыворотке крови
- •7.6. Коллоквиум по теме: «Обмен хромопротеинов и нуклеопротеинов. Биохимия крови и мочи. Биосинтез нуклеиновых кислот и белка». Вопросы, для самостоятельной подготовки
- •Варианты письменной части коллоквиума
- •Правильные ответы
- •Раздел 8: Подготовка к экзамену
- •8.1. Основные вопросы, выносимые на обсуждение
- •8.2. Пример экзаменационного тестового задания по курсу биохимии
- •59. Найти соответствие между процессом и его графическим изображением
- •60. Цикл мочевинообразования установил
- •Ответы к экзаменационному тесту
- •Раздел 9: Приложения
- •9.1. Термины, различающиеся по смыслу, но сходные по написанию и звучанию
- •9.2. Стандартные биохимические наборы и реактивы, используемые в практикуме
- •9.3. Рекомендуемая литература
- •Содержание
- •Раздел 7: Обмен хромопротеинов и нуклеопротеинов. Биохимия крови и мочи. Биосинтез нуклеиновых кислот и белков. 126
- •Раздел 8: Подготовка к экзамену 148
- •Раздел 9: Приложения 161
1.3. Количественное определение белка биуретовым методом. Построение калибровочных кривых
Определение концентрации белка проводят в научных учреждениях при изучении, выделении и очистке белков; в промышленности в процессе получения ферментов, пищевых белков, белковых лекарственных препаратов; в медицинских биохимических лабораториях для оценки состояния печени и почек.
Существует много разных методов количественного определения белков. Среди них широкое распространение получили колориметрические методы, основанные на способности белков давать окрашенные комплексы с рядом реактивов (цветные реакции). Среди этих методов наиболее распространены биуретовый метод и его модификация (метод Лоури1).
Цель работы
Освоить работу фотоэлектроколориметра (ФЭК). Научиться строить стандартные калибровочные кривые. Определить содержание белка в пробе с неизвестной концентрацией.
Принцип метода
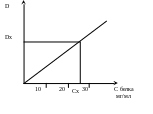
Биуретовый метод основан на образовании окрашенного в фиолетовый цвет комплекса пептидных связей белка с ионами двухвалентной меди в щелочной среде (биуретовая реакция). Интенсивность развивающейся окраски раствора прямо пропорциональна концентрации белка и определяется фотометрически. Для количественного определения белка измеряют интенсивность окраски стандартных растворов белка с известной концентрацией (величину оптической плотности Dст). По полученным данным строят график зависимости оптической плотности окрашенных растворов от концентрации в них белка (стандартную калибровочную кривую). На оси ординат всегда откладывают величину D как функцию от задаваемых значений (см. рисунок).
Измеряют оптическую плотность Dх окрашенного раствора с неизвестной концентрацией белка и по стандартной кривой определяют в нем концентрацию белка. В качестве стандартного белка обычно используют раствор сывороточного альбумина.
Выполнение работы
Реактивы, мл |
Контроль |
Стандартный белок 10 мг/мл |
Стандартный белок 20 мг/мл |
Стандартный белок 30 мг/мл |
Неизвестный белок Х мг/мл |
||
Раствор сывороточного альбумина, мл |
—
|
0,2 |
0,2 |
0,2 |
0,2 |
||
Н2О, мл |
0,2 |
— |
— |
— |
— |
||
Биуретовый реактив*, мл |
5 |
5 |
5 |
5 |
5 |
||
Перемешивают и инкубируют 30 минут при комнатной температуре |
|||||||
Фотометрируют против Н2О ( = 545 нм, толщина кюветы 1 см). D545 |
|
|
|
|
|
||
Dст – Dк; Dх – Dк |
|
|
|
|
|
||
*Биуретовый реактив: исходный концентрат (медь сернокислая – 120 ммоль/л, калий иодистый – 300 ммоль/л, калий-натрий виннокислый – 320 ммоль/л, гидроксид натрия –3 моль/л) разводят перед работой 1:19
 Оформление
работы
Оформление
работы
В рабочей тетради записать и заполнить таблицу; построить стандартную кривую и определить по ней концентрацию белка в неизвестном растворе.
Выводы
Т естовые
задания по теме: «Аминокислоты и простые
белки»
естовые
задания по теме: «Аминокислоты и простые
белки»
1) Ответить на каждый вопрос однозначно: «да» или «нет»
Имидазольное кольцо гистидина содержит 1 атом азота.
N-концевая аминокислота в дипептиде гистидиллизин - гистидин.
С-концевая аминокислота в трипептиде серилпролилглицин - глицин.
Альбумины сыворотки крови выполняют транспортную функцию.
Пролин содержит имино-группу.
Аспарагиновая кислота является производным янтарной кислоты.
Все ли пептиды дают положительную биуретовую реакцию?
Зависит ли интенсивность окраски вещества в растворе от его концентрации?
Можно ли разделить белки методом высаливания, используя сернокислую медь (сульфат меди)?
Встречаются ли в организме человека аминокислоты, которые не входят в состав белков?
Участвует ли ε-NH2-группа лизина в образовании пептидной связи в белках?
Обладают ли радикалы серина и валина гидрофильными свойствами?
2) Выбрать один правильный ответ
Аминокислота с незаряженным радикалом: треонин лизин аргинин гистидин глутаминовая кислота |
Для определения оптической плотности синего раствора используют светофильтр: голубой желтый красный зеленый синий |
3) Найти соответствие
АМК |
Химическая группа в составе радикалов |
метионин серин аргинин цистеин аспарагин |
А. гидроксильная Б. амидная В. тиометильная Г. гуанидиловая Д. сульфгидрильная |
