
- •Аннотация
- •1. Введение
- •1.1 Общие правила выполнения лабораторных работ.
- •1.2. Лабораторное оборудование.
- •1.3 Вычисления.
- •1.4 Количество и концентрация вещества.
- •Общие указания по выполнению лабораторных работ.
- •Работа 1. Ознакомление с некоторыми операциями лабораторной практики и измерительными приборами.
- •Работа 2. Классы неорганических соединений.
- •Работа 3. Определение молярной массы диоксида углерода.
- •Работа 4. Электронная структура атомов и одноатомных ионов.
- •Работа 5. Кинетика химических реакций.
- •Работа 6. Химическое и адсорбционное равновесие.
- •Работа 7. Концентрация растворов.
- •Работа 8. Свойство водных растворов электролитов.
- •Работа 9.Гидролиз солей.
- •Работа 10. Окислительно-восстановительные реакции.
- •Работа 11. Основы электрохимии.
- •Работа 12. Электролиз.
- •Работа 13. Общие химические свойства металлов.
- •Работа 14. Свойства d-элементов 4-го периода.
- •Работа 15. Свойства элементов, применяемых в полупроводниковой технике.
- •Работа 16. Определение жесткости и умягчение воды.
- •Работ 17 Органические соединения.
- •Работа. 18. Свойства элементов подгруппыViв иViiв
- •Работа 19. Свойства элементов подгруппыViiib.
- •Работа 20. Свойства элементов подгруппыIva.
- •Работа 21, Свойства элементовVAиVia.
Работа 10. Окислительно-восстановительные реакции.
Цель работы - ознакомление с окислительно-восстановительными свойствами металлов, неметаллов и их соединений, освоение методики составления уравнений окислительно-восстановительных процессов.
Реакции, протекания которых связано со смещением или полным переходом электронов от одних атомов к другим, называют окислительно-восстановительными.
Число электронов, смещенных от атома (иона) данного элемента или к атому (иону) данного элемента в соединении, называют степенью окисления. Степень окисления может быть положительной (электроны смещены от атома или иона) и отрицательной (электроны сменены к атому или иону).
Процесс
отдачи электронов, т.е. повышения степени
окисления элемента, называют окислением,
а вещества, отдающие электроны -
восстановителями. К типичным восстановителям
относятся простые вещества, атомы
которых характеризуются невысокой
электроотрицательностью (металлы,
водород, углерод), некоторые анионы (![]() ,
,![]() ,
,![]() и др.); катионы, у которых степень окисления
может возрастать (
и др.); катионы, у которых степень окисления
может возрастать (![]() ,
,![]() и др.).
и др.).
Процесс
присоединения электронов, т.е. понижения
степени окисления, называют восстановлением,
а вещества, принимающее электроны,
называют окислителями. К типичным
окислителям относятся простые вещества,
атомы которых характеризуются высокой
электроотрицательностью (элементы VI и
VII
групп главных подгрупп), катионы с
высокой степенью окисления (![]() ,
,![]() ,
,![]() ),
анионы, в которых электроположительный
элемент имеет высокую степень окисления
(
),
анионы, в которых электроположительный
элемент имеет высокую степень окисления
(![]() ,
,![]() ,
,
![]() ),
высшие оксиды, а также пероксиды.
),
высшие оксиды, а также пероксиды.
Окислительно-восстановительные реакции - это одновременно протекающие процессы окисления и восстановления. Реакции, в которых окислители и восстановители представляют собой разные вещества, называют межмолекулярными. Если окислителями и восстановителями служат атомы или ионы одной и той же молекулы, то такие реакции называют внутримолекулярными.
Составление окислительно-восстановительных реакций требует строгого соблюдения правил, изложенных в данном разделе, что поможет написать любую окислительно-восстановительную реакцию. Для этого существуют два метода электронного баланса и ионно-электронной полуреакции. Первый может пригодиться только тогда, когда известны все продукты реакции и исходные вещества, при этом основное правило - установить степени окисления элементов, которые в результате реакции изменили свою степень окисления, а затем для этих элементов записать уравнение электронного баланса, расставить коэффициенты в уравнении реакции и по кислороду проверить правильность написания уравнения.
Пример:
![]()
Установим степени окисления у всех элементов:
![]()
видно, что степень окисления изменили два элемента - железо и марганец. Составим для них уравнение электронного баланса:
![]()
расставим коэффициенты около окислителя и восстановителя:
![]()
а теперь методом "пинг-понга" устанавливаются последовательно коэффициенты в левой и правой части у всех остальных элементов так, чтобы последним уравнивался водород.
![]()
Справа и слева имеется по 80 атомов кислорода, следовательно, коэффициенты в уравнении расставлены правильно.
Метод полуреакций, или ионно-электронный, применяется только в том случае, когда неизвестны все вещества, входящие в уравнение. Этот метод решения окислительно-восстановительных реакций намного мощнее метода электронного баланса, он позволяет написать продукты и расставить коэффициенты в реакции, если известны только исходные вещества и среда, в которой происходит реакция.
Последовательность действий при написании окислительно-восстановительных реакций ионно-электронным методом следующая:
необходимо установить, какое вещество восстановитель, а какое окислитель;
в соответствии с ниже приведенными схемами записываются полуреакции (в ионном виде) с окислителями и восстановителями. Заряд в этих реакциях уравнивается прибавлением или отниманием электронов в левой части уравнения, необходимо при этом учесть, что:
окислитель превращается в ион с низшей степенью окисления;
восстановитель превращается в соединение с высшей степенью окисления;
находится число, равное наименьшему общему кратному между числом электронов в полуреакциях окисления и восстановления;
полуреакции складываются;
записывается уравнение из противоионов для левой части и такое же уравнение для правой части;
записывается суммарное молекулярное уравнение реакции.
Схемы для ионно-электронного метода (полуреакций)
Если в исходных веществах больше кислорода, то в продуктах реакций на каждый атом кислорода имеем:
в кислой среде молекулу воды
![]()
в щелочной' и нейтральной среде – гидроксогруппу
![]()
Если в исходных веществах меньше кислорода, то в продуктах на каждый атом кислорода имеем:
в кислых и нейтральных средах
![]()
в щелочной среде
![]()
Превращение, аниона перманганата в окислительно-восстановительных процессах:
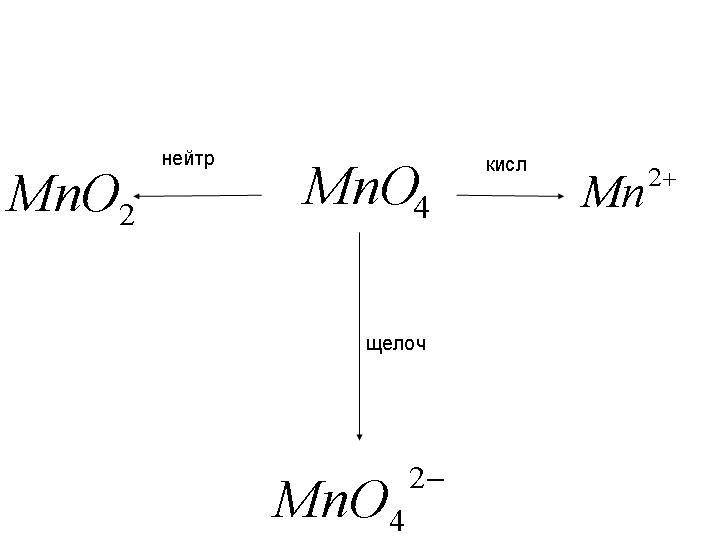
Взаимодействие концентрированной серной кислоты с металлами:

Превращения бихромат - иона в окислительно-восстановительных процессах:

Из неметалла образуется кислота с высшей степенью окисления неметалла.
Разберем принцип написания окислительно-восстановительных реакций ионно-электронным методом на следующем примере:
![]()
Окислителем
может быть только бихромат калия, т.к.
в этом соединении он имеет высшую степень
окисления +6.
![]() добавлена для создания кислой среды,
следовательно, восстановителем является
ион тиоцианата, в котором каждый элемент
является восстановителем.
добавлена для создания кислой среды,
следовательно, восстановителем является
ион тиоцианата, в котором каждый элемент
является восстановителем.
Запишем реакцию окисления восстановителя в ионном виде:
![]()
(углерод
превращается в
![]() ,
как этого требует правило превращения
восстановителя в анион высшей степени
окисления элемента). В кислой среде
недостаток кислорода в исходном веществе
требует добавления к левой части
уравнения воды:
,
как этого требует правило превращения
восстановителя в анион высшей степени
окисления элемента). В кислой среде
недостаток кислорода в исходном веществе
требует добавления к левой части
уравнения воды:
![]()
уравновесим
заряд (![]() добавили,
т.к. необходимо в левую часть прибавить
7 атомов кислорода)
добавили,
т.к. необходимо в левую часть прибавить
7 атомов кислорода)
![]()
Запишем процесс восстановления окислителя, воспользовавшись вышеприведенной схемой:
![]()
В исходном веществе больше кислорода, среда кислая, следовательно, к свой части необходимо добавить - протоны:
![]()
уравновесим заряд
![]()
и в результате получим

после сложения получим ионное уравнение:
![]()
после удаления молекул воды и протонов водорода получим:
![]()
Напишем уравнение из противоионов:
![]()
Суммарное уравнение в молекулярном виде
![]()
Обратите
внимание, что один из продуктов реакции
(![]() )
может реагировать с серной кислотой,
которую обычно добавляют в избытке:
)
может реагировать с серной кислотой,
которую обычно добавляют в избытке:
![]()
но, так как в реакции получилось 6-молекул карбоната калия, то последнее уравнение необходимо умножить на 6 и эти два уравнения сложить в результате получим:
![]()
Приведем одинаковые вещества под один коэффициент:
![]()
Экспериментальная часть.
ОПЫТ 1. Окисление алюминия ионами водорода
Внесите
кусочек алюминия в 2Н раствор
![]() .
Наблюдайте окисления и составьте
уравнение происходящей
окислительно-восстановительной реакции.
Дайте сравнительную характеристику
окислительно-восстановительных свойств
атомов и ионов алюминия и водорода.
.
Наблюдайте окисления и составьте
уравнение происходящей
окислительно-восстановительной реакции.
Дайте сравнительную характеристику
окислительно-восстановительных свойств
атомов и ионов алюминия и водорода.
ОПЫТ 2. Окисление катиона железа (II) хлором.
Налейте
в пробирку 5-6 капель свежеприготовленного
раствора соли железа (II)
и прибавьте две капли хлорной воды.
Содержимое пробирки взболтайте и
прибавьте в нее 1-2 капли раствора
![]() или
или
![]() .
Окрашивание раствора в красный цвет
свидетельствует об окислении ионов
.
Окрашивание раствора в красный цвет
свидетельствует об окислении ионов
![]() в
в![]() .
Составьте электронно-ионное уравнение
реакции окисления и восстановления.
.
Составьте электронно-ионное уравнение
реакции окисления и восстановления.
ОПЫТ 3. Окисление иодид - ионов ионами железа (III).
В
пробирку налейте 5-6 капель раствора
железа (III) и одну каплю раствора
![]() или
или![]() .
Содержимое пробирки разбавьте
дистиллированной водою до слабо-желтого
цвета и введите 1-2 капли раствора
крахмала. Появление синей окраски
свидетельствует о наличии в растворе
свободного иода. Реакция выражается
схемой:
.
Содержимое пробирки разбавьте
дистиллированной водою до слабо-желтого
цвета и введите 1-2 капли раствора
крахмала. Появление синей окраски
свидетельствует о наличии в растворе
свободного иода. Реакция выражается
схемой:
![]()
Составьте электронно-ионное уравнение процессов окисления и восстановления и уравнение реакции.
ОПЫТ
4. Окисление гидроокиси
![]() (II)
перекисью водорода.
(II)
перекисью водорода.
Налейте
в пробирку 3-4 мл свежеприготовленного
раствора соли железа (![]() или
или![]() )
и прибавьте к нему 2-3 мл раствора щелочи
(
)
и прибавьте к нему 2-3 мл раствора щелочи
(![]() или
или![]() ).
Заметьте цвет осадка. Когда гидроокись
железа сядет на дно пробирки, осторожно
слейте жидкости прибавьте 1-2 капли
Раствора
).
Заметьте цвет осадка. Когда гидроокись
железа сядет на дно пробирки, осторожно
слейте жидкости прибавьте 1-2 капли
Раствора![]() .
Наблюдайте изменение осадка. Реакция
выражается схемой:
.
Наблюдайте изменение осадка. Реакция
выражается схемой:
![]()
Составьте, электронно-ионное уравнение процессов окисления и восстановления и уравнение реакции.
ОПЫТ
5. Окисление ионов
![]() перекисью водорода.
перекисью водорода.
В
пробирку налейте 5-6 капель раствора
соли хрома (![]() ,
,![]() )
и прибавляйте по каплям 6Н раствор щелочи
(
)
и прибавляйте по каплям 6Н раствор щелочи
(![]() или
или![]() )
до тех пор, пока первоначально выпавший
осадок
)
до тех пор, пока первоначально выпавший
осадок![]() полностью растворится в результате
образования хромита. Отметьте цвет
раствора. К полученному раствору хромита
добавьте несколько капель раствора
полностью растворится в результате
образования хромита. Отметьте цвет
раствора. К полученному раствору хромита
добавьте несколько капель раствора![]() и слегка нагрейте раствор. Переход
зеленого цвета в желтый свидетельствует
о появлении в растворе ионов
и слегка нагрейте раствор. Переход
зеленого цвета в желтый свидетельствует
о появлении в растворе ионов![]() .
.
Реакция может быть выражена суммарной схемой:
![]()
Составьте электронно-ионные уравнения процессов окисления и восстановления и уравнение реакции.
ОПЫТ
6. Окисление
![]() ионами
ионами![]() .
.
В
пробирку налейте 5-6 капель раствора
перманганата калия и только же 2Н раствора
серной кислоты. Затем пипеткой по каплям
приливайте свежеприготовленный раствор
соли железа (II) до полного обесцвечивания
раствора. Обесцвечивание раствора
свидетельствует о восстановлении ионов
![]() в ионы
в ионы![]() .
В обесцвеченный раствор добавьте
несколько капель раствора
.
В обесцвеченный раствор добавьте
несколько капель раствора![]() или
или![]() и убедитесь, что ионы
и убедитесь, что ионы![]() окислились в ионы
окислились в ионы![]() .
Реакция выражается схемой:
.
Реакция выражается схемой:
![]()
Составьте электронно-ионное уравнение процессов окисления и восстановления и уравнение реакции.
ОПЫТ 7. Реакции внутримолекулярного окисления и восстановления.
Положите
в пробирку такое количество
![]() ,
чтобы оно покрыло ее дно, и нагрейте,
пока с помощью тлеющей лучинки не
определите выделение кислорода. Составьте
электронно-ионное уравнение процессов
окисления и восстановления и уравнение
реакции, зная, что в результате реакции
образовывается молекулярный кислород,
диоксид марганца и манганат калия
,
чтобы оно покрыло ее дно, и нагрейте,
пока с помощью тлеющей лучинки не
определите выделение кислорода. Составьте
электронно-ионное уравнение процессов
окисления и восстановления и уравнение
реакции, зная, что в результате реакции
образовывается молекулярный кислород,
диоксид марганца и манганат калия![]() .
.
Контрольные вопросы и задачи
Чем отличается реакция окисления-восстановления от других реакций?
Какие вещества называются окислителями, а какие - восстановителями?
В каких группах периодической системы элементов Менделеев расположены элементы с ярко выраженными окислительными свойствами?
Как изменяется окислительное число окислителя и восстановителе в результате окисления-восстановления?
Какой из галогенов является самым сильным окислителем: фтор, хлор, бром, иод?
Как изменяется электроотрицательность элементов в главных группах и в периодах?
Окислительные или восстановительные свойства проявляют следующие частицы:
 ?
Приведите примеры реакций.
?
Приведите примеры реакций.Каковы окислительно-восстановительные свойства воды? Составьте ионно-молекулярные уравнения для воды как окислителя и как восстановителя.
В чем заключается метод электронного баланса?
Как составить реакцию окисления-восстановления с помощью метода полуреакций?
