
Молекулярная физика
МКТ |
Основное уравнение МКТ |
Газовые законы |
Термодинамика |
Молярная масса M = m0NA (NA = 6*1023) M = Mr*10-3 Относительная молекулярная масса
Mr
=
Масса молекулы
m0 =
Масса вещества m = m0N Количество вещества
=
Число молекул
N =
N = NA Концентрация молекул
n =
Уравнение состояния идеального газа pV = kT R = NAk = 8,31
pV =
pV = RT
|
Давление идеального газа
p =
p = nkT =
k = 1.38*10-23
p =
p = kT , T = t + 273 Средняя кинетическая энергия
Ek
=
Средняя квадратичная скорость
v2 = Плотность
=
Молярная масса
M =
Объем V
= |
I газовый закон (Б-М) m, T = const, изотермический
I m, V = const, изохорный
I m, p = const, изобарный
|
Внутренняя энергия и.г. U = NEk = RT = pV = RT = Аг Работа газа Aг = pV, Аг = Q1 – Q2 при расширении Аг > 0, при сжатии Аг < 0. Работа внешних сил А = -Аг = p(V2 – V1) при сжатии А > 0, при расширении А < 0. Количество теплоты Qнагр = cm(t2 – t1), Qсгор = qm Qпар = rm, Qкон = - rm Qпл = m, Qкр = - m I закон термодинамики U = A + Q, Q = U + Aг I закон в изопроцессах 1. изохорный V = 0 3. изобарный p = 0 U = Q, т.к. А = 0 Q = U + Aг
п п 2. изотермический вн. энергии Т = 0, значит U = 0 4. адиабатный Q = 0 Q = Aг U = A Q газ расширяется A > 0, Aг < 0. Q газ сжимается A < 0, Aг > 0. КПД тепловой машины, цикла Карно
=
Влажность абс =
,
отн =
|

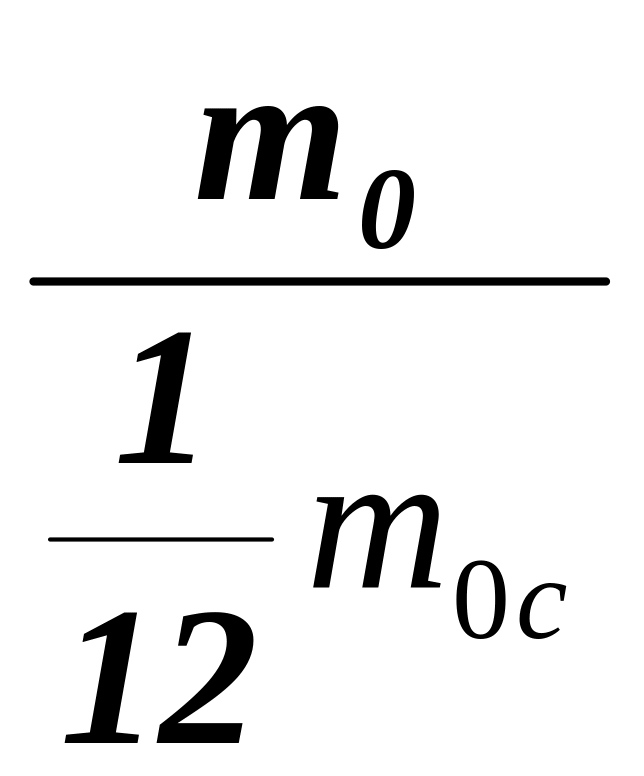 ,
m0c
= 10995*10-26
,
m0c
= 10995*10-26 I
газовый закон(Шарля)
I
газовый закон(Шарля)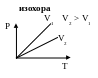 II
газовый закон (Г-Л)
II
газовый закон (Г-Л)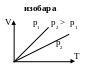
 ри
нагревании U
тепло идет на работу
ри
нагревании U
тепло идет на работу
 ри
охлаждении U
газа и изменение
ри
охлаждении U
газа и изменение
 > 0, Aг > 0,
при сжатии U
> 0, Aг > 0,
при сжатии U
 < 0, Aг < 0,
при расширении U
< 0, Aг < 0,
при расширении U